Человеку, старающемуся быть в «медицинском тренде», не пропускающему ни одной программы о здоровье начиная с попсовых творений Елены Малышевой и Сергея Агапкина и заканчивая замечательным циклом фильмов на канале «Дискавери» (хотя лучше бы в обратном порядке), скорее всего о гемофилии будет известно не много. История об исцелении Григорием Распутиным цесаревича Алексея да смутные воспоминания времен школьных уроков естествознания — это в лучшем случае. Что поделать, не пользуется гемофилия народной популярностью, уж очень редкое это заболевание, не чета насморку да ангине.
ачит, самое время закрасить белые пятна неведения яркой палитрой познания. Тем более что есть в генетических заболеваниях нечто притягивающее интерес. Возможно, причиной этому является ореол фатализма, сопровождающий любые наследственные девиации. Ведь если тем же пресловутым насморком человек заражается, просто оказавшись не в то время не в том месте, или в связи с собственной неосмотрительностью, то в случае с генетическими отклонениями вины самого человека никакой нет. Просто так сошлись звезды, или, что ближе к нашей сегодняшней теме, хромосомы.
Гемофилия: что это?
Как складывается хромосомный пасьянс гемофилии? Как известно, наш организм представлен сонмом различных клеток. Основа клетки — ее ядро — определяет индивидуальное развитие каждого человека. Хранилищем этой наследственной информации в ядре являются парные нитевидные структуры — хромосомы. Какая самая явная личностная характеристика индивида? Правильно, его пол, который определяется конкретной парой хромосом, обозначаемых буквами X и Y. Женские клетки содержат ХХ-хромосомную пару, мужские — XY. Каждый из родителей передает своему будущему ребенку по одной хромосоме из этой пары, посредством чего и складывается «гендерный пасьянс», определяющий пол малыша. Таким образом, путем пары нехитрых математических пар получаются четыре вероятных сочетания родительских хромосом, два из которых обрекают будущее творение рода человеческого нести на себе мужской крест, а два других предопределяют появление на свет хранительницы домашнего очага.
Структурной единицей хромосомы является ген. Генный состав Х-хромосомы, помимо того, что детерминирует пол человека, отвечает еще и за образование факторов свертывания крови VIII, IX, XI.
Справочно: факторы свертываемости крови — группа веществ, в основном белков, содержащихся в плазме крови и в тромбоцитах и обеспечивающих свертываемость крови.
Получая в наследство половую хромосому с дефектными генами, гемофилик приобретает и проблемы с факторами свертывания крови, что в свою очередь чревато тяжелыми кровотечениями.
Вероятность гемофилии гораздо выше у представителей мужского пола, т.к. у женщин, даже если они имеют одну хромосому с гемофильными генами, вторая Х-хромосома сможет обеспечить производство необходимого количества факторов свертывания. У мужчин же только одна Х-хромосома, и если в ней обнаруживаются генные неполадки, то пиши пропало: он будет страдать длительными кровотечениями. т.к. его вторая половая Y-хромосома не задействована в производстве факторов свертывания крови.
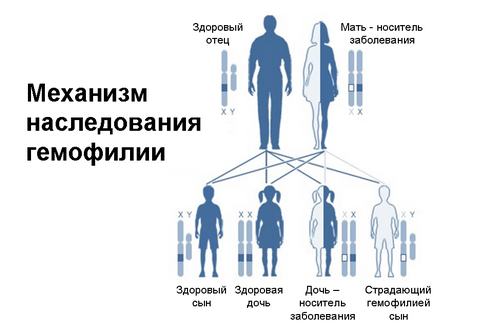
У страдающего гемофилией отца все дочери будут носительницами этого заболевания. У сыновей (при условии здоровой матери) никаких проблем со свертываемостью крови не будет. Если слепая судьба сведет мужчину-гемофилика с женщиной, которая является носителем этого заболевания (с одной нормальной Х-хромосомой и одной дефектной), то тогда гемофилия может проявиться не только у их потенциального сына, но и у дочери. Чаще всего подобная ситуация характерна для близкородственных браков.
Виды гемофилии
Гемофилии дифференцируются в зависимости от отсутствия (или недостаточной активности) конкретного фактора свертывания:
- при отсутствии VIII фактора свертывания под названием антигемофильный глобулин развивается гемофилия А: самый распространенный вид гемофилии;
- при отсутствии IX фактора свертывания крови (альтернативное название — фактор Кристмаса) развивается гемофилия В;
- при отсутствии XI фактора свертывания крови развивается самый редкий вид этого наследственного заболевания — гемофилия С.
Все эти виды гемофилии имеют схожие симптомы, но их лечение содержит в себе некоторые отличия, поэтому важно диагностировать конкретную разновидность заболевания.
Признаки гемофилии
К основным симптомам и признакам гемофилии относятся:
- постоянные стойкие кровотечения, начинающиеся спустя час-два после пореза, удаления зуба или какой-нибудь другой травмы. Бывают и кровотечения, не связанные с механическим повреждением (спонтанные);
- обширные гематомы даже после незначительных повреждений;
- частые кровотечения из носа и десен (чистка зубов превращается в кровавое зрелище);
- серьезным последствием гемофилии являются внутрисуставные кровотечения: попадание в сустав крови сопровождается нестерпимой болью, отечностью и нарушением мобильности сустава. Любое последующее внутрисуставное кровотечение может деформировать его и вызвать необратимое нарушение подвижности;
- кровь в «расходных» субстанциях — моче и кале;
Кровоизлияние в головной и спинной мозг, вероятность которого при гемофилии несравненно выше, чем в норме, может стать причиной летального исхода.
Диагностика гемофилии
Как и любое наследственное заболевание, гемофилия требует тщательного изучения генеалогического древа на предмет наличия в роду (в особенности — у ближайших родственников) данного заболевания. В частности, обращается внимание на наличие по материнской линии мужчин с повышенной кровоточивостью.
Так как гемофилия непосредственным образом связана с кровью, то анализ крови также имеет чрезвычайно большое значение в ее диагностике. В образце крови, взятом у пациента, определяют время свертывания крови. Замедленная свертываемость крови может свидетельствовать о гемофилии. Определяется также количество факторов свертывания крови и их концентрация. Конкретный вид гемофилии определяется с помощью теста генерации тромбопластина или посредством ДНК-диагностики.
Лечение гемофилии
В период обострения кровотечений назначают переливание крови (гемотерапию), причем в зависимости от вида гемофилии лечение будет различаться. Так, при гемофилии А используют очищенный концентрат VIII фактора свертывания крови (торговые названия — Криопреципитат, Агемфил А, Бериате, Гемоктин, Октави, Фанди) либо переливание свежей или антигемофильной плазмы. При гемофилиях В и С вводят плазму, концентрат нативной плазмы и протромбиновый комплекс, включающий комбинацию из факторов свертывания крови II, VII, IX и X (торговые названия — Конайн 80, Протромплекс 600).
В случае возникновения необходимости хирургического вмешательства в первую очередь восполняют содержания недостающего фактора свертывания крови, и лишь после этого проводят операцию. Это особенно актуально при внутрисуставных кровотечениях, когда пункцию сустава с удалением излившейся крови проводят только после общей гемотерапии. После операции в рамках вспомогательной регенерирующей терапии используют физиолечение (грязевые ванны, водные процедуры и лечебную гимнастику).
При гемофилии следует с особой скрупулезностью остерегаться травм, оперативные вмешательства производить только по жизненно важным показаниям, проводя перед этим предварительную подготовку.
Источник: www.webmedinfo.ru
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Гематурия при гемофилии может возникать самопроизвольно или вследствие травм поясничной области. При этом отмечаются дизурические явления, при образовании кровяных сгустков в мочевыводящих путях — приступы почечной колики. У больных с гемофилией нередко обнаруживаются пиелоэктазия, гидронефроз, пиелонефрит.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Источник: www.KrasotaiMedicina.ru
Как работают гены и что такое генетические заболевания?
 Рассмотрим понятие рецессивных и доминантных генов, поскольку это необходимо для дальнейшего понимания особенностей проявления гемофилии. Дело в том, что все гены подразделяют на доминантные и рецессивные. Как известно, каждый человек получает набор генов от обоих родителей – матери и отца, то есть имеет два варианта одного и того же гена. Например, два гена цвета глаз, два – цвета волос и прочее. При этом каждый из генов может быть доминантным или рецессивным. Доминантный ген проявляется всегда и подавляет рецессивный, а вот рецессивный проявляется – только когда он есть в обеих хромосомах – материнской и отцовской. Например, ген карих глаз – доминантный, а ген голубых глаз – рецессивный. Это значит, что если ребенок получит от матери ген карих глаз, а от отца – ген голубых, то родится он с карими глазами, то есть доминантный ген кареглазости проявится и подавит рецессивный ген голубоглазости. Чтобы ребенок родился с голубыми глазами нужно, чтобы и от матери, и от отца он получил два рецессивных гена голубоглазости, только в этом случае проявится рецессивный признак – голубые глаза.
Рассмотрим понятие рецессивных и доминантных генов, поскольку это необходимо для дальнейшего понимания особенностей проявления гемофилии. Дело в том, что все гены подразделяют на доминантные и рецессивные. Как известно, каждый человек получает набор генов от обоих родителей – матери и отца, то есть имеет два варианта одного и того же гена. Например, два гена цвета глаз, два – цвета волос и прочее. При этом каждый из генов может быть доминантным или рецессивным. Доминантный ген проявляется всегда и подавляет рецессивный, а вот рецессивный проявляется – только когда он есть в обеих хромосомах – материнской и отцовской. Например, ген карих глаз – доминантный, а ген голубых глаз – рецессивный. Это значит, что если ребенок получит от матери ген карих глаз, а от отца – ген голубых, то родится он с карими глазами, то есть доминантный ген кареглазости проявится и подавит рецессивный ген голубоглазости. Чтобы ребенок родился с голубыми глазами нужно, чтобы и от матери, и от отца он получил два рецессивных гена голубоглазости, только в этом случае проявится рецессивный признак – голубые глаза.
Почему болезнь передается по женской линии, а болеют ею только мужчины?
 Вернемся к гемофилии. Особенность гемофилии состоит в том, что женщины являются носителями данной патологии, а болеют мужчины. Почему это так? Ген гемофилии является рецессивным и находится в половой Х – хромосоме. Его наследование сцеплено с полом. То есть для его проявления необходимо наличие двух Х – хромосом с такой мутацией. Однако у женщины имеется две половые Х хромосомы, а у мужчины Х и Y – хромосомы. Посему у женщины должна быть мутация в обоих Х – хромосомах, чтобы проявилась болезнь – гемофилия. Однако такой факт невозможен. Почему? Когда женщина беременеет девочкой с мутациями в обоих Х – хромосомах, на 4 неделе беременности, когда начинается процесс образования собственной крови плода, происходит выкидыш, поскольку такой плод нежизнеспособен. Поэтому девочка может родиться только с мутацией в одной Х – хромосоме. А в этом случае болезнь не проявится, так как доминантный ген второй Х – хромосомы не даст проявиться рецессивному, ведущему к гемофилии. Поэтому женщины являются только носителями гемофилии.
Вернемся к гемофилии. Особенность гемофилии состоит в том, что женщины являются носителями данной патологии, а болеют мужчины. Почему это так? Ген гемофилии является рецессивным и находится в половой Х – хромосоме. Его наследование сцеплено с полом. То есть для его проявления необходимо наличие двух Х – хромосом с такой мутацией. Однако у женщины имеется две половые Х хромосомы, а у мужчины Х и Y – хромосомы. Посему у женщины должна быть мутация в обоих Х – хромосомах, чтобы проявилась болезнь – гемофилия. Однако такой факт невозможен. Почему? Когда женщина беременеет девочкой с мутациями в обоих Х – хромосомах, на 4 неделе беременности, когда начинается процесс образования собственной крови плода, происходит выкидыш, поскольку такой плод нежизнеспособен. Поэтому девочка может родиться только с мутацией в одной Х – хромосоме. А в этом случае болезнь не проявится, так как доминантный ген второй Х – хромосомы не даст проявиться рецессивному, ведущему к гемофилии. Поэтому женщины являются только носителями гемофилии.
У мальчиков же одна хромосома Х, а вторая Y, которая не содержит гена гемофилии. В этом случае при наличии рецессивного гена гемофилии в Х – хромосоме, в Y – хромосоме нет другого доминантного гена, чтобы подавить этот рецессивный. Поэтому у мальчика ген проявляется, и он болеет гемофилией.
Гемофилия у женщины – «викторианская болезнь»
В истории известен только один пример женщины, болевшей гемофилией – это королева Виктория. Однако у нее данная мутация произошла уже после рождения, поэтому данный случай уникален и является исключением, которое подтверждает общее правило. В связи с данным исключительным фактом гемофилию называют также «викторианской болезнью» или «царской болезнью».
Какие бывают виды гемофилии?
 Гемофилия подразделяется на три типа А, В и С. При гемофилиях всех трех типов в крови нет необходимого количества белка, который называется фактором свертывания и обеспечивает свертывание крови, а также остановку кровотечения. Таких факторов свертывания всего 12. При гемофилии А в крови имеется недостаток фактора номер VIII, при гемофилии В – недостаток фактора номер IX, а при гемофилии С – фактора номер XI. Гемофилия типа А является классической и составляет 85% от всех видов гемофилий, на гемофилии В и С приходится, соответственно, 15% от общего числа всех случаев гемофилии. Гемофилия типа С стоит «особняком», так как ее проявления значительно отличаются от проявлений гемофилий В и А.Проявления же гемофилии А и В – одинаковы. Гемофилия С чаще всего встречается у евреев – ашкенази, причем могут болеть и женщины, а не только мужчины. На сегодняшний день гемофилия С вообще исключена из гемофилий, поэтому мы рассмотрим гемофилии А и В.
Гемофилия подразделяется на три типа А, В и С. При гемофилиях всех трех типов в крови нет необходимого количества белка, который называется фактором свертывания и обеспечивает свертывание крови, а также остановку кровотечения. Таких факторов свертывания всего 12. При гемофилии А в крови имеется недостаток фактора номер VIII, при гемофилии В – недостаток фактора номер IX, а при гемофилии С – фактора номер XI. Гемофилия типа А является классической и составляет 85% от всех видов гемофилий, на гемофилии В и С приходится, соответственно, 15% от общего числа всех случаев гемофилии. Гемофилия типа С стоит «особняком», так как ее проявления значительно отличаются от проявлений гемофилий В и А.Проявления же гемофилии А и В – одинаковы. Гемофилия С чаще всего встречается у евреев – ашкенази, причем могут болеть и женщины, а не только мужчины. На сегодняшний день гемофилия С вообще исключена из гемофилий, поэтому мы рассмотрим гемофилии А и В.
Что опасно для больных гемофилией?
Чем же проявляется гемофилия? Каковы ее признаки? Среди людей бытует мнение о том, что больной гемофилией должен оберегаться от малейших незначительных травм: порезов, укусов, царапин и прочее. Так как эти незначительные повреждения могут привести человека к смерти из-за кровопотери. Однако это явное преувеличение. Опасны для таких людей сильные травмы, сильные кровотечения, удаление зубов и хирургические операции. Конечно, не следует пренебрегать мерами безопасности – необходимо остерегаться ушибов, травм, порезов и т.д. Особенно опасными являются рваные раны. Особенно тщательно необходимо объяснить нормы поведения детям и подросткам, больным гемофилией, так как у детей и подростков высокая двигательная активность, много контактных игр, что может приводить к случайным травмам.
Врожденные и детские симптомы гемофилии
 При наличии гемофилии А или В у ребенка с рождения выявляются такие симптомы:
При наличии гемофилии А или В у ребенка с рождения выявляются такие симптомы:
- образование гематом (синяков) на самых различных местах (под кожей, в суставах, во внутренних органах). Эти гематомы образуются вследствие ударов, ушибов, травм, падений, порезов и т.д.
- кровь в моче
- обильное кровотечение вследствие травмы (удаление зубов, хирургические операции)
У новорожденных детей, как правило, имеются гематомы на голове, ягодицах, развивается кровотечение из перевязанной пуповины. У детей во время прорезывания зубов также часто возникают кровотечения и кровоизлияния. В детском возрасте кровотечения из носа и рта возникают довольно часто. Причиной носовых и ротовых кровотечений служит прикусывание щеки, языка, ковыряние в носу и ранение слизистой носа ногтем и т.д. Травма глаза с последующим кровоизлиянием в глаз может привести к слепоте. Обращает на себя внимание тот факт, что данные симптомы особенно выражены в раннем возрасте, а по мере взросления человека они становятся менее выраженными. Однако, главное свойство – основной симптом – склонность к кровотечениям, конечно, остается.
Когда развивается кровотечение у больных гемофилией?
 Для больных гемофилией характерно развитие кровотечения не только сразу после травмы, но и через некоторый промежуток времени развитие повторного кровотечения. Такое повторное кровотечение может развиться и через несколько часов, и через несколько суток. В силу данных причин, если больному гемофилией необходима операция или удаление зуба, то необходимо тщательно подготовить человека к операции и проводить ее только в случае крайней необходимости.Длительные кровотечения способствуют также формированию постгеморрагических анемий.
Для больных гемофилией характерно развитие кровотечения не только сразу после травмы, но и через некоторый промежуток времени развитие повторного кровотечения. Такое повторное кровотечение может развиться и через несколько часов, и через несколько суток. В силу данных причин, если больному гемофилией необходима операция или удаление зуба, то необходимо тщательно подготовить человека к операции и проводить ее только в случае крайней необходимости.Длительные кровотечения способствуют также формированию постгеморрагических анемий.
В каких областях чаще бывают кровоизлияния у больных гемофилией?
Частота кровоизлияний в суставы при гемофилии доходит до 70%, частота образования подкожных гематом (синяков) – 10-20%. И наиболее редко при гемофилии происходят кровоизлияния в центральную нервную систему и желудочно – кишечные кровотечения. Гематомы преимущественно локализуются в тех местах, где мышцы испытывают максимальную нагрузку – это мышцы бедер, спины и голени. Если человек использует костыли, то появляются гематомы и в подмышечных впадинах.
Гематомы для больных гемофилией обычное дело
 Гематомы больных гемофилией напоминают опухоль по внешнему виду и рассасываются в течение длительного промежутка времени, который составляет до 2 месяцев.Иногда, когда гематома долго не рассасывается, может возникнуть необходимость ее вскрыть. При образовании обширных гематом возможно сдавливание окружающих тканей и нервов, что приводит к нарушениям чувствительности и движений.
Гематомы больных гемофилией напоминают опухоль по внешнему виду и рассасываются в течение длительного промежутка времени, который составляет до 2 месяцев.Иногда, когда гематома долго не рассасывается, может возникнуть необходимость ее вскрыть. При образовании обширных гематом возможно сдавливание окружающих тканей и нервов, что приводит к нарушениям чувствительности и движений.
Гемоартроз – частое проявление гемофилии
 Кровотечение в суставы – это наиболее специфический для гемофилии симптом. Кровоизлияния в суставы являются причиной формирования у больных гемофилией заболеваний суставов – гемоартрозов. Данное поражение суставов приводит к заболеваниям всей опорно – двигательной системы, и, как следствие, к инвалидности. Гемоартроз развивается наиболее быстро у больных с тяжелыми формами гемофилии, иными словами, чем тяжелее протекает гемофилия – тем быстрее у человека развивается гемоартроз. Первые признаки гемоартрозов развиваются к 8 – 10 годам. При тяжелой форме гемофилии кровоизлияния в суставы происходят самопроизвольно, а при легком течении – вследствие травм.
Кровотечение в суставы – это наиболее специфический для гемофилии симптом. Кровоизлияния в суставы являются причиной формирования у больных гемофилией заболеваний суставов – гемоартрозов. Данное поражение суставов приводит к заболеваниям всей опорно – двигательной системы, и, как следствие, к инвалидности. Гемоартроз развивается наиболее быстро у больных с тяжелыми формами гемофилии, иными словами, чем тяжелее протекает гемофилия – тем быстрее у человека развивается гемоартроз. Первые признаки гемоартрозов развиваются к 8 – 10 годам. При тяжелой форме гемофилии кровоизлияния в суставы происходят самопроизвольно, а при легком течении – вследствие травм.
Кровь в моче, заболевания почек при гемофилии
Гематурия (кровь в моче) может протекать бессимптомно или сопровождаться острой болью, приступом почечной колики, которая возникает при прохождении сгустков крови по мочевыводящим путям. У больных гемофилией могут развиваться такие заболевания почек как пиелонефрит, гидронефроз и капиллярный склероз.
Какие лекарства нельзя принимать больным гемофилией?
Больным гемофилией категорически противопоказаны препараты, снижающие свертываемость крови, такие как ацетилсалициловая кислота (аспирин), бутадион и т.д.
Признаки гемофилии у новорожденных
 Если у новорожденного ребенка долго не останавливается кровотечение из пуповины и имеются гематомы на голове, ягодицах и промежности, необходимо сдать анализы на наличие гемофилии. К сожалению, предсказать рождение ребенка с гемофилией на сегодняшний день невозможно. Существуют методы пренатальной (дородовой) диагностики, но они не являются широко распространенными ввиду их сложности. Если в семье у мальчика имеется гемофилия, то его сестры являются носителями гена гемофилии и у них могут родиться дети, больные гемофилией. Поэтому семейный анамнез имеет огромное значение в прогнозе рождения детей, которые могут страдать данным заболеванием.
Если у новорожденного ребенка долго не останавливается кровотечение из пуповины и имеются гематомы на голове, ягодицах и промежности, необходимо сдать анализы на наличие гемофилии. К сожалению, предсказать рождение ребенка с гемофилией на сегодняшний день невозможно. Существуют методы пренатальной (дородовой) диагностики, но они не являются широко распространенными ввиду их сложности. Если в семье у мальчика имеется гемофилия, то его сестры являются носителями гена гемофилии и у них могут родиться дети, больные гемофилией. Поэтому семейный анамнез имеет огромное значение в прогнозе рождения детей, которые могут страдать данным заболеванием.
Диагностика гемофилии
 Для диагностики гемофилии используют такие лабораторные методы:
Для диагностики гемофилии используют такие лабораторные методы:
- определение количества факторов свертывания в крови
- определение времени свертывания крови
- количество фибриногена в крови
- тромбиновое время (ТВ)
- протромбиновый индекс (ПТИ)
- международное нормализованное отношение (МНО)
- активированное частичное тромбопластиновое время (АЧТВ)
- микст – АЧТВ
При наличии гемофилии отмечается увеличение свыше нормальных значений следующих показателей: времени свертывания крови, активированного частичного тромбопластинового времени (АЧТВ), тромбинового времени (ТВ), международного нормализованного отношения (МНО). Также наблюдается уменьшение ниже нормальных значений протромбинового индекса (ПТИ), но нормальные значения микст – АЧТВ и количества фибриногена. Основным показателем, характеризующим гемофилию А и В является уменьшение концентрации или активности факторов свертывания в крови, VIII– при гемофилии А и IX – при гемофилии В.
Лечение гемофилии
Данное заболевание является неизлечимым, его можно только контролировать и проводить поддерживающую терапию. Для этого людям, страдающим гемофилией, вводят растворы фактора свертывания, которого у них в крови не достаточно. В настоящее время данные факторы свертывания получают из крови доноров, или крови специально выращиваемых животных. При правильном лечении продолжительность жизни больных гемофилией не отличается от продолжительности жизни людей, не страдающих данной патологией. Однако в связи с тем, что препараты для лечения гемофилии изготавливают из крови доноров, то больные гемофилией находятся в группе риска по таким опасным заболеваниям как СПИД и гепатит.
Автор: Наседкина А.К.
Источник: www.polismed.com
Этиология
Этиология не известна. Заболевание обусловлено, по-видимому, мутацией расположенного на Х-хромосоме гена, ответственного за биосинтез антигемофильного фактора.
Частоту мутации генов, ответственной за развитие Г., суммарно определяют в 2—3,2 мутантных гена на 100 000 гамет [Стерн (С. Stern), 1965], или 1,3—4,2×10-5 для гемофилии А и 0,6—4,6×10-6 для гемофилии B.
Генетика
Заболевание наследуется по сцепленному с полом рецессивному типу (см. Наследование). Гены, регулирующие синтез факторов VIII и IX, локализуются в Х-хромосомах репродуктивных клеток.
Предполагают, что формам гемофилии (А и В) соответствуют по крайней мере два различных локуса, расположенных на различных концах X-хромосом; Однако имеются данные о возможном участии в регуляции синтеза фактора VIII и аутосомных локусов. Согласно современным представлениям, Г. не только «дефицитное состояние». По аналогии с гемоглобинопатиями полагают, что причинами Г. могут быть количественные и качественные изменения факторов свертывания крови. О такой возможности свидетельствует выявление у больных мутантных фенотипов факторов VIII и IX. Генетику Г. изучали на собаках [Бринкхаус (К. Brinkhous) и др.], у которых это заболевание идентично болезни человека. В соответствии с гипотезой Лайон (М. F.Lyon, 1962) женщина с одной пораженной Х-хромосомой (гетерозигота) является только кондуктором (носителем) патол. гена, но сама не заболевает, т. к. вторая непораженная Х-хромосома обеспечивает достаточный синтез соответствующего фактора (VIII или IX) свертывания крови (чаще у кондукторов гемофилии В). У женщин-носителей патол, гена обнаруживают иногда незначительную кровоточивость и уменьшение содержания фактора VIII или IX. У женщин Г. возникает только при наличии двух пораженных X-хромосом: от больного Г. отца и от матери-носителя патол, гена. Описано 24 достоверных случая Г. у женщин [Уинтроб (М. Wintrobe), 1967]. Следовательно, гипотеза Бауэра (К. Н. Bauer, 1922) об отсутствии потомства от больного Г. мужчины и женщины-носителя патол, гена вследствие формирования так наз. летального гена не получила подтверждения.
С помощью клинико-генетических исследований различают наследственную, семейную и спонтанную (спорадическую) форму Г.; последняя является следствием вновь возникших мутаций и составляет ок. 28% для гемофилии А и 9% для гемофилии В. При гемофилии обнаруживают также сопряженное нарушение функции близлежащих в X-хромосоме генов: глюкозо-6-фосфатдегидрогеназы, цветовой слепоты и др.
Патогенез
Патогенез связан с нарушениями в первой фазе свертывания крови вследствие недостатка продукции факторов VIII или IX, которые участвуют в образовании тромбопластина. При Г. нарушен внутренний механизм образования тромбопластина, что проявляется удлинением времени свертывания крови.
Фактор VIII является гликопротеидом, содержится в плазме, концентрация его ,у здоровых людей составляет 10 мг/л. Структура фактора окончательно не установлена. Фактор VIII быстро разрушается при консервировании крови и нагревании. В процессе свертывания фактор VIII потребляется и поэтому в сыворотке не содержится. При фракционировании плазмы по методу Кона фактор VIII выделяется с I фракцией. Предполагаемое место синтеза — печень, селезенка, лейкоциты. Период полураспада 6—8 час.
Фактор IX — белок плазмы и сыворотки — относится к группе бета2-глобулинов, мол. вес ок. 80 000, стабилен при консервировании крови и нагревании. Из плазмы адсорбируется с помощью BaSO4, Al(OH)3 и др. В процессе свертывания не потребляется и потому содержится в сыворотке. При фракционировании плазмы по методу Кона выделяется с фракциями III и IV. Период полураспада — 24 часа.
Патологическая анатомия
Изменения во внутренних органах, костно-суставной системе и т. д. являются следствием массивных кровотечений и кровоизлияний (ишемия органов, изменения в костях, суставах, мышцах в результате образования осумкованных, оссифицированных гематом, кист и др.).
В межмышечных гематомах быстро (включается внешний механизм свертывания) образуются сгустки. Такие гематомы плохо рассасываются и в дальнейшем подвергаются организации, а при повторных кровоизлияниях образуются псевдоопухоли, достигающие больших размеров. Повторные кровоизлияния в суставы являются причиной нарушения их функции.
Клиническая картина
Клиническая картина гемофилии А и гемофилии В характеризуется кровоточивостью. Кровотечения возникают периодически, как правило, через 1—2 часа после травмы, причем травма может быть ничтожной, а кровотечение обильным. У некоторых больных выявляют цикличность таких кровотечений, нередко зависимых и от времени года. Кровотечения могут иметь различную локализацию, чаще кровь изливается в мягкие ткани и суставы. Наружные кровотечения возникают после перерезки пуповины, при прорезывании или экстракции зубов, после травм и оперативных вмешательств. Внутренние кровотечения могут быть забрюшинные, в органы грудной и брюшной полости, ц. н. с.
Симптомы Г. могут проявляться в момент рождения (кефалогематомы, кровотечения из пупочной ранки). С возрастом локализация кровотечения меняется. Если на первом году жизни у детей более часты кровотечения из слизистых оболочек носа и ротовой полости (вследствие прикуса языка, ранения щек, прорезывания молочных зубов), кровоизлияния под кожу и подкожную клетчатку, то у 2—3-летних детей обнаруживаются кровоизлияния в суставы и мягкие ткани. У детей 7—9 лет наряду с гемартрозами (см.) нередко наблюдаются кровотечения из десен при смене зубов; гематурия (см.) и кровоизлияния во внутренние органы. Периоды ремиссии у больных Г. детей короче, чем у взрослых.
Тяжесть клин. течения не зависит от формы Г. (А или В), а определяется уровнем дефицитного фактора. Г. протекает с периодами относительного благополучия, неодинаковыми у нескольких членов одной семьи.
Различают три формы клин, течения Г.: тяжелую, среднюю и легкую. Многие авторы выделяют четвертую форму — скрытую.
Для тяжелой формы Г. характерно раннее проявление кровоточивости и осложнений (остеоартрозы, контрактуры и т. д.). Уровень дефицитного фактора у этих больных составляет до 3% от нормы. Для средней и легкой формы Г. характерно более позднее появление кровоточивости. Содержание дефицитного фактора до 4—6% от нормы. Скрытую форму Г. (уровень фактора VIII 6—10%) обычно выявляют случайно или при проведении семейных исследований у больных, у которых обнаруживают избыточную кровоточивость после травм, при экстракции зубов, тонзиллэктомии и других хирургических вмешательствах.
Для тяжелой формы Г. характерны кровоизлияния в суставы, причем обычно суставы поражаются в 2—3-летнем возрасте. Гемартроз сопровождается болевыми ощущениями, припуханием, защитной контрактурой мышц, местным и общим повышением температуры. Продолжающееся кровотечение вызывает перерастяжение тканей с последующим некрозом их и вскрытием гематомы. Нередки кровоизлияния в поясничные мышцы, в полость брюшины. Кишечные кровоизлияния протекают с развитием симптомов острого живота. Почечные кровотечения могут проявляться почечной коликой. При упорных кровотечениях из жел.-киш. тракта нередко развивается тяжелая анемия. У больных Г. возникают обильные кровотечения после удаления зубов (описаны случай смертельных кровотечений). Чрезвычайно опасны для жизни больного кровоизлияния в головной мозг, мозжечок, мозговые оболочки, спинной мозг.
Осложнения
При Г. лёгкой и средней тяжести осложнения возникают редко. Повторные кровоизлияния в сустав вызывают утолщение капсулы, узурирование хряща и остеопороз. При кровоизлияниях в коленный сустав, который поражается чаще, кровь скапливается в верхнем завороте, вызывая резкие боли и вторичную рефлекторную атрофию четырехглавой мышцы. При отсутствии лечения развивается стойкая контрактура. Характерно образование кровяных кист в метафизе, реже в диафизе трубчатых костей. Иногда кисты локализуются в тазовых, пяточных костях. Наличие деструктивных процессов в костях нередко приводит к патол, переломам (рис. 1). При обширных подкожных, внутримышечных, забрюшинных кровотечениях может наступить сдавление сосудов и нервов с последующим развитием некрозов, параличей и ишемической контрактуры.
Локализация значительные по размеру псевдоопухолей и геморрагических кист в брюшной полости может симулировать картину кишечной непроходимости. Забрюшинная локализация их может Вести к сдавлению мочеточников. При локализации гематом по ходу магистральных сосудов и нервных стволов возможно сдавление их, что ведет к развитию параличей, ишемии органов, гангрены конечностей и др. Гематурия при Г. нередко ведет к образованию сгустков в мочевыводящих путях (особенно на фоне антифибринолитической терапии) с окклюзией мочевыводящих путей и нарушением функций почек.
Диагноз
Диагноз основывается на данных анамнеза, клин. картины и лабораторных исследований. Важное значение имеет тщательный сбор анамнеза (кровоточивость у мужчин в семье по линии матери, кровотечения с преимущественным поражением суставов, связанные с предшествующей травмой, их длительность и рецидивы). При осмотре больных обращают внимание на наличие кровоизлияний, гематом, изменения в суставах. При коагулологическом исследовании крови (см. Коагулограмма) наличие у больного Г. можно заподозрить на основании удлинения времени свертывания крови (см.) и времени рекальцификации плазмы, снижения потребления протромбина, что указывает на нарушение тромбопластинообразования. Характерны изменения тромбоэластограммы (см. Тромбоэластография). Но окончательный диагноз Г. ставят по результатам исследования парциального тромбопластинозого времени и теста генерации тромбопластина по Биггс—Дугласу. При гемофилии А этот тест корригируется добавлением плазмы, адсорбированной BaSO4 или Al(OH)3; при гемофилии В — добавлением сыворотки. Однако и он является недостаточно чувствительным. Наиболее точная диагностика основывается на количественном определении факторов VIII и IX.
Дифференциальный диагноз
Некоторые симптомы, характерные для Г., наблюдаются и при других заболеваниях. При ангиогемофилии (см.) кровоточивость встречается у лиц обоего пола, чаще у женщин; выявляется чрезмерное удлинение времени кровотечения (см.); кроме дефицита фактора VIII, в крови уменьшено содержание сосудистого фактора. При болезни Стюарта — Прауэр (см. Геморрагические диатезы) кровоточивость (преимущественно у женщин молодого возраста) обусловлена дефицитом фактора X. Одновременно с нарушением первой фазы свертывания крови выявляют нарушение парциального тромбопластинового времени и уменьшение протромбинового индекса (см. Протромбиновое время).
При коллагенозах, туберкулезе, злокачественных новообразованиях, воздействии ионизирующей радиации, медикаментозных и других интоксикациях в крови появляются циркулирующие антикоагулянты, чаще к фактору VIII, имитирующие клинику Г. При дифференциации; их с Г. большое значение имеют данные анамнеза: отсутствие , указаний на кровоточивость у других членов семьи, появление первых признаков кровоточивости в зрелом возрасте на фоне возникшего заболевания.
Важными для дифференциального диагноза тестами являются так наз. перекрестные пробы: добавление к исследуемой крови или плазме 0,1 объема крови или плазмы здорового человека нормализует время свертывания крови у больных Г.; при наличии в крови любого антикоагулянта проба отрицательна. Наоборот, добавление 0,1 объема крови с антикоагулянтом к нормальной крови увеличивает время ее свертывания. Дополнительными исследованиями являются проба Биггс—Бидуэлл, антитела к фактору VIII, определение содержания свободного гепарина и титрование с протамин-сульфатом.
Рентгенодиагностика изменений костей и суставов характеризуется признаками поражения опорно двигательного аппарата вследствие кровоизлияний в полости суставов, в костномозговые пространства и в мягкие ткани.
Однократные кровоизлияния в суставы могут быстро и бесследно рассасываться. В острый период гемартроза рентгенол. картина не специфична. На рентгенограммах иногда обнаруживается небольшое расширение суставной щели, обусловленное скоплением крови.
Повторные кровоизлияния в суставы приводят к гемофилическому остеоартрозу. Рентгенологическим признаком повторных кровоизлияний, начавшихся в детском возрасте, является изменение размеров и формы сустава.
Рентгенологически различают четыре стадии гемофилического остеоартроза. На рентгенограммах в I стадии обнаруживают остеопороз суставных концов и утолщение суставной капсулы. II стадия характеризуется уменьшением объема движений в суставе за счет утолщения капсулы и образования внутри сустава организующихся гематом. В III стадии выявляют сужение суставной щели и изменение конфигурации суставных концов костей вследствие разрушения подхрящевых отделов эпифизов, костных разрастаний (рис. 2), кистовидной перестройки эпифизов. В IV стадии суставная щель на рентгенограммах не видна или резко сужена. Подхрящевые отделы эпифизов значительно склерозированы.
Имеются некоторые особенности в рентгенол, картине различных суставов с гемофилическим остеоартрозом: в коленном суставе часто разрушаются межмыщелковая ямка бедра, боковые поверхности мыщелков и надколенник; в локтевом — полулунная выемка локтевой кости; в плечевом — вдоль анатомической шейки образуются краевые узуры, иногда напоминающие сухую костоеду; в тазо-бедренном — развивается остеохондропатия.
При внутрикостных кровоизлияниях крупные кистозные полости обнаруживаются чаще в эпифизах, но встречаются и в диафизах. Организующаяся гематома рентгенологически может дать картину так наз. гемофилической псевдоопухоли кости (рис. 3). При формировании геморрагических кист в прилежащих отделах скелета обнаруживаются атрофические процессы с почти полным рассасыванием обширных участков кости. По краям кист выявляются экзостозные костные образования, свидетельствующие о репаративных процессах в костной ткани. В области дефекта кости можно видеть костные и известковые включения, которые при дефекте, расположенном в краевом отделе кости, могут дать картину «козырька» (рис. 4), как при остеогенной саркоме. При Г. могут наблюдаться также внутрикостные очаги склероза, субпериостальные оссифицированные гематомы, параоссальные оссификаты.
Почти у половины больных выявляют оссифицирующие гематомы в мягких тканях. Г. может быть причиной прогрессирующего оссифицирующего миозита.
Правильная интерпретация клинико-рентгенол. симптоматики поражений опорно-двигательного аппарата при Г. позволяет провести дифференциальную диагностику с артрозами и изменениями костей другой этиологии и определить показания к различным видам лечения (хирургическое, ортопедическое, лучевое).
Лечение
Основным методом лечения больных Г. является возмещение недостающего фактора свертывания крови. Лечение осложнений, вызванных кровотечениями и кровоизлияниями (гематомы, гемартрозы, контрактуры и т. д.), иногда связано с хирургическими вмешательствами. Хирургические вмешательства как по поводу осложнений Г., так и в связи с заболеваниями, требующими хирургического лечения (аппендицит, непроходимость кишечника, язва желудка, травмы и т. д.), имеют свои особенности.
Лечение Г. важно начать с первых проявлений кровоточивости. Позднее начало лечения, как правило, приводит к тяжелым осложнениям и, кроме того, удлиняет курс лечения.
Больным назначают цельную кровь, плазму (нативную замороженную, лиофилизированную) и антигемофильные препараты (концентраты факторов VIII и IX), а также ингибиторы фибринолиза. Свежую кровь или плазму необходимо вводить в больших объемах (до доведения концентрации антигемофильного фактора в крови до требуемого уровня); это ограничивает их применение, т. к. наибольший объем переливаемой крови и плазмы за 24 часа не должен быть более 25 мл на 1 кг веса тела, и повторные инфузии больших объемов могут привести к перегрузке в системе циркуляции, образованию антител к фактору VIII (или IX), анафилактической и температурной реакции, гематурии, нарушению функции почек и т. д.
В антигемофильных препаратах концентрацию фактора VIII (или IX) выражают единицами активности. За 1 ед. активности фактора VIII (или IX) принято его количество, содержащееся в 1 мл нормальной плазмы, полученной при смешивании плазмы от многих доноров.
Расчет дозы антигемофильного препарата производят в единицах активности фактора VIII (или IX). При введении больному 1 ед. антигемофильного препарата на 1 кг веса тела уровень фактора VIII повышается на 1—2%. Дозу препарата рассчитывают по исходному уровню дефицитного фактора в крови больного, а также по периоду его полураспада. Период полураспада фактора VIII после однократного введения больному антигемофильного глобулина составляет 6—8 час., после остановки кровотечения период полураспада удлиняется до 13—26 час. [Бринкхаус (К. Brinkhous), 1970; Ю. И. Андреев с соавт., 1972]. Период полураспада фактора IX колеблется от 12 до 24 час. [Биггс (R. Biggs), 1970; Султан (Y. Sultan), 1970]. Концентрированные препараты вводят внутривенно, струйно, с помощью шприца или системы для переливания крови.
Методы приготовления антигемофильных препаратов
При хранении консервированной крови и плазмы при плюсовой температуре фактор VIII инактивируется в течение нескольких часов. Поэтому свежую плазму, быстро отделенную от эритроцитов, замораживают при t° —25—40°., Эту плазму готовят следующим образом. Кровь от донора набирают в пластмассовый мешок (один из двух спаренные) с консервантом. Оба мешка (с пережатой соединительной трубкой между ними) центрифугируют 20 мин. Затем слой плазмы перемещают во второй мешок путем легкой внешней компрессии, герметизируют соединительную трубку, к-рую затем перерезают. Оставшиеся в первом мешке форменные элементы крови используют для переливания. Полученная плазма используется для переливания или является исходным сырьем для приготовления антигемофильных препаратов: криопреципитата и концентрата фактора VIII.
Антигемофильная плазма содержит в 1 мл 0,2—1,6 ед. фактора VIII. Хранят ее при t°—30°. Гемостатическая доза — 10 мл на 1 кг веса тела. Суточная доза 20 мл на 1 кг веса тела.
Криопреципитат впервые получен Пул (I. Pool, 1965), широко используется во всем мире. Представляет собой белковый препарат изогенной плазмы человека, в малом объеме содержит от 5 до 15 ед/мм фактора VIII. Хранится при 1° —30° или в высушенном виде, растворим при t° 35—37°. Применяется с учетом совместимости по AB0-группам крови.
Известны также высокоочищенные лиофилизированные концентраты фактора VIII с активностью до 30—50 ед/мл.
Фактор IX адсорбируют на трикальцийфосфате, гидроокиси алюминия, сернокислом барии и других адсорбентах, на чем основаны методы выделения его. Выбор адсорбента и другие методические особенности приготовлений указанных концентратов зависят от вида консерванта, стабилизирующего плазму. Одновременно с фактором IX адсорбируются факторы II, VII и X, вместе составляющие так наз. комплекс PPSB (по первым буквам названий факторов Р-протромбин (II), Р-проконвертин (VII), S— фактор Стюарта, В — антигемофильный фактор IX. Фактор IX устойчив при хранении плазмы при плюсовой температуре и выделение его не требует таких предосторожностей, как при работе с фактором VIII.
Протромбиновый комплекс PPSВ впервые получен Ж. Сулье, в СССР— Л. В. Минаковой. Пюи получении комплекса PPSB важно правильно выбрать стабилизатор, предотвращающий свертывание крови. Первоначальное предложение об использований с этой целью ионообменных смол не получило применения в промышленных масштабах выделения комплекса PPSB.
Использование в качестве стабилизатора лимонной к-ты и ее солей резко снижает возможность адсорбции комплекса PPSB из плазмы крови, поскольку цитраты растворяют. PPSB с поверхности адсорбентов (напр., гидроокиси алюминия). Кроме того, при большом содержании в подученных препаратах цитрата натрия у больных возникают боли.
Распространенным стабилизатором крови при получений комплекса PPSB является этилендиаминтетрауксуснокислый натрий (ЭДТА-Na), который имеет, однако, сравнительно высокую токсичность, ограничивающую непосредственное применение PPSB.
Метод выделения PPSB заключается в следующем: к плазме добавляют гель трикальцийфосфата (ок. 5 вес. %) и после перемешивания центрифугируют. Осадок трикальцийфосфата с адсорбированным на нем PPSB дважды обрабатывают 2—3% р-ром цитрата натрия; отделяя осадок центрифугированием. Центрифугат объединяют и высушивают в замороженном состоянии (лиофилизация). Т. о., достигают примерно 20-кратной концентрации фактора IX. Превращение протромбина в тромбин предотвращают добавлением гепарина и кофактора гепарина.
Возможно выделение PPSB из цитратной плазмы путем адсорбции его на диэтиламиноэтилцеллюлозе с последующим растворением цитратно-фосфатным буфером. Промышленного применения метод пока не имеет.
При промышленном получении препарат PPSB выделяют из фракции III Кона. Главная трудность состоит в сложности отделения PPSB от липопротеинов, составляющих основную массу фракции III.
Комплекс PPSB содержит в 1 мл 10—60 ед. фактора IX. Вводят его после проверки на наличие тромбина. Срок хранения до 1 года. Хранят в лиофилизированном виде при t° 4°.
Ингибиторы фибринолиза вводятся с целью угнетения фибринолитических процессов. 5% р-р эпсилон-аминокапроновой к-ты вводят внутривенно в дозе до 400 мл в сутки или 4—8 г сухого порошка внутрь. Противопоказанием для назначения ингибиторов фибринолиза являются почечные кровотечения.
При обширных кровоизлияниях в мягкие ткани, полости, органы, в ц. н. с. из гемостатических средств предпочтительнее введение концентратов фактора VIII (IX). Вводят гемостатические средства до полной остановки кровотечения.
Лечение осложнений гемофилии
Важна правильная тактика ведения больных Г. с гемартрозами. При острых гемартрозах необходимо прежде всего снять болевой синдром назначением аналгезирующих средств; однако длительное применение ацетилсалициловой к-ты, бутадиона может усилить кровоточивость, а широкое назначение наркотиков — привести к развитию у больных Г. наркомании.
Лечение гемартрозов необходимо начинать в первые часы или сутки от начала кровоизлияния, т. к. только при этом условии можно рассчитывать на восстановление функции сустава. На фоне трансфузии антигемофильных препаратов аспирируют из полости сустава кровь с последующим введением гидрокортизона и иммобилизацией сустава на 1—2 дня.
При хрон. гемофилических остеоартрозах в фазе организации гематом в ряде случаев показана местная рентгенотерапия (рис. З и 4). Кроме того, она способствует уплотнению сосудистой стенки.
При развитии стойких контрактур с целью их коррекции показаны: липкопластырное вытяжение, этапные гипсовые повязки. При сопутствующем синовите рекомендуется вводить гидрокортизон.
При отсутствии эффекта от консервативного лечения (запущенные формы синовита) производится синовэктомия. Операция иссечения синовиальной оболочки сустава способствует восстановлению функции сустава, прекращению повторных кровоизлияний. Операция резекции суставов и корригирующая остеотомия производятся при дегенеративных формах поражения.
Пунктирование глубоких межмышечных гематом эффекта не даёт вследствие быстрого свертывания в них крови; длительно сохраняющаяся гематома является показанием для оперативного опорожнения ее на фоне введения антигемофильных препаратов.
Обширные гемофилические псевдоопухоли, располагающиеся внутрибрюшинно или вблизи жизненно важных органов, удаляют с полным иссечением их капсулы; подлежат удалению и малые гематомы при появлении признаков их нагноения.
Для полной остановки наружного кровотечения вводят 20 ед. антигемофильного препарата на 1 кг веса тела, чтобы повысить уровень фактора VIII до 40% от нормы.
При жел.-киш. кровотечениях леч. мероприятия должны быть направлены на остановку кровотечения и на ликвидацию анемии. Некупирующиеся при активной гемостатической терапии жел.-киш. кровотечения являются показанием для лапаротомии с последующей перевязкой кровоточащего сосуда или, если это невозможно, резекцией органа.
Особенности ведения больных гемофилией при хирургических вмешательствах
Всякое хирургическое вмешательство у больных Г. связано с опасностью тяжелого кровотечения, особенно в послеоперационном периоде.
При подготовке больных Г. к хирургическим вмешательствам уровень фактора VIII (или IX) должен быть доведен до 50% от нормы и более.
При необходимости, в зависимости от характера предстоящих хирургических вмешательств, содержание дефицитного фактора повышают до 100% и поддерживают этот уровень в течение 3—5 дней. Перед операцией вводят 30—60 ед. антигемофильного препарата на 1 кг веса тела.
В послеоперационном периоде после больших операций более рационально одномоментно вводить всю суточную дозу препарата либо по 20 ед. на 1 кг веса через 8 час.
В течение 10 дней после операции уровень дефицитного фактора необходимо повышать до 30—40% нормы, а затем, в зависимости от состояния, можно переводить больного на профилактические дозы препарата до полного выздоровления. Длительность гемостатической терапии при больших операциях, в т. ч. и костнопластических, составляет 7—14 дней. Одновременно применяют антифибринолитические средства (5% р-р эпсилон-аминокапроновой к-ты 300—500 мл или 40% р-р ацепрамина 60—80 мл в сутки); кортикостероидные гормоны (преднизолон внутривенно 20—30 мг, гидрокортизон 50—100 мг в сутки); сосудоукрепляющие средства (препараты кальция, аскорбиновая к-та, рутин и т. д.).
При экстракции зубов за 30 мин. до операции вводят 30—40 ед. на 1 кг веса тела антигемофильного препарата (чтобы повысить уровень дефицитного фактора до 30—40%); повторно препарат вводят через 12— 24 часа в дозе 10—15 ед. (для поддержания дефицитного фактора не ниже 15—25%). Длительность антигемофильной терапии зависит от характера заживления раны.
Прогноз
Прогноз в отношении выздоровления неблагоприятный, однако система диспансеризации и профилактическое введение антигемофильных препаратов значительно улучшают течение заболевания. Заместительная терапия в момент кровотечений позволяет во многих случаях предупредить развитие осложнений, в т. ч. тяжелых гемартрозов, и сохранить трудоспособность больных.
Источник: xn--90aw5c.xn--c1avg
Механизм развития и причины
В основе названного расстройства лежит передача генетической информации. Нарушение переходит от родителей детям. Это единственный возможный путь, хотя, как уже было сказано, бывают и спонтанные мутации, вызывающие отклонение у потомства и у вполне здоровых матери и отца.
Тип наследования гемофилии рецессивный, сцеплен с передачей материала X-хромосомы. Почему болеют в основном мужчины? Это становится понятно, если разобраться в пути передачи информации.
Поскольку нарушение, условно говоря, заложено в X, женщина практически не способна оказаться больной гемофилией. Поскольку в основе ее генетического материала находятся две хромосомы X.
При дефективности одной, компенсирующую роль берет на себя другая. Но при этом измененный материал никуда не девается. Он также остается в фундаменте организма матери.
Такие женщины, которые носят аномальный ген, но сами не болеют, называются кондукторами.
При формировании нового организма, возможны следующие варианты:
Отец и мать здоровы. Отсутствуют аномальные гены. В таком случае патология не развивается.
- Женщина является носительницей измененной X-хромосомы. Отец здоров. У дочери генотип представлен комбинацией XX. С вероятностью примерно в 50% она станет кондуктором. Поскольку у мальчиков сочетание будет XY, с тем же риском он заболеет гемофилией. У мужчин нет второго гена, который способен скомпенсировать измененный.

- Отец болен, мать здорова. В таком случае расклад идентичен, только вероятность развития патологического процесса у детей куда меньше.

- Мать кондуктор, отец страдает гемофилией. Это самая неблагоприятная ситуация. При негативном сценарии могут заболеть даже девочки. Если женщина передает потомству дефектную X-хромосому и то же самое сделает отец, компенсации в XX комбинации уже не будет.
Не говоря о вероятности становления проблемы у ребенка мужского пола. Такой вариант, однако, встречается редко.

На долю наследственных причин приходится основная масса клинических случаев. Около 70% и даже более по некоторым оценкам.
Но это далеко не единственная причина гемофилии у детей, в оставшейся части ситуаций имеет место спорадическая, спонтанная мутация, которая и становится основным фактором развития болезни.
Проблема в том, что меняется не только фенотип, то есть устойчивые качества одного конкретного организма без передачи потомству, но и генотип.
В результате такого отклонения, отмечается дефект в хромосомах, появляются риски наследования нарушения потомством.
Обследоваться нужно еще на этапе планирования беременности. Это позволит избежать ненужных проблем в будущем.
Классификация
Подразделение патологического процесса проводится по критерию недостаточной выработки фактора свертывания. Многое зависит от конкретной формы болезни. Всего по этому основанию выделают три ключевых вида.
- Типичная. Или классическая. Она же гемофилия А. Возникает примерно в 80% ситуаций. Обнаруживается у пациентов особенно часто. Симптоматика соответствует описываемой в литературе, когда говорят об общем правиле. Характеризуется скудным синтезом VIII фактора свертывания. Лечится с большим трудом, имеется возможность только устранить симптоматику и то на время и не полностью.
- Гемофилия Б. Вырабатывается мало фактора свертывания IX, что сказывается на скорости гемостаза. Также возможен вариант, когда это вещество не синтезируется вовсе. Принципиальных отличий с точки зрения пациента нет, поскольку клиника будет примерно той же, с некоторыми отличиями и значительными расхождениями с точки зрения объективных показателей. На долю этого типа приходится порядка 17% ситуаций.
- Гемофилия С. Редкая разновидность. Наблюдается всего у 2% пациентов. Плюс-минус. Отличительных черт не имеет, не считая лабораторных специализированных показателей.

Есть и другие типы нарушения, которые можно выделить по тому же критерию. Но они встречаются исключительно редко. Примерно в половине процента случаев. Потому имеют куда меньшую эпидемиологическую значимость.
Гемофилия у детей и взрослых классифицируется и по степени тяжести. Исходя из клиники, интенсивности необходимого провокатора, выделяют три основных разновидности расстройства.
- Легкая степень. Фактор вырабатывается в больших количествах, но его все же недостаточно. До определенного возраста пациент и его родители могут и не предполагать о наличии проблемы. Все вскрывается случайно. При получении тяжелой травмы, проведении операции и т.д. Интенсивность провокатора должна быть высокой.
С такой формой патологического процесса человек вполне качественно и долго живет, имеет положительные прогнозы. Не всегда вообще требуется лечение.
- Средняя степень. Фактора синтезируется значительно меньше положенной нормы. Что заметно сказывается на состоянии человека. Если при легком течении изменение обнаруживается порой в подростковые годы, тут все понятно с начальных дней жизни пациента.
Достаточно незначительного физического воздействия, чтобы спровоцировать кровоточивость. Такая форма нарушения трудно поддается коррекции. Однако прогнозы все же неплохие. При достаточной внимательности к собственному здоровью есть шансы на выживание.
- Тяжелая степень. Встречается часто. В том случае вообще нет необходимости во влиянии на тело извне. Нарушения настолько выраженные, что пациент становится жертвой кровотечений спонтанно, без видимых факторов. С точки зрения сохранения жизни, шансы невелики.
Обе классификации применяются для понимания сути болезни, разработки тактики терапии, выбора оптимальной схемы.
Симптомы
Клиническая картина обычно тяжелая. Неспецифичная, поскольку существуют и другие формы коагулопатий, которые не сопряжены с недостаточным синтезом факторов свертывания. Нужно разбираться в ситуации предметно.
Что касается конкретных проявлений проблемы:
- Гематомы на теле. Образование синяков без видимых причин или после незначительного по интенсивности воздействия на структуры организма. Типична большая площадь поражения, поскольку кровь не останавливается довольно длительное время.
Расстройство характерно и для тромбоцитопатий, потому выяснять природу нужно посредством диагностических мероприятий. Возможно спонтанное формирование гематом.
Локализация подкожных кровоизлияний в основном — руки, ноги, живот, область лица, паха. Те места, которые подвергаются наибольшему механическому воздействию.

Суть явления такова, что достаточно трения одеждой, давления и прочих незначительных с точки зрения здорового человека причин.

- Кровотечения. Типичнейшая клиническая черта рассматриваемого патологического процесса. Интенсивность таковых зависит от степени тяжести расстройства. Локализация может быть любой. Наиболее часто имеет место излияние в полости суставов (гемартрозы), желудочно-кишечный тракт, центральную нервную систему.

Также возможен выход крови с мочой при поражении почечных сосудов. Не считая уже названных гематом, когда жидкая ткань скапливается в области подкожно-жировой клетчатки.
Характерно, что процесс начинается не сразу по окончании влияния негативного фактора. Например, после травмы. А спустя 6-8 и даже более часов. Когда пациент успокаивается и считает, что все нормально.
- Геморрагический диатез. Провоцируется инфекционно-воспалительными заболеваниями. В данном случае имеет место интенсивная реакция иммунитета на возбудителей извне и высвобождение ими конечных продуктов жизнедеятельности, токсинов.
Названный симптом определяется развитием на теле массивных очагов кровоизлияний в виде красной сыпи, пятен или небольших выпуклых петехий. Размеры таковых редко достигают более 2-3 мм в диаметре.

Возможны варианты. Область покрытия большая. Как правило, страдают руки, нижние конечности, лицо, грудь, пах.
Связи с механическим фактором нет. Сыпь возникает спонтанно. Возрастных особенностей также не наблюдается. Симптоматика присутствует в равной мере у взрослых и детей.
- Осложнения со стороны опорно-двигательного аппарата. При длительном существовании болезни велика вероятность развития таких расстройств, как артроз и прочие нарушения. Подобное — результат хронического течения заболевания. Собственно симптоматикой гемофилии такое назвать нельзя. Это уже осложнения.
- Астенический синдром. Пациент постоянно теряет кровь в разных объемах. Проявление присутствует у больных с нарушением средней степени тяжести и далее.
Поскольку объем жидкой соединительной ткани становится недостаточным для обеспечения головного мозга и центральной нервной системы вообще кислородом и полезными соединениями.
Как следствие — постоянная слабость, сонливость, повышенная усталость и утомляемость, невозможность работать и даже обслуживать себя в быту.
- Последствия со стороны органов. Поражение пищеварительного тракта, расстройства в работе легких, сердечно-сосудистой системы. Гемофилия у женщин может проявляться в виде маточных кровотечений. Особенно опасен период беременности, естественный менструальный цикл.
Клиника не исчерпывается названными отклонениями. Описаны лишь основные группы и типы признаков. На деле все зависит от клинической ситуации, ее тяжести и формы заболевания.
Диагностика
Обследование проводится с первых дней жизни пациента. Кроме того, имеет смысл еще на этапе планирования беременности обратиться к специалисту по генетике.
В ходе первичной оценки состояния родителей, проводится опрос, выявляются анамнестические данные. После чего назначается серия специфических тестов, чтобы обнаружить возможного носителя дефектного гена.
По окончании уже есть смысл делать выводы относительно целесообразности зачатия с данными конкретными партнерами и рисков развития патологического процесса у ребенка в будущем, после появления на свет.
Что касается проведения обследования у самого пациента. В основном применяются лабораторные методики.
Какие именно:
- Устный опрос. Нужно выявить все жалобы на здоровье. Как правило, у больных они уже есть. Классифицировать, систематизировать симптомы и выдвинуть гипотезы — вот основные задачи врачей на этом этапе диагностики.
- Сбор анамнеза. Исследование семейной истории. Если в роду были люди, страдавшие гемофилией или нарушениями свертывания, вероятность встретиться с подобной же проблемой велика. Какую роль сыграл этот фактор — нужно выяснять отдельно.
Иногда суть лежит глубже, чем кажется. Отсутствие предков с плохой генетикой также не является основанием отбрасывать версию с гемофилией. Возможно, имеет место спонтанная мутация.
- Исследование свертываемости крови. Коагулограмма. Используется для констатации факта наличия проблемы у пациента. Больше информации получить таким способом невозможно.
- Специфические тесты для выявления концентрации факторов свертывания. Наиболее полезны в рамках диагностики.
- УЗИ брюшной полости. Применяется, чтобы оценить сохранность органов пищеварительного тракта, частично и почек. Поскольку на фоне течения гемофилии они в особенности становятся мишенями.
- Оценка общего неврологического статуса пациента. Посредством рутинных методов.
По потребности проводятся дополнительные мероприятия. В основном же достаточно и названных.
Гемофилия представляет собой междисциплинарную проблему. Она бьет по всему организму. Потому при проведении обследования необходимо привлекать группу специалистов: от гематолога до педиатра (терапевта) и прочих.
Лечение
Коррекция представляет существенные трудности и ставит пациента в зависимое положение от препаратов. Без них шансов на выживание, особенно при тяжелых формах, нет вообще.
Что именно вводится больному:
- Заместители факторов свертывания. Собственно средства, которые работают как естественные вещества, обеспечивающие гомеостатическую функцию. Применяются систематически. В зависимости от формы патологического процесса частота введения может составлять от раза до трех в неделю. Плюс-минус, исходи из клинической ситуации. Концентрация также подбирается в индивидуальном порядке.
- Поскольку факторы свертывания по химической и биологической структуре представляют собой белки, при длительном лечении практически не миновать иммунного ответа организма пациента. Это большая проблема. По потребности назначаются иммуносупрессоры. Препараты, угнетающие активность защитных сил.
- Препараты-гемостатики. Средства для остановки кровотечений. В основном их вводят в разгар процесса. Чтобы остановить нарушение и не допустить критических осложнений. Наименования подбираются отдельно.
- Хорошо зарекомендовал метод переливания эритроцитарной массы и плазмы. В определенные моменты, с периодичностью раз в несколько лет или чаще. Метод позволяет на некоторое время снизить интенсивность симптоматики.
- Также проводится плазмаферез.
В обязательном порядке лечение гемофилии дополняется диетой с высоким содержанием витаминов и фосфора. Показан систематический контроль состояния. По потребности, но не реже раза в три месяца.
Прогноз
Перспективы весьма туманные. При легкой степени нарушения риски летального исхода минимальны. Пациенты проживают долго, без особых проблем.
При планировании операции наличие гемофилии учитывается, предпринимаются дополнительные меры. Средняя требует постоянного лечения без гарантий результата. Если соблюдать все рекомендации также есть хорошие шансы на сохранение жизни.
Что касается тяжелой степени, вероятность смерти максимальна. Погибает 8 из 10 пациентов в течение первых нескольких лет от появления на свет. К счастью, и это не приговор. Хотя перспективы хуже всего.
Последствия
Основное осложнение — массивное кровотечение, летальный исход. Среди менее очевидных — нарушения работы внутренних органов вплоть до функциональной недостаточности и даже полной несостоятельности. Отклонения со стороны опорно-двигательного аппарата.
Гемофилия — крайне опасное заболевание. Без лечения в большинстве своем ведет к смерти пациента в короткие сроки. Необходимо помощь группы специалистов.
Источник: CardioGid.com
