Подготовка пациента осуществляется по общим правилам для проведения катетеризационных вмешательств на крупных сосудах. Проведение общего наркоза для проведения ЭФИ не показано. Если нет необходимости, не применяются и другие седатирующие препараты, в связи с их вагусными или симпатическими влияниями на сердце. Перед проведением исследования отменяются все препараты, имеющие антиаритмическое влияние на сердце. В большинстве случаев катетеры вводят в правое сердце, что требует доступа через венозную систему. Для венозного доступа пригодны бедренная,
нкция проводится под местной анестезией раствором новокаина или другим анестетиком. После пункции через иглу проводится проволочный проводник, по которому, после удаление иглы, в сосуд вводится интрадьюсер необходимого диаметра и длины. Желательно, чтобы интрадьюсер имел клапан обратного тока и боковой канал для введения через него гепарина или других растворов. После установки интрадьюсеров, через них обязательно необходимо болюсом ввести раствор гепарина, 1,5 тысячи ЕД болюсом и далее, через каждые 30 минут по 500 ЕД для профилактики тромбоэмболических осложнений. Проведение и установка электродов осуществляется под рентгеноскопическим контролем. Места установки электродов определяются задачей проведения ЭФИ. Наиболее общепринятой схемой установки является следующая: двух – четырехполюсный электрод в правом предсердии, четырех – шестиполюсный электрод в коронарный синус, четырех – шестиполюсный электрод в области пучка Гиса, двухполюсный электрод — в области верхушки правого желудочка.
Источник: www.medicus.ru
Содержание
ЭФИ И ПОКАЗАНИЯ К ЕГО ПРОВЕДЕНИЮ
Более 30 лет тому назад впервые с помощью электродного катетера зарегистрирована электрическая активность пучка Гиса. Это открытие стало новым шагом в развитии существующих представлений о механизмах нарушений ритма сердца и проводимости. Сначала эта методика получила название «исследование пучка Гиса», но уже в 1970 г. (Sheslag et al.) был внедрен термин «электрофизиологическое исследование» (ЭФИ). С того времени ЭФИ активно развивается и широко применяется в клинической практике. Применение ЭФИ дает возможность не только по-новому рассмотреть и понять механизмы нарушений ритма и проводимости сердца, но и подобрать оптимальную тактику лечения пациентов. Сформировались принципиально новые представления о механизмах действия антиаритмических средств. Благодаря активному внедрению ЭФИ в клинику получили интенсивное развитие кардиохирургические методы лечения аритмий, появился новый терапевтический метод — катетерная радиочастотная деструкция.
Задача внутрисердечного ЭФИ
- Определение функциональных характеристик проводящей системы сердца.
- Изучение механизмов аритмии, факторов ее индукции и прекращения, выявление анатомических субстратов аритмии на основе анатомо-электрофизиологических характеристик.
- Точная топическая диагностика субстрата аритмии перед радикальным хирургическим вмешательством или катетерной абляцией.
- Выявление аритмической патологии у больных с синкопальными состояниями, выявление больных с риском внезапной смерти.
- Осуществление подбора медикаментозной терапии (медикаментозное тестирование).
- Подбор режимов антитахикардитической электрокардиостимуляции, режимов кардиоверсии и дефибрилляции при имплантации кардиовертеров-дефибрилляторов.
- Проведение катетерной деструкции субстратов аритмии.
Требования к электрофизиологическим лабораториям
Инвазивные ЭФИ должны выполняться в центрах, которые имеют кардиологическую, анестезиологическую и кардиохирургическую службы, при наличии оборудованного кабинета ЭФИ, персонала, подготовленного по клинической электрофизиологии сердца. Неинвазивное ЭФИ могут выполнять на базе кабинетов функциональной диагностики кардиологических отделений при обеспечении их эффективными быстродействующими препаратами, дефибрилляторами и возможностями быстрой транспортировки больного в реанимационное отделение.
Требования к персоналу лаборатории ЭФИ
В проведении ЭФИ принимают участие такие специалисты: 2 врача-электрофизиолога, анестезиолог, инженер-электронщик и медицинская сестра. Персонал лаборатории работает в условиях рентгеновского облучения. Кардиохирурги привлекаются для предоставления хирургической помощи при возникновении угрожающих для жизни осложнений.
Оборудование лаборатории ЭФИ
- Рентгенотелевизионная система передвижного или стационарного типа.
- Универсальный электрокардиостимулятор.
- Многоканальное регистрирующее устройство для синхронной регистрации ЭКГ и внутрисердечных электрограмм.
- Эндокардиальные электроды.
- Оборудование для проведения реанимации.
Протокол ЭФИ
Под местной анестезией пунктируют и катетеризируют большую вену (обычно бедренную или подключичную) и под рентгенологическим контролем устанавливают эндокардиальные электроды в разных отделах сердца. Стандартными позициями электродов являются верхние отделы правого предсердия (HRA, high right atrium), венечный синус сердца (CS, coronary sinus), AV-соединение с пучком Гиса (НВ, His band), верхушечным отделом ПЖ (RV, right ventricular). Для размещения электрода в венечном синусе его вводят в левую подключичную или яремную вену. После проведения электродов в типичные позиции регистрируют полостные эндокардиальные электрограммы, обычно в биполярном режиме с синхронной записью стандартных и грудных отведений на разной скорости протяжения ленты (50 и 100 мм·с-1). После анализа базовых интервалов гисограммы на синусовом ритме приступают к выполнению стимуляции различных камер сердца. Обычно применяют биполярную стимуляцию с дистальным полюсом электрода как катода. В большинстве употребляемых в данное время протоколов стимуляций используется сила тока, которая в 2 раза превышает порог стимуляции (1–4 мА). Продолжительность стимулирующего импульса обычно 1–2 мс.
На электрограмме определяют такие интервалы (рис. 5.1).
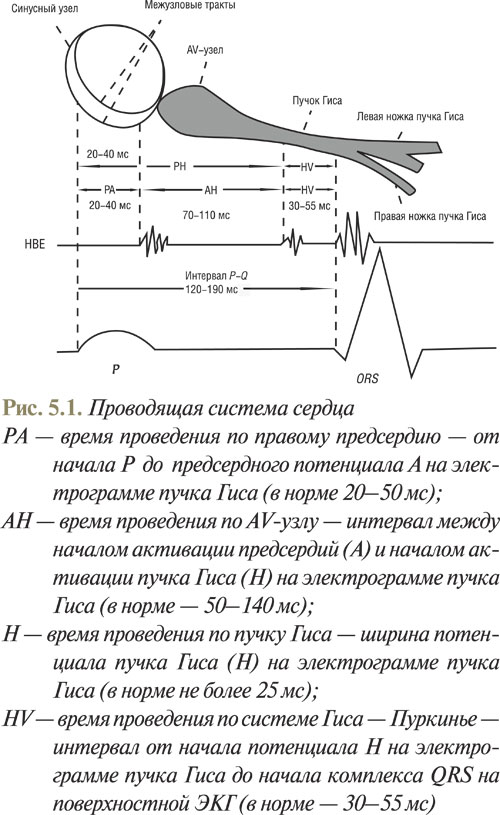
При проведении ЭФИ рекомендуют такую последовательность выполнения протокола исследования:
- Анализируют состояние проводящей системы сердца на начальном ритме по анализу базовых показателей электрограммы;
- Оценивают функцию синусного узла;
- Возрастающая по частоте стимуляция предсердия для оценки антероградного проведения и точки Венкебаха;
- Программированная стимуляция правого предсердия одним и двойным экстрастимулом на спонтанном и заданном ритме (2–3 базовых цикла);
- Стимуляция ПЖ вначале на верхушке, затем при необходимости на выходном тракте в 2–3 базовых циклах одним или двумя экстрастимулами;
- Далее можно выполнять медикаментозные пробы, направленные на выявление преходящих нарушений функции синусного узла и AV-проведения или провокацию пароксизмальных тахиаритмий.
Последовательность выполнения программы исследования может отличаться в зависимости от цели исследования, патологии и конкретной ситуации, возникающей в процессе проведения ЭФИ. Для получения максимально возможной информации следует придерживаться некоторых принципиальных моментов.
ЭФИ В ИЗУЧЕНИИ ФУНКЦИИ СИНУСНОГО УЗЛА
ЭКГ-проявления дисфункции синусного узла включают синусовую брадикардию в покое, неадекватный хронотропный ответ на нагрузку или стресс, синоатриальную блокаду выхода или остановку синусного узла. Общие проявления включают потерю сознания, предобморочное состояние, кратковременное головокружение или выраженную слабость. Аритмии обычно обусловлены одним или несколькими перечисленными факторами: поражение собственно синусного узла (например идиопатическая дегенерация, фиброз, ишемия или хирургическая травма), нарушение функции автономной нервной системы, а также действием препаратов. Клинически выявление возможной дисфункции синусного узла часто затруднено, поскольку симптомы аномалии могут быть кратковременными и доброкачественными, а у пациентов, не имеющих симптомов, возможно значительное изменение синусового ритма. Были предложены различные инвазивные тесты для оценки функции синусного узла.
Время восстановления функции синусного узла (ВВФСУ) используется для оценки влияния сверхчастой стимуляции на автоматизм синусного узла. Часто вносится поправка на продолжительность синусового цикла (СЦ), что определяется как корректированное время восстановления функции синусного узла (КВВФСУ = ВВФСУ — СЦ). В норме ВВФСУ не превышает 1500–2000 мс, а КВВФСУ — 600 мс. Чувствительность обоих показателей до 60%, специфичность — 88%. Таким образом нормальные их значения не всегда дают возможность исключить наличие дисфункции синусного узла. Рекомендации по проведению ЭФИ для оценки функции синусного узла даны в табл. 5.1.
Таблица 5.1
Рекомендации по проведению ЭФИ для оценки функции синусного узла
Синоатриальное проведение может быть измерено непосредственно или с помощью нанесения предсердного экстрастимула на фоне синусового ритма или при стимуляции предсердия.
Синопредсердная пароксизмальная тахикардия
- Во время тахикардии потенциал верхней части правого предсердия предшествует потенциалу нижней его части и существенным образом не отличается от такового на фоне синусового ритма.
- Тахикардия провоцируется электростимулом, нанесенным в период сердечного цикла, который предшествует блокаде его проведения в синусный узел. Интервал сцепления такого электростимула несколько короче интервала, при котором электростимул замещает синусовый импульс.
- Единичный электростимул, нанесенный на предсердие с несколько меньшим интервалом сцепления, чем тот, при котором возник пароксизм, способен прекратить приступ тахикардии.
- Частая стимуляция также провоцирует и угнетает эктопический ритм.
- Дополнительными критериями диагностики является развитие блокады II степени антероградного проведения импульса в AV-узле во время тахикардии, которая не сопровождается прекращением приступа, а также ретроградная блокада проведения импульса при искусственной стимуляции желудочков.
Предсердная пароксизмальная тахикардия
- Потенциал предсердия предшествует потенциалу пучка Гиса.
- Последовательность распространения возбуждения по предсердию в некоторых случаях нарушена. Если эктопический водитель ритма размещен в нижней части предсердия, потенциал его предшествует потенциалу верхней части правого предсердия; если водитель ритма находится в левом предсердии, то оно возбуждается прежде правого предсердия.
- В некоторых случаях зарегистрированные предсердные потенциалы имеют разную конфигурацию (несколько очагов эктопического ритма).
- Единичными электростимулами невозможно прекратить пароксизм. Частая стимуляция может лишь временно подавить эктопический ритм. В тех случаях, когда прогнозируют реципрокный механизм тахикардии, важнейшим диагностическим признаком считают ухудшение внутрипредсердной проводимости в момент провокации пароксизма.
- Дополнительным признаком является антероградная или ретроградная блокада проведения импульса по AV-узлу, поскольку наличие этих нарушений исключает узловую пароксизмальную тахикардию.
AV-узловая пароксизмальная тахикардия
- Предсердные электростимулы с интервалом сцепления, который постоянно становится короче, вызывают пароксизм тахикардии, возникновению которого предшествует внезапное или постепенное удлинение интервала P–R.
- Потенциал пучка Гиса предшествует во время тахикардии потенциалу желудочка.
- Потенциал нижней части предсердия предшествует потенциалу его верхней части и по времени возникновения совпадает с потенциалом желудочка.
- Стимуляция желудочка с возрастающей частотой или с помощью единичных импульсов с интервалом сцепления, который постоянно укорачивается, сопровождается постепенным замедлением ретроградного распространения возбуждения по предсердию. Это указывает на то, что импульс проводится AV-узлом, а не по дополнительному предсердно-желудочковому соединению.
- Прекращение пароксизма происходит лишь в результате блокирования импульса в AV-узле.
Фибрилляция, трепетание предсердий
Диагноз пароксизмальной мерцательной аритмии обычно не вызывает затруднений, поэтому ЭФИ проводить не обязательно. Лишь при необходимости дифференциации между желудочковой экстрасистолией и аберрантными комплексами следует провести регистрацию электрограммы пучка Гиса. Регистрация потенциала пучка Гиса на гисограмме и нормальной продолжительности интервала Н–V дает возможность утверждать, что желудочковые комплексы являются аберрантными. И, наоборот, отсутствие потенциала Н или значительное укорочение интервала Н–V является характерным для желудочковых экстрасистол. При трепетании предсердий очень четко выделяются волны f, связанные или частично диссоциированные с желудочковыми комплексами.
ЭФИ У ПАЦИЕНТОВ С ПРИОБРЕТЕННОЙ AV-БЛОКАДОЙ/ХРОНИЧЕСКИМ НАРУШЕНИЕМ AV-ПРОВЕДЕНИЯ
Возможность регистрации потенциала пучка Гиса во время ЭФИ дает возможность описать 3 анатомических участка AV-блокады:
а) Проксимальный (над пучком Гиса) — задержка проведения или блокада в AV-узле.
б) Интрагисовый — задержка проведения или блокада в пределах пучка Гиса.
в) Дистальный — размещен дистальнее пучка Гиса и располагается на уровне ножек пучка Гиса.
Такая диагностика является крайне важной, поскольку прогноз больных с AV-блокадой зависит от уровня блокады: чем ниже уровень блокады, тем хуже прогноз.
При прогрессирующем повышении частоты стимуляции правого предсердия отмечают постепенное удлинение интервала А–Н до развития AV-блокады II степени на уровне AV-узла — «точка Венкебаха». В норме этот показатель превышает 110–130 импульсов в минуту.
Есть определенные корреляции между картиной ЭКГ и уровнем блокады. При AV-блокаде II степени I типа с узкими комплексами QRS блокада обычно возникает на уровне AV-узла, реже может локализоваться в пучке Гиса. При AV-блокаде II степени тип I с широкими комплексами QRS (блокада ветви пучка Гиса) блокада проведения может возникать на уровне AV-узла, внутри или ниже пучка Гиса. AV-блокада II степени II типа обычно возникает на уровне пучка Гиса или ниже и чаще объединяется с блокадой ножки пучка Гиса. Изредка AV-блокада II типа возникает в AV-узле. При полной AV-блокаде с выскальзывающим ритмом и узкими комплексами QRS место блокады может локализоваться в AV-узле или пучке Гиса. При полной AV-блокаде с выскальзывающим ритмом с широкими комплексами QRS место блокады может располагаться в AV-узле, внутри или ниже пучка Гиса. Обычно она расположена ниже пучка Гиса.
Прогноз пациентов с AV-блокадой зависит от уровня ее возникновения. Хроническая AV-блокада I степени, особенно блокада на уровне AV-узла, обычно имеет доброкачественное течение. Данная аномалия часто связана с приемом лекарственных препаратов и имеет обратимый характер. Клиническое течение узловой AV-блокады II степени обычно доброкачественное, прогноз зависит от наличия и состояния основного заболевания сердца. Прогноз пациентов с AV-блокадой II степени на уровне пучка Гиса неоднозначный. У таких пациентов часто возникают потери сознания и проявления СН. При отсутствии лечения AV-блокада II степени на уровне ниже пучка Гиса имеет плохой прогноз, блокада у таких пациентов часто прогрессирует до более высоких степеней, появляется симптоматика с потерей сознания. У пациентов с приобретенной полной AV-блокадой без лечения часто отмечают симптоматику независимо от уровня блокады (табл. 5.2).
Согласно электрокардиографической классификации внутрижелудочковая проводящая система состоит из 3 пучков: переднего и заднего пучков левой ножки пучка Гиса и правой ножки пучка Гиса. Анатомическая основа деления проводящей системы у человека на 3 пучка не совсем понятна. Пациенты с двухпучковой блокадой имеют повышенный риск развития полной трехпучковой блокады.
Таблица 5.2
Рекомендации по проведению ЭФИ у пациентов с приобретенной AV-блокадой
Внезапная смерть пациентов с двухпучковой блокадой может быть вызвана не только развитием полной трехпучковой блокады, но также и развитием желудочковых тахиаритмий. Последние могут играть важную роль у пациентов с прогресирующим заболеванием сердца и двухпучковой блокадой. По этой причине ЭФИ пациентов с дефектами внутрижелудочкового проведения и необъяснимыми симптомами должно также включать исследование AV-проводящей системы и оценку функции синусного узла, а также программированную предсердную и желудочковую стимуляцию с целью провокации тахиаритмии для выявления склонности к развитию как брадиаритмий, так и тахиаритмий (табл. 5.3).
Таблица 5.3
Рекомендации по проведению ЭФИ
ЭФИ В ДИАГНОСТИКЕ ПАЦИЕНТОВ С ТАХИКАРДИЕЙ И ШИРОКИМИ КОМПЛЕКСАМИ QRS
При широких комплексах QRS (>120 мс) важно дифференцировать наджелудочковую тахикардию от желудочковой тахикардии. Для отличия наджелудочковых тахикардий от желудочковых стойкие симптомы тахикардии непоказательны. Если диагноз наджелудочковой тахикардии невозможно подтвердить или установить, то тахиаритмию следует расценивать как желудочковую тахикардию и лечить соответственно.
Тахикардия с широкими комплексами QRS может быть разделена на 3 группы: наджелудочковая тахикардия с блокадой ножек пучка Гиса, наджелудочковая тахикардия с проведением по дополнительному предсердно-желудочковому соединению и желудочковая тахикардия. ЭФИ позволяет точно диагностировать практически все тахикардии с широкими комплексами, а также определить последовательность и соотношение между активацией предсердий и желудочков. При этом можно зарегистрировать электрограммы от структур, которые не отображаются на стандартной ЭКГ (таких как пучок Гиса или дополнительные пути проведения), а также могут быть проанализированы ответы на разные пробы со стимуляцией. Поскольку знание механизма аритмии обычно имеет критическое значение для выбора надлежащей терапии, ЭФИ часто занимают важное место в клинической диагностике у пациентов, имеющих тахикардии с широкими комплексами (табл. 5.4).
Таблица 5.4
Рекомендации по проведению ЭФИ у пациентов с тахикардией и широкими комплексами QRS
ЭФИ В ДИАГНОСТИКЕ ПАЦИЕНТОВ С ТАХИКАРДИЕЙ И УЗКИМИ КОМПЛЕКСАМИ QRS
Таблица 5.5
Рекомендации по проведению ЭФИ у пациентов с тахикардией и узкими комплексами QRS
ЭФИ У ПАЦИЕНТОВ С УДЛИНЕННЫМ ИНТЕРВАЛОМ Q-T
Удлинение интервала Q–T, связанное с потенциальной угрозой возникновения опасных для жизни аритмий, может регистрироваться постоянно или периодически как проявление врожденного синдрома удлиненного интервала Q–T или может возникать вследствие метаболических, токсических или патофизиологических факторов. ЭФИ имеет ограниченное значение для выявления, постановки диагноза или подбора терапии при врожденном или приобретенном удлинении интервала Q–T. ЭФИ у пациентов с врожденным синдромом удлиненного Q–T нередко приводит к запуску желудочковых аритмий, тогда как его диагностическое значение невысоко или отсутствует совсем (табл. 5.6).
Таблица 5.6
Рекомендации для проведения ЭФИ у пациентов с удлиненным интервалом Q–T
НАДЖЕЛУДОЧКОВЫЕ ТАХИКАРДИИ ПРИ ДОПОЛНИТЕЛЬНЫХ ПУТЯХ ПРОВЕДЕНИЯ
Дополнительные пути Кента и Джеймса
- Навязывание ритма предсердия, постоянно возрастающего по частоте, или нанесение отдельных стимулов с постоянным укорочением интервала сцепления при наличии пучка Кента приводит к росту выраженности волны дельта, интервал Р — дельта-волна остается стабильным. При этом как для пучка Кента, так и для пучка Джеймса характерен на определенном этапе скачкообразный переход проведения импульсов лишь по дополнительному предсердно-желудочковому соединению.
- Программированная стимуляция предсердия, вызывая пароксизм тахикардии, не выявляет отличитальных особенностей, присущих AV-узловой тахикардии, то есть внезапного удлинения интервала А–Н или появления периодики Венкебаха.
- Программированная стимуляция желудочка не сопровождается увеличением времени ретроградного проведения возбуждения на предсердие, которое отражает его распространение по дополнительному предсердно-желудочковому соединению, а не по AV-узлу.
- Выявляет нарушение последовательности ретроградного распространения волны возбуждения на предсердие. Это проявляется тем, что потенциал левого предсердия регистрируется раньше, чем правого.
- Дополнительным признаком является регистрация нижнепредсердного потенциала на гисограмме после желудочкового комплекса в отличие от узловой тахикардии, при которой этот потенциал по времени возникновения совпадает с желудочковым.
Дополнительный путь Махайма
- Потенциал Н на гисограмме по времени возникновения совпадает с деформированным желудочковым комплексом в отведении электрограммы от желудочка и предшествует ему, тогда как регистрируемый комплекс QRS нормальной формы.
- Частая стимуляция предсердия приводит к удлинению интервала P–Q и укорочению интервала H–V или даже к его слиянию с желудочковым комплексом, что сочетается с возникновением его аберрации по типу блокады одной из ножек пучка Гиса.
- Аберрантный желудочковый комплекс нормализуется после введения атропина или на фоне стимуляции пучка Гиса.
ЭФИ у пациентов с WPW-синдромом
Рекомендации по проведению ЭФИ у пациентов с WPW-синдромом приведены в табл. 5.7.
Таблица 5.7
Рекомендации по проведению ЭФИ у пациентов с WPW-синдромом
ЭФИ У ПАЦИЕНТОВ С ЖЕЛУДОЧКОВЫМИ ЭКСТРАСИСТОЛАМИ, ПАРНЫМИ ЭКСТРАСИСТОЛАМИ И НЕСТОЙКОЙ ЖЕЛУДОЧКОВОЙ ТАХИКАРДИЕЙ
Таблица 5.8
Рекомендации по проведению ЭФИ у пациентов с желудочковыми экстрасистолами, парными экстрасистолами и нестойкой желудочковой тахикардией
Пароксизмальные желудочковые тахикардии
- Наличие предсердно-желудочковой диссоциации, которая регистрируется на электрограмме пучка Гиса. Этот критерий является очень важным, но не абсолютным, так как выявляется, хотя и очень редко, при наджелудочковых тахикардиях с аберрантной желудочковой проводимостью.
- Отсутствие потенциала Н перед желудочковыми комплексами или значительное укорочение интервала Н–V на гисограмме.
- Частая и программированная стимуляция ПЖ в большинстве случаев приводит к возникновению желудочковой тахикардии. Конфигурация комплексов при этом аналогична тем, которые возникают во время спонтанно возникшего приступа.
- Программированная стимуляция желудочков в большинстве случаев приводит к прекращению тахикардии. Желудочковая тахикардия с частотой ритма <175 уд./мин прекращается отдельными электростимулами или с помощью навязывания искусственного желудочкового ритма небольшой частоты. Для ее прекращения при тахикардии >175 уд./мин используют парные стимулы или частую стимуляцию желудочков.
ЭФИ У ПАЦИЕНТОВ С НЕОБЪЯСНИМОЙ ПОТЕРЕЙ СОЗНАНИЯ
Таблица 5.9
Рекомендации по проведению ЭФИ у пациентов с необъяснимой потерей сознания
ЭФИ У ПАЦИЕНТОВ, ВЫЖИВШИХ ПОСЛЕ ОСТАНОВКИ СЕРДЦА
Таблица 5.10
Рекомендации по проведению ЭФИ у пациентов, выживших после остановки сердца
ЭФИ У ПАЦИЕНТОВ С НЕОБЪЯСНИМЫМ СЕРДЦЕБИЕНИЕМ
Таблица 5.11
Рекомендации по проведению ЭФИ у пациентов с необъяснимым сердцебиением
ЭФИ ПРИ ПОДБОРЕ АНТИАРИТМИЧЕСКОЙ ТЕРАПИИ У РАЗНЫХ ГРУПП ПАЦИЕНТОВ
ЭФИ позволяет серийно оценивать вызванные лекарственными препаратами изменения проводимости и рефрактерности тканей сердца, а также особенности аритмий, включая индуцированность; при индуцированных аритмиях — оценить частоту, морфологию и гемодинамические последствия. После базового исследования (желательно без препаратов), в течение которого индуцируется аритмия, назначается препарат и повторяется электрическая стимуляция. Предполагается, что вызванное антиаритмическим препаратом снижение возможности повторно индуцировать аритмию свидетельствует об отсутствии рецидивов аритмии. Наоборот, если аритмия остается индуцированной, то достоверность повтора аритмии выше, чем в группе больных, где удалось достичь ее прекращения препаратами. Такой подход используется прежде всего у пациентов со стойкими желудочковыми тахикардиями и у пациентов, которые выжили после остановки сердца, хотя проведение ЭФИ возможно и у пациентов с наджелудочковыми аритмиями (табл. 5.12).
Таблица 5.12
Рекомендации по проведению ЭФИ при подборе антиаритмической терапии у разных групп пациентов
ЭФИ У ПАЦИЕНТОВ, ЯВЛЯЮЩИХСЯ КАНДИДАТАМИ ИЛИ УЖЕ ИМЕЮЩИХ ИМПЛАНТИРОВАННЫЕ АНТИАРИТМИЧЕСКИЕ УСТРОЙСТВА
Таблица 5.13
Рекомендации по проведению ЭФИ у пациентов, являющихся кандидатами или уже имеющих имплантированные антиаритмические устройства
ЛИТЕРАТУРА
- Бредикис Ю.Ю. (1967) Электрическая стимуляция сердца в клинической практике. М: Медицина, 200 с.
- Бредикис Ю.Ю., Дрогайцев А.Д., Стирбис П.П. (1983) Физиологическая электростимуляция сердца: Обзор. Кардиология, 9, 114-118.
- Емельяненко В.М., Ефремов А.И., Кофаль Л.А. и др. (1995) Критерии клинической оценки тяжести нарушений ритма сердца. Клин мед и патофизиол; 2, 92-93.
- Ревишвили А.Ш. (1990) Электрофизиологическая диагностика и хирургическое лечение наджелудочковых тахиаритмий. Кардиология, 11, 56-59.
- Черняк Б.А., Никитина Т.Н., Фукс Р.А. и др. (1983) Клинико-функциональная характеристика синдрома преждевременной реполяризации желудочков. Тер арх; 4, 57-61.
- Шевченко Н.М. (1997) Рациональная кардиология, М., Стар’Ко, 256 с.
- Шубик Ю.В. (1999) Неинвазивное электрофизиологическое исследование при аномалиях проводящей системы сердца. СПб., ИНКАРТ, 84 с.
- Akhtar M., Achord J.L., Reynolds W.A. (1994) Clinical competence in invasive cardiac electrophysiological studies. ACP/ACC/AHA Task Force on Clinical Privileges in Cardiology. J Am Coll Cardiol; 23, 1258-1261.
- Andresen D., Steinbeck G., Habort R. et al. (1990) Programmed ventricular stimulation: Prognostic volue of noninducibility in patients with malignant ventricular tachyarhythmias. Eur. Heart J., Vol. 11, Abstr. Suppl. 3.
- Blomstrm-Lundqvist, Scheinman М.М. et al. ACC/AHA/ESC Guidelines for the Management of Patients With Supraventricular Arrhythmias — Executive Summary A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Supraventricular Arrhythmias).
- Brembilla-Perrot B., Spatz F., Khaldi E. et al. (1990) Value of esophageal pacing in evaluation of supraventricular tachycardia. Am. J. Cardiol.; 65, 322-330.
- Flowers N.C., Abildskov J.A., Armstrong W.F. et al. (1991) ACC policy statement: recommended guidelines for training in adult clinical cardiac electrophysiology. Electrophysiology. Electrocardiography Subcommittee, American College of Cardiology. J Am Coll Cardiol; 18, 637-640.
- Gallagher J.J., Smith W.M., Kerr C.R. et al. (1982) Esophageal pacing: a diagnostic and therapeutic tool. Circulation. Vol. 65, 2, 336-341.
- Hall R.J.C., Boyle R.M., Webb-Peploe M. et al. (1995) Guidelines for specialist training in cardiology. Council of the British Cardiac Society and the Specialist Advisory Committee in Cardiovascular Medicine of the Royal College of Physicians. Br Heart J; 73, 1-24.
- Hindricks G., for the Multicentre European Radiofrequency Survey (MERFS) investigators of the Working Group on Arrhythmias of the European Society of Cardiology (1993) The Multicentre European Radiofrequency Survey (MERFS): complications of radiofrequency catheter ablation of arrhythmias, fur Heart J; 14, 1644-1653.
- Horowitz L.N., Josephson M.E. (1990) Intracardiac electriphysiological tidy as a method of optimization of drug therapy in chronic V.T. Progr. Cardiovasc. Res. Vol. 2, 381-389.
- Josephson M.E., Maloney J.D., Barold S.S. (1995) Guidelines for training in adult cardiovascular medicine. Core Cardiology Training Symposium (COCATS) Task Force 6: training in specialized electrophysiology, cardiac pacing and arrhythmia management. J Am Coll Cardiol; 25, 23-26.
- Miller J.M. (1996) Therapy of Wolff-Parkinson-White syndrome and concealed bypass tracts. J Cardiovasc Electrophysiol., Vol. 7, 1, 85-93.
- Santini M., Ansalone G., Cacciatore G. et al. (1990) Transesophageal pacing. PACE, Vol. 13, 10, 1298-1323.
- Snezhitsky V.A., Baranovsky P.A., Roman T.S. et al. (1994) Transesophageal atrial programmed pacing for assessment of atrioventricular conduction function. RBM, Vol. 16, 3-4, 120-123.
- Zipes D.P., DiMarco J.P., Gillette P.C. et al. (1995) Guidelines for clinical intracardiac electrophysiological and catheter ablation procedures. A report of the American College of Cardiology. American Heart Association Task Force on practice guidelines. J Cardiovasc Electrophysiol., Vol. 6, 8, 652-679.
- Zipes D.P., DiMarco J.P., Gillette P.C. et al. (1995) Guidelines for clinical intracardiac electrophysiological and catheter ablation procedures: a report of the American College of Cardiology. American Heart Association Task Force on Practice Guidelines (Committee on Clinical Intracardiac Electrophysiologic and Catheter Ablation Procedures), developed in collaboration with the North American Society of Pacing and Electrophysiology. J Am Coll Cardiol; 26, 555-573.
Источник: compendium.com.ua
Суть метода, преимущества и недостатки
Сущность ЭФИ обследования сердца заключается в следующем:
- Обычно различные нарушения ритма сердца или ишемическая болезнь сердца могут быть установлены на основании стандартной электрокардиограммы.
- Если же аритмию или ишемию миокарда не удается зарегистрировать с помощью однократной ЭКГ, врач назначает проведение суточного мониторирования АД и ЭКГ по Холтеру. В условиях обычной бытовой активности за сутки в большинстве случаев могут быть зарегистрированы указанные заболевания.
- Если и по монитору не удалось их отследить, пациент выполняет пробы с физической нагрузкой. Как правило, на основании таких проб (велосипед, беговая дорожка, тест 6-минутной ходьбы) устанавливается точный диагноз, так как сердце находится в условиях повышенной нагрузки, но повышенной естественным путем (ходьба, бег).
- Когда же вышеперечисленные методики не позволяют достоверно установить диагноз аритмии или ишемии, а у пациента сохраняются жалобы со стороны сердца, ему назначается ЭФИ (электрофизиологическое исследование сердца).
При ЭФИ нагрузка на сердце тоже возрастает, но не вследствие физической активности, а в результате электрической стимуляции миокарда. Такая стимуляция проводится с помощью электродов, которые начинают подавать к сердечной мышце электротоки физиологической мощности, но с высокой частотой. В итоге миокард сокращается быстрее, возникает спровоцированное учащение сердцебиения. А при высокой частоте сердечных сокращений возникают либо аритмия, либо ишемия, если у человека уже имеются патологические процессы в миокарде, являющиеся предпосылками к развитию этих заболеваний. Другими словами, ЭФИ позволяет спровоцировать искомые заболевания и зарегистрировать их на ЭКГ с целью дальнейшего лечения пациента.
А вот в зависимости от того, каким образом электроды подводят к сердечной мышце, выделяют три разновидности методики:
- Чреспищеводное ЭФИ (ЧПЭФИ). Электроды подводятся с помощью зонда, вводимого в просвет пищевода. Является неинвазивной методикой, а по технике напоминает обычную фиброгастроскопию. Выполняется чаще, чем следующие два вида ЭФИ. (На технике проведения ЧПЭФИ в этой статье слишком подробно останавливаться не будем, о нем есть отдельный материал).
- Эндокардиальное ЭФИ (эндоЭФИ). Является инвазивной методикой, электроды с помощью стерильного зонда вводятся в крупные сосуды и продвигаются под контролем рентген-оборудования. Относится к высоко-технологичным видам медицинской помощи (ВТМП). Несмотря на сложность выполнения, а также необходимость использования высококлассного кадрового и дорогостоящего технического оснащения, является очень информативным методом диагностики, а кардиологические заболевания выявляет лучше, чем ЧПЭФИ.
- Эпикардиальное ЭФИ (эпиЭФИ). Также является инвазивной методикой, когда стимуляция миокарда проводится во время операции на открытом сердце с рассечением грудной клетки (торакотомия). По информативности не уступает эндоЭФИ. В связи с таким недостатком, как необходимость торакотомии, выполняется в основном при проведении операции на сердце по поводу других заболеваний.
Когда показано проведение ЭФИ?
Любое из видов ЭФИ проводится при наличии у пациента определенных жалоб, которые врачу не удается связать с выявленными по ЭКГ нарушениями или которые возникают у пациента при удовлетворительных результатах обследования, либо при подозрении на определенные заболевания.
Так инвазивное ЭФИ сердца проводится при возникновении симптомов следующего характера:
- Приступообразные перебои в работе сердца, особенно кратковременные, но вызывающие значительный субъективный дискомфорт,
- Перебои в сердце, сопровождающиеся выраженным общим плохим самочувствием, а также одышкой и хрипами в грудной клетке в покое, голубым окрашиванием носогубного треугольника или кожи других участков тела (цианоз), сильной бледностью кожи, очень высоким или низким артериальным давлением, интенсивными болями за грудиной или в грудной клетке слева,
- Потеря сознания и предобморочные состояния, при исключении патологии центральной нервной системы или других заболеваний (в случае кардиологических причин потеря сознания называется приступом или эквивалентом Морганьи-Адамса-Стокса, приступом МЭС),
- Эпизоды остановки сердца (асистолии), приводящие к клинической смерти с успешной реанимацией пациента.

Из заболеваний, требующих выполнения инвазивного ЭФИ сердца для уточнения диагноза, можно отметить такие, как:
- Пароксизмальные виды аритмий – мерцание-трепетание предсердий, наджелудочковая тахиаритмия, частая желудочковая экстрасистолия с переходом в желудочковую тахикардию,
- Синдром слабости синусового узла (СССУ), сопровождающийся чередованием тахи- и брадикардии (синдром тахи-бради), а также брадикардией с вышеупомянутыми приступами МЭС,
- Фибрилляция желудочков с переходом в асистолию,
- Ишемическая болезнь сердца.
В том случае, когда ЧПЭФИ не помогает достоверно установить или исключить диагноз, то есть в диагностически неясных случаях, пациенту проводится эндо- или эпиЭФИ.
Кроме этого, эндоЭФИ проводится в рамках интраоперационного обследования при выполнении внутрисосудистой операции РЧА (радиочастотной аблации), при которой внутрисердечным зондом разрушаются патологические пути следования импульса, являющиеся причиной того или иного типа аритмии.
В каких случаях проведение ЭФИ противопоказано?
Любой из видов ЭФИ сердца имеет ряд противопоказаний. К ним относятся следующие:
- Развитие у пациента острого инфаркта или инсульта,
- Возникновение лихорадки, острого инфекционного заболевания,
- Нестабильная стенокардия (впервые возникшая или прогрессирующая),
- Подозрение на тромбоэмболию легочной артерии (ТЭЛА),
- Острая хирургическая патология,
- Тяжелая декомпенсация хронических заболеваний (сахарный диабет, бронхиальная астма),
- Развитие острой сердечной недостаточности (сердечная астма, отек легких), или тяжелая декомпенсация хронической сердечной недостаточности,
- Декомпенсированные пороки сердца,
- III стадия хронической сердечной недостаточности,
- Выраженная дилатационная кардиомиопатия с низкой фракцией выброса (менее 20=30%).
Как подготовиться к процедуре?
Все нюансы подготовки к исследованию должны быть тщательно разъяснены врачом пациенту. Во первых, пациент (под контролем и по указанию врача !) должен прекратить прием любых антиаритмических препаратов, так как они способны исказить результаты исследования. Во вторых, перед процедурой ЧПЭФИ, пациенту, испытывающему даже незначительный дискомфорт со стороны желудка, необходимо провести фиброгастроскопию с целью исключения острой гастро-эзофагеальной патологии.

Перед процедурой эндоЭФИ по поводу приступов потери сознания врач-невропатолог должен исключить патологию головного мозга, способную послужить причиной обмороков, а для этого может потребоваться проведение КТ или МРТ черепа.
В связи с тем, что проведение эндо- или эпиЭФИ требует госпитализации в стационар, пациенту, проходящему обследование в плановом порядке, необходимо предоставить врачу результаты анализов на ВИЧ, сифилис, гепатиты и на свертываемость крови не позднее двухнедельной давности (в разных учреждениях свои сроки).
Исследование проводится строго натощак. Необходимость проведения эпиЭФИ натощак обусловлена тем, что во время общего наркоза может возникнуть рвота съеденной пищей или жидкостью и аспирация рвотными массами.
После необходимой подготовки осуществляется госпитализация пациента в стационар. На руках у него должны быть результаты обследования (УЗИ сердца, суточный монитор), а также выписка из амбулаторной карты или выписной эпикриз из учреждения, в котором он получал обследование и лечение до этого. В выписке должно быть указано обоснование необходимости проведения ЭФИ с развернутым клиническим диагнозом.
Проведение ЭФИ сердца
В связи с тем, что суть электрической стимуляции миокарда у всех трех методик одинакова, а ЧПЭФИ по технике напоминает ФЭГДС, есть смысл подробнее остановиться на инвазивных методах ЭФИ.
Итак, инвазивное эндоЭФИ проводится в отделении рентгено-хирургических методов диагностики, в то время, как пациент находится на стационарном лечении в кардиологическом, кардиоаритмологическом или кардиохирургическом отделении.

После небольшой подготовки в виде внутривенного введения седативных препаратов пациент на лежачей каталке доставляется в рентген-хирургию. Врач, проводящий обследование, в условиях полной стерильности осуществляет доступ к бедренной (реже к подключичной) вене под местной анестезией. Делается небольшой надрез вены в наиболее удачном для методики месте (называется венесекцией).
Далее через полученный разрез в вену пациента вводится тонкий пластиковый или металлический проводник, называемый интродьюсером. По нему подводится зонд с электродами на конце, имеющий рентгено-контрастные свойства, и потому видимый на экране. После постепенного продвижения зонда по вене к правому предсердию, контролируемого на экране, и достижения зондом необходимой для исследования камеры сердца (предсердия или желудочка), осуществляется стимуляция миокарда в физиологическом режиме.
Зонд как правило, имеет от трех до пяти миниатюрных электродов, которые подключены к устройству, способному переключать их работу с режима стимуляции на режим регистрации, и наоборот. Запись полученных кардиограмм ведется с помощью компьютерного устройства.
Продолжительность процедуры составляет от получаса и более, не способствуя возникновению значимых болевых ощущений. Больной в течение всей операции находится в сознании. После извлечения зонда на кожу в зоне венесекции будет наложена давящая асептическая повязка.
ЭпиЭФИ проводится в отделении кардиохирургии. После погружения пациента в медикаментозный сон (общий наркоз) осуществляется рассечение грудной клетки с доступом в перикардиальную полость. Вопрос об использовании аппарата искусственного кровообращения (АИК) решается строго индивидуально. После обнажения внутреннего листка наружной оболочки сердца (эпикарда) к нему подводятся электроды, и начинается стимуляция с одновременной регистрацией полученного ответа от сердечной мышцы. Исследование по времени занимает более часа. После осуществления всех необходимых манипуляций рана послойно ушивается, а в плевральной полости остаются дренажи, удаляемые на 2-3-и сутки.
После любого из инвазивных методов ЭФИ пациент остается под наблюдением в отделении интенсивной терапии и реанимации на период времени от суток и более, в зависимости от тяжести состояния пациента.
Возможны ли осложнения?
Как и при любом инвазивном методе исследования, осложнения эндо и эпи ЭФИ возможны, но встречаются они в крайне редких случаях. Основными видами неблагоприятных последствий являются кардиологические острые состояния, спровоцированные искусственно созданной тахикардией. К ним относятся:
- Приступ стенокардии,
- Развитие острого инфаркта миокарда,
- Тромбоэмболические осложнения, вызванные попаданием оторвавшегося из полости сердца тромба, если последний не был выявлен до процедуры с помощью эхокардиографии (УЗИ сердца).
Профилактикой подобного рода осложнений является тщательное обследование пациента перед операцией, а также грамотное определение показаний для обследования.
В постоперационном периоде существует крайне низкая вероятность развития воспалительных и тромбоэмболических осложнений, а также возникновения жизнеугрожающих аритмий.
Расшифровка результатов
Интерпретация результатов проводится врачом, выполняющим исследование и лечащим врачом, направившим пациента на процедуру.
В норме на электрограмме, полученной при ЭФИ, выявляется синусовая тахикардия с ЧСС от 100 до 120 в минуту и более. Такая тахикардия является преходящей и не опасна для пациента.
Если в протоколе исследования указана фраза о том, что с помощью всех видов стимуляции нарушений ритма не достигнуто, значит, подозреваемый тип аритмии у пациента отсутствует, а результаты ЭФИ расцениваются, как нормальные. Также в норме не должно быть обнаружено депрессии или подъема сегмента ST и отрицательных зубцов T, свидетельствующих об ишемии миокарда.
Если же такие изменения выявлены, указывается их локализация, а также вид электростимуляции, при котором они возникли.
При выявлении аритмии указывается ее тип (мерцание предсердий, пробежка желудочковой тахикардии, частая желудочковая экстрасистолия и др), и параметры стимуляции, при которой возникло нарушение ритма.
Любое из нарушений, зарегистрированных на электрограмме, требует тщательного врачебного контроля в связи с необходимостью назначения тех или иных антиаритмических препаратов или проведения РЧА.
Примерная стоимость ЭФИ
ЭФИ сердца может быть проведено в любом крупном лечебном учреждении, располагающим соответствующим кадрово-техническим оснащением. Обычно ЭФИ проводится в областных или районных центрах, а также в городских больницах крупных городов (Москва, Санкт-Петербург, Тюмень, Челябинск и др).
Обычно ЭФИ сердца проводится по квоте Минздрава с использованием денежных средств федерального бюджета. Однако, если пациент может самостоятельно оплатить процедуру, то нет необходимости ждать несколько недель, так как можно провести ЭФИ по платным услугам.
Цены на электрофизиологическое исследование сердца сильно разнятся. Так, стоимость ЧПЭФИ составляет от 2000 до 4000 рублей, в зависимости от учреждения и оборудования. Стоимость эндоЭФИ гораздо выше и составляет до 60-180 тысяч рублей, в зависимости от оплаты зонда и катетеров, а также от оплаты последующего пребывания в клинике.
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос в форму ниже ответит один из ведущих авторов сайта.
На вопросы данного раздела в текущий момент отвечает: Сазыкина Оксана Юрьевна, кардиолог, терапевт
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Источник: sosudinfo.ru
ЭЛЕКТРОФИЗИОЛОГИЧЕСКИЕ ИССЛЕДОВАНИЯ В РКМЦ
Специалистами кабинета ангиографии и рентгенэндоваскулярной хирургии ЭФИ производится с целью определения участка воздействия для проведения радиочастотной аблации очага аритмии (РЧА). Вмешательство проводится под местной анестезией под рентгеновским контролем в специально оборудованной операционной.
В надрез для введения катетера на бедренной или подключичной вене вводится интродьюс (металлический или пластиковый проводник). По нему проводят зонд с электродом. Движение зонда наблюдают на экране благодаря введению контрастного вещества. Зонд проводят до предсердия или желудочка. Врачом производится электростимулирование. При помощи компьютера все данные записываются.
ПРОТИВОПОКАЗАНИЯ
- повышенная температура
- инфекционное заболевание
- сильная стенокардия
- ряд типов пороков сердца
- тяжелая форма сердечной недостаточности
- подозрение на наличие тромбоэмболии лёгочной артерии
- аневризма сердца или аорты
ПОДГОТОВКА К ЭФИ
- За 1-2 недели до процедуры проводятся анализы крови, коагулограмма, ЭКГ в 12 отведениях, рентгенография грудной клетки и Эхо-КГ. При необходимости назначаются дополнительные исследования.
- По рекомендации врача временно отменить прием некоторых лекарств.
- За несколько дней до исследования прекратить курение, употребление кофеина и алкоголя.
- За 8-10 часов до исследования прекратить принимать пищу и жидкости.
КАК ПРОЙТИ ЭЛЕКТРОФИЗИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ В РКМЦ
- Позвонить в Контакт-центр или по тел. (017)543-43-80 для записи на консультацию к рентгено-эндоваскулярному хирургу Сиваку С.А.
- Прийти на консультацию в назначенное время.
- В день проведения процедуры в регистратуре заключить договор на оказание платных услуг
- Оплатить счет в кассе РКМЦ или через ЕРИП
Источник: www.vip-clinic.by
Историческая справка

Несмотря на то, что процедура ЭФИ на сердце начала применяться относительно недавно, сами эксперименты по электрофизиологическим методикам начали применяться еще в конце XVIII века знаменитым врачом Луиджи Гальвани. Он не добился особых результатов, однако на протяжении последующих лет его эксперименты продолжали развивать его ученики и последователи.
Новый виток начинается в 1970-х годах, когда группа ученых вновь открыла интерес к данному методу диагностики. Сейчас все большее количество врачей в своей деятельности пользуются методом ЭФИ сердца.
Суть методики

Сейчас исследования ЭФИ сердца проводится для проведения диагностики проводимости сердечной мышцы и нарушений ритма. В конечном итоге врач может сполна оценить состояние электрической сердечной системы, а с полученными знаниями оптимально подобрать принцип лечения.
Во время проведения ЭФИ сердца различные отделы сердца стимулируются, чтобы выявить имеющиеся нарушения сердечного ритма. Широко применяемые ЭКГ и суточное мониторирование электрокардиографии не позволяют добиться нужного результата в данной ситуации.
В медицине применяется два вида операций ЭФИ на сердце, каждый из которых в свою очередь делится на подвиды.
Расшифровка результатов
Нормальным результатом инвазивных и неинвазивных исследований считается отсутствие нарушений ритма при подаче импульсов через электрод. Иногда при отрицательном результате при ЧПЭФИ требуется его повторное выполнение через 1-2 недели либо пациента готовят к введению электрода в сердце через сосудистую систему.
Если нарушения ритма выявлены, то определяют его свойства:
- разновидность ари src=»https://osostavekrovi.com/wp-content/uploads/2019/02d/elektrofiziologicheskoe-issledovanie-efi-9.jpg» class=»aligncenter» width=»580″ height=»330″[/img]
- длительность приступа,
- время появления,
- характеристика электрических сигналов.
На основании полученных данных определяется тактика ведения пациента, назначается дальнейшее лечение.
Инвазивное исследование

Подобное диагностирование проводится исключительно в стационарных условиях и разделяется на 3 подвида в зависимости от того, как ЭФИ сердца делается.
1. Эндокардиальное ЭФИ проводится при стимуляции внутренней оболочки самого сердца — эндокарда. Сама процедура не приводит к болевым ощущениям, поскольку здесь нет рецепторов боли, поэтому не требуется делать наркоз или давать медикаменты больному.
2. Эпикардиальное ЭФИ сердца стимулирует во время процедуры эпикард, поэтому применяется только в случаях операций на открытой сердечной мышце.
3. Комбинированное исследование применяет совместно оба способа.
Инвазивный метод ЭФИ имеет ряд преимуществ перед неинвазивным — в первую очередь подобным способом можно осуществить стимулирование любой из камер сердца, а всего их в теле четыре.
Преимущества и недостатки метода
Достоинствами этого способа диагностики являются такие возможности:
- обследование редких и коротких форм тахикардий наджелудочкового происхождения;
- изучение точного места, где возможна выработка частых сигналов или блокирования прохождения импульсов;
- можно использовать как альтернативу нагрузочным тестам, при невозможности пациента выполнить задания для таких исследований;
- незначительная травматичность;
- доступность;
- не требуется проникновения в сосудистое русло;
- нет противопоказаний для многократного проведения.
К недостаткам относится дискомфорт во время заведения электрода.
Рекомендуем прочитать статью о том, как проводится фонокардиография. Из нее вы узнаете о том, почему аускультации бывает недостаточно, показаниях для фонокардиографии, вариантах ее проведения, противопоказаниях и расшифровке результата. А здесь подробнее о допплеровской ЭхоКГ.
Неинвазивный метод
Данная методика более известна как чреспищеводное ЭФИ сердца или чреспищеводная электростимуляция. Распространена более широко, поскольку не требуется условий стационара. Проводиться процедура может и при простых амбулаторных условиях, поскольку стимулируется всего лишь 2 отдела сердца: левый желудочек и левое предсердие. Во время операции обязательно требуется применять наркоз, поскольку последствия ЭФИ сердца будут не только неприятны, но и весьма болезненны.
Все особенности проведения подобной процедуры обязательно предварительно решаются и обговариваются совместно с пациентом перед непосредственной отправкой. Но при этом всего одна проведенная процедура может полностью открыть картину на неясный диагноз и установить тактику лечения аритмии у больного.
Условия соглашения
В соответствии с требованиями статьи 9 Федерального закона «О персональных данных» от 27.07.2006 N 152-ФЗ, подтверждаю свое согласие на обработку ФГБУ «Консультативно-диагностический центр с поликлиникой» (далее — Оператор) моих персональных данных, включающих: фамилию, имя, отчество, контактные телефоны, адрес электронной почты, данные о состоянии моего здоровья, заболеваниях, случаях обращения за медицинской помощью — в медико-профилактических целях, в целях установления медицинского диагноза и оказания медицинских услуг при условии, что их обработка осуществляется лицом, профессионально занимающимся медицинской деятельностью и обязанным сохранять врачебную тайну. В процессе оказания Оператором мне медицинской помощи я предоставляю право медицинским работникам передавать мои персональные данные, содержащие сведения, составляющие врачебную тайну, другим должностным лицам Оператора в интересах моего обследования и лечения. Предоставляю Оператору право осуществлять все действия (операции) с моими персональными данными, включая сбор, систематизацию, накопление, хранение, обновление, изменение, использование, обезличивание, блокирование, уничтожение. Оператор вправе обрабатывать мои персональные данные посредством внесения их в электронную базу данных, включения в списки (реестры) и отчетные формы, предусмотренные документами, регламентирующими порядок ведения и состав данных в учетно-отчетной медицинской документации. Срок хранения моих персональных данных соответствует сроку хранения первичных медицинских документов (медицинской карты) и составляет двадцать пять лет для стационара и пять лет для поликлиники. Передача моих персональных данных иным лицам или иное их разглашение может осуществляться только с моего письменного согласия. Настоящее согласие дано мной и действует бессрочно. Я оставляю за собой право отозвать свое согласие посредством составления соответствующего письменного документа, который может быть направлен мной в адрес Оператора по почте заказным письмом с уведомлением о вручении либо вручен лично под расписку представителю Оператора. В случае получения моего письменного заявления об отзыве настоящего согласия на обработку персональных данных Оператор обязан: по истечении указанного выше срока хранения моих персональных данных уничтожить (стереть) все мои персональные данные из баз данных автоматизированной информационной системы Оператора, включая все копии на машинных носителях информации, без уведомления меня об этом.
Назначения врача
Из-за современного ритма жизни все чаще люди обращаются к врачам с проблемой аритмии, то есть нарушением сердечного ритма. Стандартно у здорового человека электрические сигналы проходят через сердце однообразно и очень четко. Но при этом повышенное давление, старение, сердечные приступы и многие иные причины могут привести к тому, что постепенно сердце начинает покрываться рубцами или кальциевыми отложениями. Все это сильно препятствует импульсам. Что и ведет к нарушениям сердечного ритма — будет ли это регулярность или последовательность пульса. Подобные нарушения и может выявить ЭФИ сердца.
Что такое чреспищеводная эхокардиография?
ЧПэхоКГ – это исследование сердца ультразвуковым методом через пищевод, при котором датчик сканера вводится через эндоскоп максимально близко к сердцу. Принцип метода состоит в регистрации отражаемых различными отделами органа ультразвуковых волн. Их улавливает датчик, находящийся в пищеводе, передает на анализатор сканера, и после преобразования на дисплее возникает изображение структуры желудочков, предсердий, клапанов, оболочек, сосудов.
Методика высоко информативна и точна, потому что отраженные волны не проходят через ткани грудной клетки, а идут непосредственно от сердца лишь через стенку пищевода к датчику, то есть не происходит их потери.
Что можно выявить?
Чреспищеводная эхокардиография или УЗИ сердца позволяет выявить структурные изменения: патологию клапанов и оболочек, толщину желудочков и предсердий во время систолы и расслабления, наличие рубцов, опухолей, тромбов, сужение или расширение сосудов.
Преимущества и недостатки метода
Пищеводный метод исследования имеет весомые преимущества по сравнению с традиционной чрезгрудной эхокардиограммой. Он располагает гораздо большей разрешающей способностью и более широкими возможностями визуализации структур и тканей, вплоть до их мельчайших элементов.
Единственным недостатком метода является невозможность его применения при различных заболеваниях пищевода – спазме, сужении, дивертикулах, а также аллергия на лидокаин и другие анестетики, применяющиеся при введении эндоскопа.
Основные показания к инвазивной диагностике

В зависимости от методики исследования электрофизиологическая стимуляция сердца требует наличия следующих показаний.
Инвазивный ЭФИ проводится для установления диагноза при подобных сердечных нарушениях:
- мерцательной аритмии и узловой тахикардии, а также иных суправентрикулярных тахикардиях;
- брадиаритмии с приступами МАС;
- любой степени блокады антиовентрикулярной природы;
- пароксизмальной тахикардии желудочков со спонтанной фибрилляцией;
- блокадой Гиса с последующим переходом в блокаду, ведущую к смерти сердца;
- перед проведением операций по установлению кардиостимулятора, при проведении радиочастотной аблации и кардиоверсии.
Читайте также:
- Телемониторирование – инновационная методика холтеровского мониторирования ЭКГ
- Кардиология
- Эхокардиография (УЗИ сердца)
- Пассивная ортостатическая проба (тилт-тест)
- Медикаментозные пробы
- Холтеровское мониторирование
- ЭКГ
- Жизнеопасные желудочковые аритмии, внезапная сердечная смерть
- Обмороки и предобморочные состояния
- Пароксизмальная тахикардия
- Фибрилляция предсердий (мерцательная аритмия)
- Перебои в работе сердца
- Прейскурант. Кардиология/Аритмология
- Кардиология/Аритмология
- Аритмология
Основные показания к неинвазивной стимуляции
Для проведения чреспищеводной стимуляции обязательно требуется наличие ряда следующих показаний:
- Частое замедление частоты сердечного пульса.
- Наджелудочковая тахикардия пароксизмальной природы.
- Одновременный синдром брадикардии и тахикардии.
- Решение вопроса о последующей установке кардиостимулятора в случаях, когда лечение медикаментозными препаратами не принесло успеха.
- Оценка эффективности антиаритмической терапии, которой подвергается больной.
Радиочастотная абляция
Для решения проблем с тахикардией, которая проявляется в ускоренном сердцебиении, используется ЭФИ РЧА сердца. Чаще всего это называется прижиганием, поскольку в данном случае полностью уничтожается небольшой участок сердца, в котором формируется патология частотного возбуждения. Тем, кто интересуется, как делается ЭФИ РЧА сердца, следует знать о воздействии на ткань радиочастотных сигналов, которые имеют эффект повреждения. Это препятствует появлению иных путей пульса. Но при этом не вредит нормальному сердцебиению, поэтому сердце продолжает функционировать в естественном состоянии.
Сколько стоит процедура
Электрофизиологическое исследование сердца можно проводить только в крупных специализированных центрах, которые имеют необходимое медицинское оборудование и квалифицированных специалистов. Эти манипуляции чаще всего проводятся совершенно бесплатно по квоте Минздрава. Но нужно будет иногда довольно долго стоять в очереди. Ожидание может затянуться на несколько месяцев. Для тех, кто не хочет слишком долго ждать и может самостоятельно оплатить эту процедуру, существуют платные услуги. Цены на ЭФИ сегодня разнятся довольно сильно. Например, ЧПЭФИ могут стоить от 2000 до 4000 рублей. ЭндоЭФИ стоит гораздо дороже – от 60 до 180 тысяч. Здесь учитываются стоимость зонда и катетера. Кроме того, нужно будет оплатить и пребывание в специализированной клинике, что тоже недёшево.
Ряд противопоказаний
Несмотря на эффективность процедуры существует ряд противопоказаний, при наличии которых ни в коем случае нельзя проводить ЭФИ. В настоящее время к ним причисляются проблемы с внутренними органами, главным образом сердечно-сосудистые:
- длительная стенокардия на протяжении минимум месяца;
- острый инфаркт миокарда;
- аневризма в сердце или аорте;
- сердечные пороки с наличием сердечной недостаточности;
- тромбоэмболия;
- инсульт — геморрагический или ишемический;
- повышенная температура тела;
- нарушения кровообращения вместе с кардиомиопатией;
- воспаления пищеварительной системы;
- опухоли и стриктуры пищевода.
Проводящая система сердца
В общих чертах проводящая система сердца (система, ответственная за проведение электрических импульсов в сердце) устроена следующим образом. Импульсы генерируются синусовым узлом, расположенным в правом предсердии. По внутрипредсердным путям проведения эти импульсы достигают атриовентрикулярного (АВ) узла, где происходит некоторая задержка импульсов: предсердия и желудочки должны сокращаться неодновременно. Затем импульс идет по ножкам пучка Гиса к клеткам (кардиомиоцитам) желудочков. Пучок Гиса состоит из двух ножек — правой и левой. Левая ножка пучка Гиса состоит из двух ветвей — передней и задней.
Предварительная подготовка

Назначение процедуры начинается с обязательного изучения истории болезни. Вся процедура обговаривается с пациентом, поскольку обязательно требуется наличие подписанного согласия. В зависимости от типа процедуры она проводится в стационарных или амбулаторных условиях.
При проведении ее амбулаторно больной обязан прибыть в клинику непосредственно за несколько часов до самой процедуры, поскольку часто требуется провести предварительный анализ крови. Врач в обязательном порядке обязан ознакомить больного с планом питания, однако лучше всего не пить и ничего не есть как минимум за 8 часов до самой процедуры, хотя этот промежуток может быть и дольше.
Также может понадобиться принять ряд лекарственных средств — они назначаются исключительно врачом и предназначаются для сужения сосудов и нормализации сердечного ритма. Может понадобиться прекратить прием некоторых медикаментов за несколько дней до процедуры, поэтому предварительно следует рассказать врачу обо всех препаратах, которые больной принимает для избегания осложнений.
После этого перед процедурой обязательно ставится капельница для седатации и обезболивания. Часто она остается на весь промежуток операции и даже после самого исследования.
Возможности ЭФИ и подготовка к исследованию
С целью диагностики ЭФИ выполняется для таких целей:
- измерения внутриполостного кардиального давления;
- определения сердечного выброса;
- выявления органного, функционального кардиального поражения;
- взятия биопсии;
- диагностики пороков;
- выполнения ангиографии коронарных сосудов при ИБС.
Лечебные возможности подразумевают:
- дилатацию сосудов при стенокардии;
- точную доставку лекарственных средств, растворяющих тромб;
- лечение некоторых пороков.
Пациент приходит на ЭФИ из кардиологического отделения, где проводится лечение аритмий и другой патологии.
Независимо от вида исследования, процедура должна проводиться натощак, желательно утром. Кроме того, накануне пациенту не рекомендуется злоупотреблять сигаретами, кофе, алкогольными напитками, стимулирующими тахикардию; следует также отменить лекарства, оказывающие влияние на сердечно-сосудистую систему.
Перед тем как выполнять ЭФИ, следует провести стандартные методы исследования, например, ЭКГ, суточное мониторирование, УЗИ и нагрузочные пробы.
Помимо этого, пациенту может потребоваться консультация невролога, эндокринолога, кардиохирурга и сосудистого хирурга.
Особенности проведения ЭФИ

Согласно отзывам, ЭФИ сердца не является приятной процедурой, но нельзя отрицать, что она позволяет эффективно диагностировать имеющиеся проблемы с нарушениями сердечного ритма.
Для осуществления процедуры инвазивной ЭФИ врач вставляет в кровеносный сосуд, обычно им выступает бедренная вена, тончайшую трубку, называемую катетером. Этот сосуд обязательно должен двигаться к сердечной мышце. Находящийся на катетере электрод периодически позволяет посылать сигналы, но при этом и осуществлять запись собственной электрической активности сердца. Обычно проводится процедура под седацией (легким наркозом), или когда пациент находится в сознании.
Для проведения процедуры требуются условия стационара, поэтому больной ложится в больницу минимум на 2 дня. Сама процедура стандартно не занимает более 45 минут.
Неинвазивное исследование проводится иным методом, поскольку не требуется доступа к сосудам. Сама процедура очень неприятна, поэтому о появившихся неудобствах следует немедленно уведомить врача. Для получения результата предварительно записывается нормальная электрокардиограмма, а затем в рот или нос вставляется зонд с электродом, который постепенно вводится в пищевод. Его останавливают поблизости от сердца, а затем сравнивают полученные результаты.
Подобное ЭФИ может продлиться от часа до четырех часов. Оно может сопровождаться болями в груди или рвотным рефлексом, что сильно осложняет проведение исследования.
Техника выполнения неинвазивной и инвазивной методики
Неинвазивное чреспищеводное ЭФИ проводится в кабинете функциональной диагностики. Перед процедурой врач разъясняет пациенту, каким образом будет проводиться исследование. Затем больного укладывают на кушетку.
Через нос вводится специальный зонд с маленьким электродом, благодаря которому осуществляется электростимуляция левого предсердия. После введения зонда на определенную глубину следует стимуляция, регистрация электрограммы, затем зонд извлекается.
Благодаря анализу электрограммы компьютерной программой выявляются аномалии ритма. Далее врач на основании результатов всех обследований определяет лечебную тактику.
Стимулированная тахиаритмия купируется самостоятельно или медикаментозно. Длительность процедуры составляет около получаса, в течение которых вероятно жжение за грудиной.
Инвазивная процедура проводится в кабинете для рентгенхирургических исследований, выполняется исключительно врачом с опытом проведения подобных методик. Предварительно осуществляется премедикация путем внутривенного введения лекарственных средств: седативных и анальгетиков, что способствует уменьшению страха человека.
Расположив пациента на операционном столе, следует измерить артериальное давление и провести ЭКГ. Процедура начинается местным обезболиванием требуемой области, пункцией бедренной, подключичной вены.
Далее по специальному проводнику проводится внутривенный катетер (под рентгенконтролем) в сердечную полость. На кончике его располагается несколько небольших электродов, с помощью которых выполняется стимуляция сердца и запись электрограммы.
Полтора часа длится процедура, после чего программа анализирует результаты и делает выводы. Если решается вопрос о выполнении абляции, процедура пролонгируется.
После окончания катетер извлекается, а на область пунктируемого кровеносного сосуда накладывается давящая повязка, с помощью которой останавливается кровоточивость. Пациент должен находиться под врачебным контролем в течение суток после процедуры.
Побочные эффекты
Во время проведения операции часто проявляются хоть и не опасные, но неприятные побочные эффекты. К ним относятся:
- Сердечная аритмия, которая часто приводит к сильному головокружению и даже обморокам. Это считается вполне нормальной ситуацией, поэтому врач не прерывает ЭФИ сердца, а просто отправляет небольшой электрический разряд для последующего восстановления сердечного ритма.
- Кровяные сгустки на конце вводимого катетера. Временами они могут отрываться, а потому блокировать другие кровеносные сосуды. Для избегания подобных ситуаций во время ЭФИ вводятся препараты для разжижения крови на основе гепарина.
- В областях, куда непосредственно вводится катетер, могут начать появляться кровоподтеки или кровотечения. Также имеется возможность подхватить инфекцию, поэтому следует внимательно прислушиваться к советам врачей.
Отзывы пациентов и врачей
Чреспищеводные методы исследования, судя по отзывам врачей – специалистов в области кардиологии и кардиохирургии, дают очень ценную и важную информацию, позволяют провести точную диагностику и выбрать наиболее подходящий метод лечения, в том числе хирургический.
Что касается пациентов, проходивших исследование, то в отзывах на форумах больше фигурируют такие фразы, как «ничего страшного», «совсем не больно», «очень быстрая процедура», «езжу в клинику на ЧПЭФИ каждый год, проводят профессионально».
Исследование сердца чреспищеводными методами – это необходимость, которой нельзя пренебрегать. Они располагают большими диагностическими возможностями, на которых базируется наиболее эффективное лечение.
Последствия ЭФИ

После непосредственного окончания процедуры больной должен отдыхать в лежачем положении еще от часа до трех часов. Во время этого промежутка отдыха следует соблюдать следующие рекомендации: ни в коем случае не двигаться, пока не разрешит медсестра. Использованную в процедуре конечность следует держать в расслабленном состоянии.
Некоторое время после процедуры за состоянием пациента обязательно следит медсестра, чтобы сразу же выявить появившееся кровотечение или припухлости. После того, как пациент отойдет от наркоза, врач разъясняет результаты полученного исследования, а затем отпускает домой или через день.
Перед выпиской врач также обязательно дает инструкцию по дальнейшему лечению, которую необходимо исполнять. Прием пищи и лекарств обычно разрешается уже через 4 часа после диагностики. К нормальной жизни человек может вернуться уже спустя сутки. В течение нескольких дней место прокола будет неприятно болеть, может появиться синяк или кровоподтек — это вполне нормальное явление.
Как подготовиться к процедуре?
Подготовиться к проведению исследования пациенту необходимо следующим образом:
- Перестать принимать назначенные антиаритмические препараты не позднее, чем за неделю до исследования, но только по согласованию с направившим на ЧПЭФИ врачом,
- Из назначенных препаратов допустимо использование только нитроглицерина короткого действия под язык при приступах стенокардии,
- За несколько недель или дней до обследования выполнить ЭКГ, УЗИ сердца и суточное мониторирование АД и ЭКГ,
- В течение недели до процедуры желательно не курить и не употреблять алкоголь,
- Накануне исследования разрешается легкий ужин, желательно исключить кофе,
- В день исследования пациент должен явиться на процедуру полностью натощак, исключается даже прием воды.
Возможные осложнения
В некоторых ситуациях обязательно следует вызвать скорую помощь:
- сильное и внезапное усиление припухлости в месте прокола;
- невозможность остановить кровотечение, несмотря на все рекомендации;
- онемение или покалывание конечности, через которую врач проводил исследование;
- рука или нога начинают менять цвет или ощущать холод;
- синяк или кровоподтек начинает становиться больше, распространяясь по разным сторонам;
- на месте прокола имеются выделения, или он отекает.
На самом деле, ЭФИ считается процедурой с малой степенью риска, поэтому осложнения бывают крайне редки. Правильно проведенная процедура с дезинфекцией и всеми аппаратами не приводит к осложнениям, зато позволяет точно установить диагноз. Неприятные ощущения, возникающие при процедуре, перетерпеть вполне возможно, но все же обо всех изменениях необходимо уведомлять врача.
Источник: xn—-jtbnfnblbkihf4j.xn--p1ai

