Существуют два основных варианта изменения морфологии лейкоцитов, которые не следует путать, – это дегенеративные и токсические изменения. К дегенеративным изменениям морфологии нейтрофилов относят изменения, происходящие с клетками непосредственно в кровеносном русле (после их созревания). Они включают в себя ядерные изменения (гиперсегментацию, полиплоидию, фрагментацию и пикноз), цитоплазматические изменения и повреждение клеточной стенки. Подобные изменения морфологии нейтрофилов мы можем часто встречать в длительно хранившихся образцах крови (как правило, более суток). Они связаны с запрограммированной гибелью клеток – апоптозом. Существуют также дегенеративные изменения, происходящие под воздействием токсинов (кариорексис, кариолизис и потеря клеточной мембраны). Более подробно в данной статье будет описана нейтрофильная токсичность, ее варианты и диагностическое значение. Нейтрофильная токсичность Токсические изменения морфологии нейтрофилов возникают в костном мозге в результате их усиленного производства и сокращения времени созревания.
йтрофильная токсичность не отражает в буквальном смысле «токсический эффект» бактерий на нейтрофил, находящийся в кровеносном русле.Впервые токсические изменения морфологии нейтрофилов были описаны в медицине у пациентов с грамотрицательным сепсисом и интоксикацией в результате воздействия эндотоксинов, в связи с чем долгое время считалось, что нейтрофильная токсичность связана исключительно с токсикозом. Действительно, основная причина появления нейтрофильной токсичности – это системные токсикозы, вызванные инфекционными заболеваниями, но существуют и неинфекционные причины. У животных, имеющих заболевания костного мозга или получающих гемопоэтические цитокины (например, гранулоцитарный колониестимулирующий фактор или G-CSF), также может возникнуть нейтрофильная токсичность.
Большинство токсических изменений отражает асинхронность созревания между ядром и цитоплазмой. Во время нормального гранулоцитопоэза удлинение и пикноз ядра происходят одновременно с конденсированием хроматина и исчезновением цитоплазматических белков (РНК – в виде рибосом и шероховатой эндоплазматической сети, которые придают синий цвет цитоплазме). В результате ускоренного созревания в периферическую кровь попадают незрелые клетки. Они могут быть более крупными (гигантизм), с остатками шероховатой эндоплазматической сети, рибосомами, менее конденсированным хроматином. Эти клетки также могут иметь пенистую или вакуолизированную цитоплазму.
Основные причины появления нейтрофильной токсичности:
– Тяжелые бактериальные инфекции (пиоторакс у кошек, пиометра, тяжелый простатит у собак, септические артриты и т. д.);
– Тяжелые вирусные инфекции (парвовирусный и коронавирусный энтерит собак, панлейкопения кошек, инфекционный перитонит кошек, чума плотоядных и т. д.);
– Иммунная гемолитическая анемия (IHA);
– Острый панкреатит; – некроз тканей;
– Тяжелые отравления (цинк, свинец и т.д .);
– Химиотерапия.
Нейтрофильная токсичность встречается как у палочкоядерных, так и у сегментоядерных нейтрофилов. Нейтрофильную токсичность в мазке крови оценивают субъективно и полуколичественно. Различают легкую, умеренную и выраженную нейтрофильную токсичность.
<10% измененных клеток – легкая нейтрофильная токсичность;
10-30% измененных клеток – умеренная нейтрофильная токсичность;
>30% измененных клеток – выраженная нейтрофильная токсичность.
Далее каждый вид нейтрофильной токсичности оценивается в баллах или «+».
Различают 5 основных видов нейтрофильной токсичности:
Тельца Деле являются, как правило, самым ранним индикатором токсических изменений в клетке. Они представляют собой цитоплазматические включения серо-голубого цвета округлой или овальной формы. Их количество в цитоплазме нейтрофилов может варьироваться от одного до четырех и более. Тельца Деле представляют собой остатки шероховатой эндоплазматической сети. У кошек наличие небольшого количества телец Деле в цитоплазме нейтрофилов рассматривается как вариант нормы.
Возможно появление телец
Деле в цитоплазме нейтрофилов при длительном хранении образца крови (более суток). Следовательно, их появление следует интерпретировать с осторожностью. Наличие 1-2 телец Деле в цитоплазме нейтрофилов оценивается как легкая нейтрофильная токсичность, 3-4 – как умеренная, более 4 – как выраженная.
В отличие от бело-розовой цитоплазмы «здорового» нейтрофила, у токсически измененной клетки цвет цитоплазмы будет варьироваться от серо-голубого до темно- синего. Подобное диффузное неравномерное окрашивание цитоплазмы нейтрофилов связано с наличием рибосом и остатков шероховатой эндоплазматической сети. Изменение цвета цитоплазмы от неоднородно серого до светло-голубого оценивается как легкая нейтрофильная токсичность, окрашивание цитоплазмы в равномерно голубой цвет – как умеренная, от синего до темно-синего – как выраженная.
Пенистый вид цитоплазме придают вакуоли, которые образуются в результате дегрануляции лизосом. Потеря четкости структур в цитоплазме клеток расценивается как легкая нейтрофильная токсичность, наличие небольшого количества вакуолей в цитоплазме – как умеренная, интенсивная вакуолизация цитоплазмы с появлением серой сетки – как выраженная. Хорошо заметные точечные вакуоли в цитоплазме, как правило, не относятся ктоксическим изменениям и часто являются артефактом, возникающим в результате длительного хранения образца крови (более 4 часов с момента отбора).
Ядерный хроматин у таких клеток более рыхлый, тонкий, менее конденсированный. Могут встречаться клетки, значительно превосходящие в размере нейтрофилы здоровых животных (гигантские нейтрофилы). Гигантские нейтрофилы возникают в результате пропуска одного из клеточных делений в костном мозге. Эти клетки могут иметь как нормальную морфологию ядра, так и гипосегментированные ядра. Появление подобных клеток мы можем часто наблюдать в крови у кошек, реже – у собак. Гигантские нейтрофилы всегда свидетельствуют о выраженной нейтрофильной токсичности. Появление гигантских нейтрофилов в крови характерно для тяжелых воспалительных процессов или дисгранулопоэза.
Основные причины появления гигантских нейтрофилов в крови кошек:
1. тяжелые бактериальные инфекции (пиоторакс, пиометра и т. д.);
2. острая миелоидная лейкемия (ОМЛ);
3. миелодиспластический синдром;
4. вирусная лейкемия кошек (FeLV);
5. вирус иммунодефицита кошек (FIV);
6. панлейкопения (в результате временной гранулоцитарной гипоплазии).
Под токсической зернистостью принято понимать появление мелких красных зерен (гранул) в цитоплазме нейтрофилов. Данный вид нейтрофильной токсичности характерен для лошадей, коров, лам, верблюдов, он редко встречается у собак и кошек.
и зерна представляют собой первичные гранулы, сохранившие способность окрашиваться с той же интенсивностью, как это в норме свойственно гранулам промиелоцитов. Токсическую зернистость следует дифференцировать от гранул, содержащихся в цитоплазме нейтрофилов животных с лизосомными болезнями накопления. Ее следует отличать от розовой окраски вторичных гранул, которая не является признаком токсичности. Следует также помнить, что у кроликов, морских свинок, птиц и рептилий вторичные гранулы нейтрофилов окрашиваются в красный цвет (гетерофилы). Токсическая зернистость всегда свидетельствует о выраженной нейтрофильной токсичности.
Степени тяжести нейтрофильной токсичности:
Тельца Деле+
Базофилия цитоплазмы+
Пенистость цитоплазмы++
Темная серо-синяя пенистая цитоплазма+++
Токсическая зернистость+++
Следует помнить, что общеклинический анализ крови (ОАК) должен обязательно включать в себя подсчет лейкограммы вручную и оценку морфологии лейкоцитов. Врач-лаборант всегда должен указывать любой вид нейтрофильной токсичности в бланке результата ОАК. Автоматический подсчет лейкограммы очень сомнителен и не способен оценить изменения морфологии нейтрофилов. Для исследования морфологии нейтрофилов не рекомендуется использовать быстрые красители (например, лейкодиф). Оптимальной окраской считается окраска по Романовскому или Паппенгейму. Токсические изменения часто указывают на тяжелый воспалительный процесс и сопровождаются выраженным нейтрофильным лейкоцитозом со сдвигом ядра влево и появлением незрелых клеток (промиелоцитов, миелоцитов и метамиелоцитов), что является плохим прогностическим признаком.
циентам с подобной картиной крови необходимы ежедневные исследования общеклинического анализа крови для оценки реакции на проводимое лечение. Важно помнить, что некоторые животные могут иметь сдвиг влево без нейтрофильной токсичности и токсические изменения без сдвига влево (редко). В последнем случае врач- клиницист должен искать другие причины появления токсичности (например, миелодисплазии, длительное хранение образца крови и т. д.). Появлению нейтрофильной токсичности способствуют инфекционные процессы, опухолевые, метаболические. В случае нейтрофилии со сдвигом ядра вправо, нейтропении или при отсутствии изменений в лейкограмме оценка морфологии нейтрофилов может оказатьдополнительную помощь врачу-клиницисту в постановке диагноза.
Список используемой литературы:
- Atlas of Veterinary Hematology. Blood and Bone Marrow of Domestic Animals. John W. Harvey, 2001.
- Diagnostic Cytology and Hematology of the dog and cat. Third Edition. Rick L. Cowell, Ronald D. Tyler, James H. Meinkoth, Dennis B. Denicola.
- Laboratory Urinalysis and Hematology for the Small Animal Practitioner. Carolyn A. Sink, Bernard F. Feldman, 2004.
- Hemogram Interpretation for Dogs and Cats. Ralston Purina Company Clinical Handbook series.
- Israel Journal Veterinary Medicine. Abstracts of papers presented at the 29 th annual Israel veterinary symposium february 2005. Clinical aspects of neutrophil cytoplasmic toxicity in dogs and cats.
- Veterinary Medicine. Evaluating blood films. Take 3 minutes to bring abnormalities to light. December, 2004.
- Ветеринарная лабораторная медицина. Интерпретация и диагностика. Денни Мейер, Джон Харви, Москва, Софион, 2007.
Источник: www.spbvet.info
Токсическая (токсогенная) зернистость нейтрофилов
Токсическая (токсогенная) зернистость нейтрофилов — грубая зернистость, сходная с азурофильными гранулами. Образование ее происходит внутри клетки в результате физико-химических изменений белковой структуры цитоплазмы под влиянием продуктов интоксикации. Наблюдается при инфекционных или воспалительных процессах. Может сопровождаться присутствием цитоплазматических вакуолей и телец Деле.
Токсическая зернистость нейтрофилов нередко появляется раньше ядерного сдвига. Ее нарастание при гнойно-септических заболеваниях, крупозной пневмонии и ряде воспалительных заболеваний указывает на прогрессирование патологического процесса и возможность неблагоприятного исхода. В большом количестве токсическая зернистость нейтрофилов появляется при распаде опухолевой ткани под влиянием лучевой терапии. Наиболее выражена токсическая зернистость при крупозной пневмонии в период рассасывания воспалительного инфильтрата, при скарлатине, септикопиемии, перитоните, флегмоне и прочих гнойных процессах. Особенно важное значение имеет она в диагностике острого живота (например, гангренозного аппендицита, протекающего с незначительно повышенной температурой тела и, нередко, при отсутствии лейкоцитоза).
Токсическую зернистость нейтрофилов можно обнаружить при окраске мазков обычным способом. Однако, даже при качественной окраске, пылевидная токсогенная зернистость может быть не видна, а при перекрашивании мазка (даже незначительном) за токсогенную можно принять специфическую зернистость нейтрофильных гранулоцитов. Поэтому для выявления токсической зернистости нейтрофилов предложены специальные методы окраски, из которых наиболее распространенным и доступным является метод Фрейфельд
Метод Фрейфельд
Для окраски мазка используют следующие красители:
- 1 г основного фуксина растворяют при слабом нагревании в 15 г этилового спирта (96
Источник: www.clinlab.info
Токсогенная зернистость нейтрофилов (ТЗН) [ править | править код ]
Качественное изменение лейкоцитов, представляет собой темные крупные грубые гранулы внутри лейкоцита, образующиеся в результате физико-химических изменений белковой структуры жидкой части цитоплазмы — коагуляции белка под влиянием продуктов интоксикации и агломерации белка, вокруг обычных нейтрофильных зерен. Белок как бы сваривается в процессе воспаления.
Значение в клинике [ править | править код ]
ТЗН характерна для интоксикаций организма при гнойных процессах, воспалительных процессов кокковой этиологии, распаде опухолевой ткани, действии ионизирующей радиации, а также для дегенеративных изменений в костном мозге вследствие предшествующей продолжительной избыточной стимуляции гранулопоэза или при первичном угнетении гранулопоэза, без предшествующей стимуляции. Но отсутствует при туберкулезе (используется для его исключения при дифференциальной диагностике с пневмонией другого происхождения), столбняке, энцефалите, тифах.
Тельца Князькова-Деле [ править | править код ]
Крупные бледно-голубые комочки различной формы в цитоплазме нейтрофилов, представляющие собой РНК и фрагменты шероховатого эндоплазматического ретикулума. Наблюдаются при скарлатине, сепсисе, кори, пневмонии, ожогах и т. д. Полагают что они имеют то же происхождение, что и ТЗН и встречаются, когда ТЗН не вполне выражена или совсем отсутствует.
Зерна Амато [ править | править код ]
Небольшие округлые овальные или типа запятой образования красящиеся в бледно-голубой цвет; в них наблюдаются красные или красно-фиолетовые зерна. Описаны зерна Амато при скарлатине, но встречаются и при других инфекциях. Близки к тельцам Деле.
Вакуолизация цитоплазмы [ править | править код ]
Наблюдается реже, чем ТЗН, но имеет не меньшее, диагностическое значение, указывая на тяжесть заболевания и интоксикации. Наиболее характерна для тяжелейших форм сепсиса, абсцессов, острой дистрофии печени. Иногда наблюдается почти тотальная вакуолизация всех лейкоцитов: «дырявые», «простреленные» лейкоциты. Возникает в результате растворения капелек жира в жироперерожденной клетке (жировая дистрофия) при фиксации спиртом, то есть в прогностическом отношении более грозный симптом чем ТЗН, так как ТЗН свидетельствует о белковой дегенерации клеток, а вакуолизация о глубокой форме клеточной дистрофии.
Вакуолизация цитоплазмы выявляется реже, чем токсогенная зернистость, но имеет не меньшее диагностическое значение. Эти изменения лейкоцитов можно выявить при сепсисе (особенно вызванном анаэробной инфекцией), абсцессах, острой дистрофии печени.
Тельца Князькова—Деле — крупные бело-голубые участки цитоплазмы различной формы, свободные от специфических гранул. Эти изменения лейкоцитов можно обнаружить при воспалительных заболеваниях, инфекциях (корь, скарлатина), сепсисе, ожогах.
Гиперсегментация ядер пейтрофилов — наличие 5 сегментов и более в ядрах нейтрофи-лов. Эти изменения лейкоцитов наблюдаются при наследственной конституциональной особенности, дефиците витамина В12 и фолиевой кислоты. Врожденная гиперсегментация не дает никаких клинических симптомов.
Пельгеровская аномалия — доминантно наследуемое нарушение созревания гранулоци-тов, характеризующееся уменьшением сегментации ядер нейтрофилов. Наиболее часто зрелые нейтрофилы содержат двухсегментное или несегментное ядро, редко — трехсегментное. По своим физиологическим свойствам такие клетки не отличаются от нормальных, зрелых нейтрофилов.
Псевдопельгеровская аномалия — уменьшение сегментации ядер гранулоцитов — изменения лейкоцитов можно выявить при миелопролиферативных заболеваниях, агранулопито-зе, множественной миеломе. туберкулезе. Они имеют временный, преходящий характер. По выздоровлении больного псевдопельгеровские лейкоциты исчезают. В основе аномалии созревания ядер лежит нарушение метаболизма нуклеиновых кислот.
Клетки лейколиза (тени Боткина—Гумпрехта) — полуразрушенные ядра лимфоцитов с остатками ядрышек — обнаруживают при хроническом лимфолейкозе.
Скорость оседания эритроцитов (СОЭ)
Скорость оседания эритроцитов в плазме прямо пропорциональна массе эритроцитов, разнице в плотности эритроцитов и плазмы и обратно пропорциональна вязкости плазмы. Показатели СОЭ в норме приведены в табл. 1.29. Образование монетных столбиков и агглютинация эритроцитов, увеличивая массу оседающих частиц, ускоряют оседание. Основным фактором, влияющим на образование монетных столбиков из эритроцитов, является белковый состав плазмы крови. Все белковые молекулы снижают дзета-потенциал эритроцитов (отрицательный заряд, способствующий взаимному отталкиванию эритроцитов и поддержанию их во взвешенном состоянии), но наибольшее влияние оказывают асимметричные молекулы — фибриноген, иммуноглобулины, а также гаптоглобин. Особенно выраженное ускорение СОЭ (60—80 мм/ч) характерно для парапротеинемических гемобластозов (миелом-ная болезнь, болезнь Вальденстрема). На дзета-потенциал эритроцитов влияют и другие факторы: рН плазмы (ацидоз снижает СОЭ, алкалоз повышает), ионный заряд плазмы, ли-пиды, вязкость крови, наличие антиэритроцитарных антител. Число, форма и размер эритроцитов также влияют на оседание. Эритропения ускоряет оседание, однако при выраженной серповидности, сфероцитозе, анизоцитозе СОЭ может быть низкой, так как форма клеток препятствует образованию монетных столбиков.
Читайте также:
- XVIII. ПАТОФИЗИОЛОГИЯ ЛЕЙКОЦИТОВ
- Адгезия лейкоцитов к эндотелию сосудов обнаруживается
- Анализ теории раннего сексуального соблазнения. Раннее соблазнение и психопатология.
- ВИДЫ ЛЕЙКОЦИТОЗОВ ПО ПРЕОБЛАДАНИЮ ОТДЕЛЬНЫХ ФОРМ ЛЕЙКОЦИТОВ
- Диагноз с точки зрения объектных отношений: пограничная психопатология
- Индукция липоксигеназы лейкоцитов
- Метапатология
- Морфологические аномалии лейкоцитов
- НАСЛЕДСТВЕННОСТЬ И ПАТОЛОГИЯ. ЭТИОЛОГИЯ И ПАТОГЕНЕЗ НАСЛЕДСТВЕННЫХ БОЛЕЗНЕЙ
- Невропатология
- Некоронарогенная патология сердечной мышцы неревматической этиологии
- Норма и патология проявления воли
Все лейкоциты делятся на гранулоциты (нейтрофил, эозинофил, базофил) и агранулоциты (лимфоцит, моноцит).
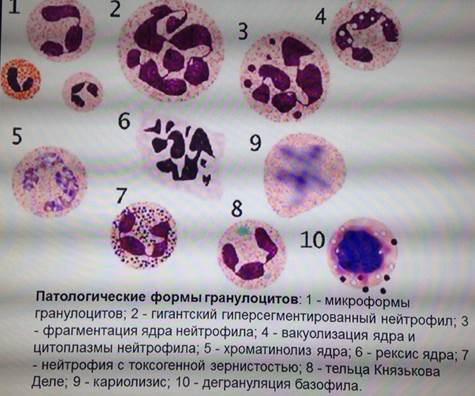
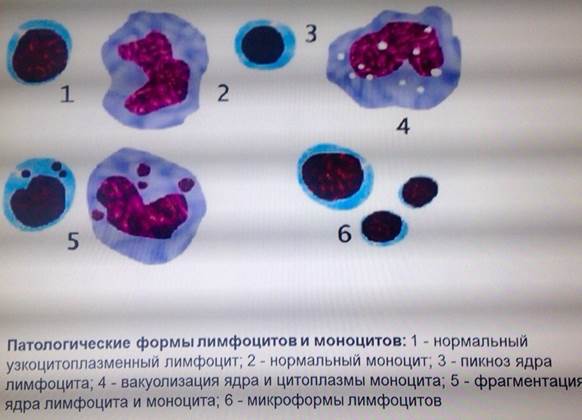
Патологические формы лейкоцитов: регенераторные и дегенеративные.
Регенераторные формы в норме они находятся только в костном мозге. К ним относятся миелоциты и метамиелоциты. Дегенеративные формы – деструктивно-измененные формы при такой патологии, как лейкозы, хронические инфекционные заболевания, где юные лейкоциты находятся в периферической крови; они выявляются по окраске и включениям в цитоплазме. Признаки дегенерации:
— Токсогенная зернистость в цитоплазме нейтрофилов
— Вакуолизация цитоплазмы, ядра
— Пикноз и рексис ядра
Эта патология связана с интоксикацией организма, в результате жировой дистрофии, в результате, абсцессов, тяжелых сепсисов, лучевой болезни и при некоторых формах лейкоза.
Лейкоцитарная формула. Обратите внимание на видовые особенности: у КРС высокий уровень лимфоцитов, у птиц псевдоэозинофилы являются аналогом нейтрофилов млекопитающих.
Вид жив-х Гранулоциты Агранулоциты Базо-филы Эозино-филы Нейтрофилы (гетерофилы) Лимфо-циты Моно-циты Миело-циты Юные Палочко-ядерные Сегменто-ядерные Человек 0-1 3-5 1-6 47-72 19-37 3-11 КРС 0-2 5-8 0-1 2-5 20-35 40-65 2-7 Овца 0-1 4-12 0-2 3-6 35-45 40-50 2-5 Свинья 0-1 1-4 0-2 2-4 40-48 40-50 2-6 Лошадь 0-1 2-6 0-5 3-6 45-62 25-44 2-4 Курица 1-3 6-10 Псевдоэозинофилы 52-60 4-10 24-30 Изменение количественного состава лейкоцитов – ЛЕЙКОЦИТОЗ. Лейкоцитозы – нейтрофильный, эозинофильный, базофильный, а также лимфоцитоз и моноцитоз.
Нейтрофильный лейкоцитоз (нейтрофилия) наблюдается при острых инфекционных заболеваниях, гнойных воспалительных процессах, инфаркте миокарда, укусах ядовитых насекомых, после острой кровопотери. Практическое значение имеет определение степени ядерного сдвига в лейкоцитарной формуле.
Индекс ядерного сдвига – отношение всех несегментоядерных нейтрофилов в % к процентному содержанию сегментоядерных клеток. 6 признаков:
1)Без ядерного сдвига – увеличение количества зрелых нейтрофилов на фоне общего лейкоцитоза
2)С гипорегенеративным ядерным сдвигом влево – увеличение содержания палочкоядерных форм нейтрофилов на фоне нейтрофилии. Сдвиг характерен для течения ряда инфекционных заболеваний и воспалений.
3)С регенеративным ядерным сдвигом вправо – на фоне нейтрофилии и увеличенного содержания палочкоядерных форм обнаруживаются метамиелоциты. Такой сдвиг характерен для гнойно-септических процессов.
4)С гиперрегенеративным ядерным сдвигом влево – характеризуется появлением молодых форм лейкоцитов – миелоцитов, промиелоцитов, миелобластов. Эта картина – тревожный показатель неблагополучного течения инфекционных и гнойно-септических заболеваний.
5)С дегенеративным ядерным сдвигом – характеризуется повышением содержания палочкоядерных нейтрофилов с появлением значительного числа диструктивно измененных сегментоядерных форм. При этом наблюдается пикноз ядра, токсигенная зернистость, вакуолизация цитоплазмы. Это показатель угнетенности красного костного мозга. Встречается при тяжелой интоксикации и тяжелых формах инфекционных заболеваний.
6)С ядерным сдвигом вправо – характеризуется появлением в гемограмме гиперсегментированных (более 5 сегментов) нейтрофилов. Наблюдается при лучевой болезни и у здоровых животных.
Эозинофилия – увеличение содержания эозинофилов, является своеобразной реакцией организма на поступление в него чужеродных белков и гистаминов. Связана с антитоксической и фагоцитарной функцией эозинофилов. Развитие эозинофилии происходит при аллергической реакции, синдромах паразитарных, кожных болезней, гельминтозах, при туберкулезе, при беспорядочном принятии лекарственных веществ и антибиотиков, у человека – при венерических заболеваниях.
Базофильный лейкоцитоз (базофилия) – очень редкая форма лейкоцитозов, встречается при гемолитических анемиях, при вакцинациях и введении в организм чужеродного белка.
Лимфоцитоз – увеличение лимфоцитов в условиях патологии при ряде инфекционных заболеваний (бруцеллез), при алиментарной дистрофии, бронхиальной астме, эндокринных расстройствах.
Моноцитоз является показателем развития в организме иммунных процессов при таких инфекционных, вирусных болезнях, как (оспа, корь, краснуха).
Лейкопения – уменьшение общего количества лейкоцитов. Число лейкоцитов сильно связано с уменьшением общего числа нейтрофилов и наблюдается при пневмонии, сепсисе, лимфогранулематозе.
ЛЕЙКОЗЫ (гемобластозы) – группа опухолей, развивающихся в результате злокачественной трансформации гемопоэтических клеток в красном костном мозге и лимфоидной ткани, где они угнетают нормальный гемопоэз и иммунитет. Лейкозированные клетки поступают в кровь и инфильтрируют в органы и ткани. Чтобы животное заболело лейкозом, достаточно чтобы одна кроветворная клетка мутировала в раковую. Мутации возникают в результате действия вирусов (вирусная этиология – птица, грызуны, кошки, КРС), химических, физических факторов, воздействия ионизации.
Теории возникновения лейкозов
Условия, при которых лейкоз может развиваться: 1) наследственная предрасположенность; 2) активное действие эндо- и экзогенных факторов; 3) состояние организма, благоприятствующее действию вирусных активаторов.
Патогенный агент, проникнувший в клетку, может оставаться латентным, не провоцируя болезнь, а при действии определенного фактора наступает развитие лейкоза. Любой злокачественный процесс начинается с поражения ДНК или РНК. Так как это генетическая информация, она сразу же дает сигнал остальным клеткам, и они тут же начинают мутировать.
Классификация
Лейкозы бывают острые и хронические.
| следующая лекция ==> О романе Б. Пруса Фараон | ИСКЛЮЧИТЕЛЬНЫЕ ПРАВА. ЛИЧНЫЕ НЕИМУЩЕСТВЕННЫЕ ПРАВА Дата добавления: 2015-06-04 ; Просмотров: 3134 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник: ogomeopatii.ru

