Суть болезни
Миелодиспластические синдромы (МДС) – группа заболеваний, которые характеризуются нарушениями кроветворения миелоидной линии. В результате этих нарушений возможность выработки зрелых клеток крови частично сохраняется, но наблюдается дефицит тех или иных их видов, а сами клетки при этом изменены и плохо функционируют.
У значительной части больных МДС через некоторый промежуток времени, обычно от нескольких месяцев до нескольких лет, развивается острый миелоидный лейкоз.
МДС в обиходе иногда называют «предлейкемией», ранее применялись также термины «малопроцентный лейкоз», «тлеющий лейкоз» или «дремлющий лейкоз». Это связано с содержанием бластных клеток в костном мозге: если их более 20% (согласно классификации Всемирной организации здравоохранения) или более 30% (согласно франко-американо-британской классификации FAB), то речь уже идет о миелоидном лейкозе, если же их уровень ниже порогового значения, то может быть диагностирован МДС.
Под термином «миелодиспластический синдром» в настоящее время подразумевается целая группа заболеваний, различающихся по частоте встречаемости, клиническим проявлениям, а также по вероятности и ожидаемым срокам трансформации в лейкоз. Специалисты используют две классификации МДС: франко-американо-британскую (FAB) и классификацию Всемирной организации здравоохранения (ВОЗ). Рассмотрим классификацию FAB как более простую:
- Рефрактерная анемия (РА). Термин «рефрактерная» здесь означает, что анемия не поддается лечению препаратами железа и витаминами. В костном мозге менее 5% миелобластов, аномалии в основном касаются предшественников эритроцитов.
- Рефрактерная анемия с кольцевыми сидеробластами (РАКС): миелобластов в костном мозге менее 5%, но не менее 15% предшественников эритроцитов представлены особыми аномальными клетками – так называемыми кольцевыми сидеробластами. Это клетки с кольцеобразными «отложениями» железа, которые не могут обеспечивать эффективный транспорт кислорода.
- Рефрактерная анемия с избытком бластов (РАИБ): миелобластов в костном мозге 5–20%. В классификации ВОЗ дополнительно подразделяется на РАИБ-I (5–9% бластов) и РАИБ-II (10-19% бластов).
- Рефрактерная анемия с избытком бластов на стадии трансформации (РАИБ-T): миелобластов 21–30% (по классификации ВОЗ это уже острый миелоидный лейкоз).
- Хронический миеломоноцитарный лейкоз, ХММЛ (по классификации ВОЗ относится к миелодиспластическим-миелопролиферативным заболеваниям).
Частота встречаемости, факторы риска
Общая частота МДС составляет 3-5 случаев на 100 000 населения. Однако у детей и молодых взрослых это заболевание встречается во много раз реже: более 80% случаев МДС фиксируется после 60 лет, причем несколько чаще у мужчин, чем у женщин.
В большинстве случаев МДС возникает без какой-либо известной причины, но иногда его развитие может быть спровоцировано предшествующей химиотерапией или лучевой терапией по поводу какой-либо опухоли — например, лимфогранулематоза или неходжкинской лимфомы. В этих случаях говорят о вторичном МДС.
Частота МДС (как и острого миелоидного лейкоза) повышена у людей с определенными генетическими аномалиями, такими как синдром Дауна, анемия Фанкони, нейрофиброматоз и некоторые другие.
Изучается роль и других факторов в возникновении этого заболевания – например, воздействия некоторых вредных химических веществ. Но у детей и молодых взрослых эти факторы не играют существенной роли.
Признаки и симптомы
Симптомы и степень их выраженности могут различаться в зависимости от разновидности МДС и конкретного случая. Но большинство наблюдаемых проявлений возникает в результате цитопении, то есть дефицита нормальных клеток крови.
Анемия (недостаток эритроцитов, сниженный уровень гемоглобина) характерна для подавляющего большинства случаев МДС; она проявляется бледностью, утомляемостью, плохой переносимостью физических нагрузок; могут также возникнуть одышка, головокружения, боли в груди и т.п.
Примерно у половины больных встречается нейтропения (то есть пониженное содержание зрелых функциональных нейтрофилов) и поэтому снижена сопротивляемость инфекциям; может обнаруживаться стойкое повышение температуры. Нередко наблюдается и тромбоцитопения, то есть недостаточное содержание тромбоцитов, что ведет к возникновению кровотечений, синяков, петехий (мелкоточечных подкожных кровоизлияний). Возможны и другие симптомы.
Впрочем, в некоторых случаях пациенты с МДС долгое время не замечают существенного ухудшения самочувствия, и тогда проблемы обнаруживаются только в ходе обычного медосмотра по отклонениям от нормы в клиническом анализе крови.
Диагностика
Как правило, поводом к медицинскому осмотру служат жалобы на симптомы, связанные с анемией, причем эта анемия не поддается обычному лечению препаратами железа и витаминами. В клиническом анализе крови снижено количество эритроцитов, может быть также снижено количество лейкоцитов (нейтрофилов) и/или тромбоцитов. Характерно, что при уменьшении числа эритроцитов их размеры и цветовой показатель крови могут быть увеличены. Полезен также подсчет числа ретикулоцитов — незрелых эритроцитов, так как он дает информацию об интенсивности образования новых красных клеток крови.
Для точной диагностики и определения конкретной разновидности МДС необходимо детальное исследование образца костного мозга, взятого в ходе трепанобиопсии: анализируются характер расположения различных клеток («архитектоника» костного мозга), число бластных клеток, содержание кольцевых сидеробластов и других аномальных клеток, степень изменений во всех ростках кроветворения – то есть среди предшественников эритроцитов, гранулоцитов и тромбоцитов, изменения стромы – соединительной ткани костного мозга.
явленные нарушения могут быть очень разнообразными.
Так как развитие МДС нередко связано с известными хромосомными аномалиями, определенную роль в диагностике и прогнозе играют цитогенетические исследования.
Лечение
Лечение МДС зависит от его конкретной формы. Так, если речь идет об относительно «доброкачественных» разновидностях МДС с небольшим числом бластных клеток, то больные из групп низкого риска могут длительное время сохранять нормальное качество жизни, просто время от времени получая заместительную терапию компонентами крови – эритроцитами и, возможно, тромбоцитами. При перегрузке железом после множественных переливаний необходима соответствующая терапия (десферал, эксиджад). Иногда для стимуляции кроветворения используют факторы роста. При инфекционных осложнениях требуется антибактериальная и противогрибковая терапия. В ряде случаев применяют и другие лекарственные средства.
Если же речь идет о формах болезни, связанных с более высоким риском, то вопрос о лечении таких пацентов достаточно сложен. Химиотерапия с использованием обычных цитостатиков (цитарабин и т.п.) малоэффективна и не приводит к долговременной ремиссии. Общепринятых стандартов химиотерапии при МДС практически не существует. Разрабатываются новые лекарства; в частности, обнадеживающие результаты показало применение дакогена (децитабина). Иногда может применяться иммуносупрессивная терапия и другие методы.
Единственным методом, позволяющим в случае успеха рассчитывать на полное излечение больных с МДС, является аллогенная трансплантация костного мозга – особенно у молодых пациентов, которые лучше переносят эту процедуру и связанные с ней осложнения. Однако аллогенная трансплантация по поводу МДС, как и по поводу других заболеваний, связана с проблемой поиска совместимого донора и с опасностью жизнеугрожающих осложнений.
При трансформации МДС в острый миелоидный лейкоз проводится химиотерапия этого лейкоза. Однако вторичный лейкоз, развившийся из МДС, обычно плохо поддается терапии. В этой ситуации, как правило, также показано проведение аллогенной трансплантации костного мозга, особенно у молодых больных.
Источник: podari-zhizn.ru
Что такое миелодиспластический синдром?
Миелодиспластический синдром (МДС) — это диагноз рака. Является группой заболеваний, влияющих на кровь и мозг, различной степени тяжести, потребностей в лечении и продолжительности жизни.
Может быть первичным (самостоятельным) или следствием лечения рака. Первичная МДС не имеет очевидной причины. Связанная с лечением МДС имеет очевидную причину.
Как развивается миелодиспластический синдром?
ДНК (генетический материал) развивающиеся стволовые клетки в костном мозге повреждается. Это называется «приобретенной мутацией».
- Стволовые клетки образуют клетки крови (белые клетки, эритроциты и тромбоциты).
Это повреждение препятствует нормальному функционированию костного мозга. Когда костный мозг не работает должным образом, он не может производить достаточно здоровых клеток крови.
- Костный мозг производит недоразвитые (незрелые) клетки аномального размера, формы или внешнего вида, которые называются диспластическими (аномально сформированными) клетками.
- Может происходить скопление бластных клеток (незрелых клеток костного мозга), которые еще не могут выполнять специфическую функцию зрелой клетки.
- Костный мозг не может произвести достаточно здоровых эритроцитов, лейкоцитов или тромбоцитов.
В результате количество здоровых клеток крови (эритроцитов, лейкоцитов и тромбоцитов) обычно ниже нормы.
- Анемия — это состояние, когда в крови мало эритроцитов, что может вызвать усталость и одышку.
- Нейтропения — это состояние, при котором мало белых клеток, поэтому иммунная система не может эффективно защитить себя от инфекции из-за недостатка нейтрофилов (типа белых клеток).
- Тромбоцитопения — это состояние, при котором имеется небольшое количество тромбоцитов, которые могут вызвать кровотечение и легкие кровоподтеки без видимой причины.
- Панцитопения является состоянием, когда все три типа клеток в крови низкие.
Тем не менее, нарушения в клетках костного мозга у пациентов с МДС варьируются от легких до очень тяжелых.
- У некоторых пациентов клетки МДС все еще могут функционировать и попадать в кровь. Эритроциты продолжают нести кислород, белые клетки (нейтрофилы и моноциты) поглощают и убивают бактерии и тромбоциты, приводящие к повреждению кровеносных сосудов.
- В более тяжелых случаях МДС, образование клеток крови является более беспорядочным, и аномальные бластные клетки (бласты) накапливаются в костном мозге и крови. Эти клетки не созревают в клетки, которые функционируют должным образом. Они не так способны, как нормальные клетки, созревать в эритроциты, нейтрофилы и тромбоциты.
- Обычно бласты составляют менее 5 процентов всех клеток в костном мозге. При миелодиспластическом синдроме бласты часто составляют более 5 процентов клеток в костном мозге. Количество бластов в организме является ключевым для определения степени тяжести МДС.
Причины и факторы риска
В большинстве случаев врачи не могут определить конкретную причину МДС. Миелодиспластический синдром может быть либо первичным, также известным как «de novo», когда причина неизвестна, либо вторичным, известным как «связанный с лечением». У большинства людей с МДС диагностируется первичный или миелодиспластическим синдромом de novo.
- Первичная или МДС de novo — болезнь не имеет известной причины. В большинстве случаев случайные мутации (изменения ДНК) накапливаются в стволовых клетках при старении, и если эти мутации происходят в определенных генах и в определенных местах, возникает МДС.
- Вторичная (связанная с лечением) МДС — некоторые люди, которые проходили лечение от другого рака, имеют небольшой риск развития связанной с лечением МДС. Это происходит только у небольшого числа пациентов, подвергшихся химиотерапии и/или лучевой терапии, и встречается реже, чем случаи первичной МДС. В целом, вероятность развития МДС в результате лечения другого рака очень низка. У некоторых пациентов с редкими наследственными заболеваниями костного мозга, такими как анемия Фанкони или врожденный дискератоз, также может развиться вторичная МДС, как и у пациентов, ранее диагностированных с другим расстройством недостаточности костного мозга, называемым апластической анемией.
Нет никакого способа предотвратить возникновение миелодиспластического синдрома, и вы не можете его подцепить или передать кому-либо.
Признаки и симптомы миелодиспластического синдрома
У некоторых пациентов могут отсутствовать симптомы заболевания. Миелодиспластический синдром может быть обнаружен до появления симптомов в результате лабораторных анализов, которые были частью обычного медицинского обследования.
Тем не менее, люди с МДС часто имеют низкий уровень одного или нескольких типов клеток крови. Уменьшение количества клеток крови ниже нормы называется цитопенией. Большинство симптомов миелодиспластического синдрома вызваны нехваткой эритроцитов, лейкоцитов или тромбоцитов в крови.
Анемия — это уменьшение количества здоровых эритроцитов. Эритроциты переносят кислород по всему организму. Анемия может вызвать такие симптомы, как
- усталость;
- головокружение;
- слабость;
- одышка или дискомфорт в груди, особенно при физической нагрузке;
- бледность кожи (см. фото ниже).
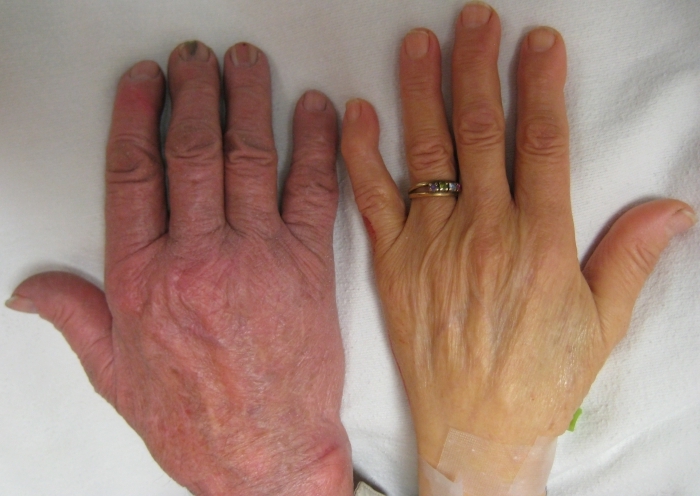
Нейтропения — это уменьшение количества здоровых лейкоцитов. Белые клетки крови помогают организму бороться с инфекцией. Нейтропения может привести к частым или тяжелым инфекциям у пациентов.
Тромбоцитопения — это уменьшение количества здоровых тромбоцитов. Тромбоциты помогают контролировать кровотечение и участвуют в заживлении ран. Тромбоцитопения может вызвать такие симптомы, как
- синяки на теле;
- кровотечения и кровоподтеки (см. фото ниже).
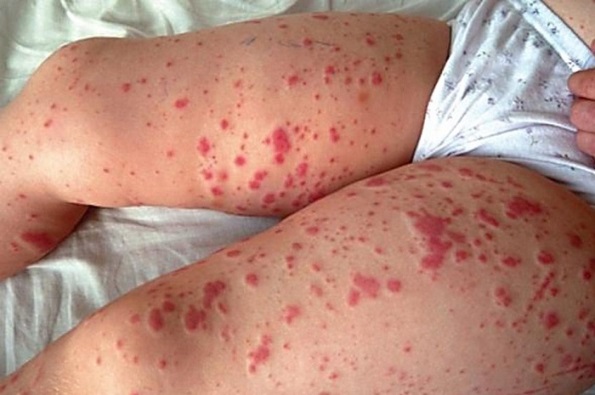
Диагностика МДС
Точный диагноз — один из важнейших аспектов ухода за человеком. Получение точного диагноза поможет врачу:
- оцените, как болезнь будет прогрессировать;
- определить наиболее подходящее лечение.
Поскольку МДС может быть трудно диагностируемым заболеванием, вы можете получить второе медицинское заключение у опытного гематопатолога до начала лечения.
Диагностические критерии
Диагноз миелодиспластического синдрома требует, чтобы в костном мозге была обнаружена хотя бы одна из следующих характеристик:
- бласты, составляющие от 5 до 19 процентов клеток костного мозга;
- очевидные изменения в структуре или форме клеток костного мозга (дисплазия);
- цитогенетические нарушения (хромосомное повреждение ДНК в клетках):
- «простая» цитогенетика означает, что поражено менее трех хромосом;
- «комплексная» цитогенетика означает, что три или более хромосом поражены.
Следующие анализы и обследования помогут врачу поставить диагноз.
Анализы крови

ОАК с дифференциалом. Врач назначит общий анализ крови (ОАК), который поможет измерить количество эритроцитов, лейкоцитов и тромбоцитов в крови. Эти измерения показывают степень, при которой клетки миелодиспластического синдрома в костном мозге влияют на нормальное развитие клеток крови.
Пациенты с МДС часто имеют небольшое количество одного или нескольких типов клеток крови. Общий анализ крови должен включать дифференциал, помогающий сравнить различные типы белых кровяных клеток в образце.
Низкое количество эритроцитов означает, что у вас анемия . Если у вас анемия, врач обследует ваши эритроциты, чтобы выяснить, вызвано ли ваше состояние миелодиспластическим синдромом или:
- низким содержанием железа, фолиевой кислоты или витамина B12;
- другой тип рака или проблемы с костным мозгом;
- еще одна причина анемии, например, почечная недостаточность.
Количество ретикулоцитов. Ретикулоциты — это клетки-предшественники (незрелые), которые развиваются в зрелые эритроциты. Количество ретикулоцитов измеряет количество ретикулоцитов в циркулирующей крови. Это может показать, как быстро эти клетки вырабатываются и высвобождаются костным мозгом и функционирует ли костный мозг должным образом. Когда у человека анемия, нормальным ответом является то, что костный мозг производит больше ретикулоцитов. Низкое количество ретикулоцитов указывает на то, что костный мозг работает плохо.
Анализ крови на эритропоэтин. Эритропоэтин — это вещество, вырабатываемое почками. Эритропоэтин стимулирует костный мозг производить больше эритроцитов. Анализ количества эритропоэтина в крови может помочь определить причину анемии.
Низкий уровень эритропоэтина может вызвать анемию и может быть признаком проблемы со здоровьем, кроме МДС. Низкий уровень эритропоэтина также может ухудшить анемию у человека с миелодиспластическим синдромом. Большинство пациентов с МДС, связанной с анемией имеют относительно низкие сывороточные уровни эритропоэтина.
Обследование костного мозга: аспирация и биопсия
Эти методы диагностики используются для подтверждения миелодиспластического синдрома. Обычно они проводятся одновременно в кабинете врача или в больнице. После того, как образцы взяты, патолог рассматривает образцы под микроскопом, чтобы оценить тип, размер, внешний вид и зрелость клеток.
- при аспирации костного мозга удаляется небольшое количество жидкого костного мозга изнутри кости.
- при биопсии костного мозга удаляет небольшой кусочек твердой кости вместе с небольшим количеством костного мозга.
Ниже приведены признаки миелодиспластического синдрома при обследовании:
- клетки аномального размера или формы (дисплазия);
- ненормальное количество (слишком много или слишком мало) клеток крови любого типа;
- увеличенное количество бластных клеток (незрелых клеток костного мозга);
- аномально низкое или высокое количество клеток в костном мозге;
- красные кровяные клетки, которые имеют слишком много или слишком мало железа.
Флуоресцентная гибридизация in situ, или метод FISH и кариотип
Эти методы обследования используются для идентификации клеток, которые содержат хромосомные аномалии. Исследования также могут помочь выявить аномальные клетки для диагностики заболевания, а также могут отслеживать и измерять результаты терапии. Хромосомные аномалии являются важными факторами при определении конкретных подтипов МДС, и иногда могут помочь врачам определить наиболее эффективный подход к лечению.
Цитогенетические аномалии.
Обычно клетки МДС имеют аномальные хромосомы. Приблизительно 50 процентов пациентов имеют один или несколько хромосомных дефектов. Существуют разные типы дефектов хромосом; например, часть хромосомы или вся хромосома может отсутствовать. Или может быть дополнительная копия хромосомы. Каждая хромосома делится на две секции, или «руки». Короткое плечо хромосомы обозначено как «p arm». Длинное плечо хромосомы обозначено «q arm».
Молекулярные генетические исследования
Эти обследования ищут мутации в генах, которые связаны с миелодиспластическим синдромом. Иногда результаты мутационного тестирования влияют на лечение МДС или его результаты. Молекулярное тестирование может быть сделано на образце крови или костного мозга. У некоторых пациентов с МДС он проводится для выявления генных аномалий.
Секвенирование ДНК — это тип молекулярного теста, который проверяет специфические генные мутации в раковых клетках. Определенные мутации связаны с лучшим или худшим исходом. Врачи используют результаты молекулярного тестирования, чтобы помочь планировать лечение.
Генетические мутации.
В последние годы исследования выявили несколько генных мутаций среди пациентов с МДС. Некоторые из этих мутаций могут оказывать влияние на исход заболевания.
Это заслуживает внимания, потому что:
- существует более 40 генов, которые могут быть видоизменены в миелодиспластический синдром;
- большое количество пациентов (более 80 процентов) могут иметь по крайней мере одну мутацию;
- основываясь на функциях этих мутированных генов, исследователи узнали о молекулярных механизмах, ответственных за развитие МДС;
- конкретный характер мутаций, наблюдаемый у пациентов с МДС, может частично объяснить изменчивость их заболевания и, вероятно, приведет к появлению более новых систем классификации, основанных на этих генетических отклонениях;
- подмножество мутаций может иметь прогностическое значение. Мутации в определенных генах ассоциировались как с лучшими, так и с худшими прогнозами, чем те, которые предсказаны Международной шкалой оценки прогноза (IPSS).
Подтипы миелодиспластического синдрома
Существует несколько видов (подтипов) МДС. Врачи классифицируют подтипы миелодиспластического синдрома в соответствии с различными факторами. Для их классификации врачи часто используют одну из двух систем: французскую, американскую, британскую (FAB (French-American-British)) систему классификации или систему классификации Всемирной организации здравоохранения (ВОЗ).
Классификация миелодиспластического синдрома значительно изменилась за последние несколько десятилетий. В 1982 году французско-американо-британская (FAB) рабочая группа разработала классификацию МДС. В 2001 году
Всемирная организация здравоохранения (ВОЗ) предложила альтернативную классификацию, которая была изменена по сравнению с первоначальным FAB и включала молекулярные и цитогенетические факторы. С тех пор классификация ВОЗ обновлялась дважды: один раз в 2008 году и еще раз в 2016 году.
Врачи также используют Международную шкалу оценки прогноза (IPSS) для более узкого определения степени тяжести заболевания, определения факторов риска для пациентов и планирования лечения.
FAB классификация
Классификация FAB разделила МДС на пять подтипов, основываясь на проценте бластов в костном мозге и периферической крови, количестве кольцевых сидеробластов (КС) и степени моноцитоза (повышенное количество лейкоцитов) следующим образом:
- Рефрактерная анемия (РА);
- Рефрактерная анемия с кольцевыми сидеробластами (РАКС);
- Рефрактерная анемия с избытком бластов (РАИБ);
- Рефрактерная анемия с избытком бластов в процессе трансформации ((РАИБ-Т);
- Хронический миеломоноцитарный лейкоз (ХММЛ).
Классификация ВОЗ
Текущие руководящие принципы классификации ВОЗ определяют 6 подтипов миелодиспластического синдрома на основе результатов анализа крови и костного мозга. Он классифицирует МДС по факторам, которые отличаются от факторов системы FAB:
- МДС с дисплазией одной линии:
- Рефрактерная анемия;
- Рефрактерная нейтропения;
- Рефрактерная тромбоцитопения.
- МДС с кольцевыми сидеробластами:
- Одноклеточная дисплазия;
- Многолинейная дисплазия.
- МДС с многолинейной дисплазией;
- МДС с избытком бластов:
- МДС с избытком бластов-1;
- МДС с избытком бластов-2.
- МДС с изолированной del (5q);
- МДС не не поддающееся классификации.
Международную шкалу оценки прогноза (IPSS)
Конкретные факторы могут повлиять на прогноз (вероятный исход) миелодиспластического синдрома (МДС) и помочь врачам определить, когда начинать лечение и насколько интенсивным должно быть лечение. Эти факторы включают:
- подтип МДСа;
- количество и тяжесть цитопений (низкое количество клеток крови);
- процент бластных клеток в костном мозге;
- тип и количество изменений хромосом.
Врачи используют эти прогностические факторы, чтобы назначить оценку и группу риска. Каждому прогностическому фактору присваивается число в зависимости от его серьезности. Более низкий балл обычно указывает на лучший прогноз. Баллы по всем факторам затем складываются, чтобы создать общую оценку риска.
Оценка риска описывает, насколько быстро заболевание может прогрессировать, и используется для отнесения пациента к определенной группе риска. Врачи используют информацию о группе риска пациента, чтобы выбрать подход к лечению.
Существует три основных прогностических системы оценки:
- шкала IPSS (International Prostate Symptom Score Международную шкалу оценки прогноза);
- прогностическая шкала IPSS-R (пересмотренная международная система прогностической оценки);
- шкала WPSS (система прогнозной оценки, основанная на классификации ВОЗ).
Первая — это наиболее часто используемая прогностическая система оценки. IPSS использует три «прогностических показателя» для прогнозирования течения заболевания пациента:
- процент лейкозных бластных клеток в костном мозге;
- тип хромосомных изменений, если таковые имеются, в клетках костного мозга (цитогенетика);
- наличие одного или нескольких клеток крови с низким содержанием (цитопения).
Низкие и промежуточные категории иногда объединяются в группу низкого риска; промежуточные 2 и высокие категории иногда объединяются в группу более высокого риска.
Второй IPSS —, известный как «IPSS-R», охватывает те же факторы заболевания, что и IPSS, но эти факторы определены более детально. IPSS-R показывает пять факторов заболевания:
- бластные клетки;
- цитогенетику;
- гемоглобин;
- абсолютное количество нейтрофилов;
- количество тромбоцитов.
Третий — WPSS используется не так часто, как IPPS и IPSS-R. Он отличается от двух других систем тем, что включает подтип миелодиспластического синдрома в качестве прогностического фактора. Он также назначает оценку на основе наличия или отсутствия тяжелой анемии.
Группы риска
Перед началом лечения врачи группируют состояние пациента в одну из двух категорий риска: МДС «с низким риском» или «с высоким риском». Каждая категория включает в себя определенные группы риска от каждой из систем оценки.
Важно отметить, что прогностические системы и группы риска не предсказывают, как МДС будет реагировать на лечение, а вместо этого они подскажут, как МДС, вероятно, будет вести себя со временем без лечения.
МДС с меньшим риском имеет тенденцию расти и прогрессировать медленно. Она может не вызывать много или даже серьезных симптомов в течение длительного времени. Следовательно, часто используется менее интенсивное лечение. Напротив, миелодиспластический синдром с более высоким риском может прогрессировать быстрее или превратиться в острый миелоидный лейкоз без лечения, что может вызвать больше симптомов и осложнений со здоровьем за короткое время. Таким образом, часто требуется более интенсивная терапия.
Лечение миелодиспластического синдрома
Положение каждого пациента должно оцениваться индивидуально гематологом-онкологом, который специализируется на лечении МДС и который обсудит с пациентом подтип заболевания, прогностические факторы и варианты лечения. Также важно обратиться за лечением в центр, который имеет опыт лечения миелодиспластического синдрома.
Типы лечения МДС
Врачи используют несколько типов подходов и комбинаций лечения МДС:
- поддерживающая терапия:
- переливания крови;
- хелатная терапия железом;
- факторы роста клеток крови;
- медикаментозная терапия:
- аллогенная трансплантация стволовых клеток.
Также врач может предложить принять участие в клиническом испытании. Клинические испытания могут включать терапию новыми препаратами и новыми комбинациями лекарств или новыми подходами к трансплантации стволовых клеток.
В поисках лучшего подхода к лечению
Лечение, которое рекомендует врач, основано на нескольких факторах, в том числе:
- находитесь ли вы в категории низкого или высокого риска;
- подтип вашего МДС;
- общее состояние здоровья;
- другие болезни, которые у вас могут быть, называемые сопутствующими заболеваниями, такие как болезни сердца, болезни почек, болезни легких или сахарный диабет.
Поскольку МДС с меньшим риском прогрессирует медленнее, обычно в первую очередь используются низкоинтенсивное лечение. Цели для пациентов с МДС с низким риском:
- улучшить показатели крови;
- уменьшите потребность в переливаниях крови;
- снизить риск заражения;
- улучшить качество жизни.
МДС с высоким риском имеет тенденцию быстро расти и прогрессировать в острый миелоидный лейкоз в более короткие сроки. По этой причине обычно используются более интенсивные методы лечения. Цели для пациентов с МДС высокого риска:
- замедлить или остановить прогрессирование миелодиспластического синдрома до острого миелоидного лейкоза;
- увеличить продолжительность жизни.
Возможно, вам будет полезно пригласить любимого человека к себе на прием к врачу, а также делать записи и задавать дополнительные вопросы. Хорошей идеей будет подготовить вопросы, которые вы хотели бы задать, посетив врача. Вы также можете записывать разговор с врачом и более внимательно прослушать, когда вернетесь домой.
Поддерживающая терапия
Лечение, проводимое для облегчения симптомов заболевания и побочных эффектов терапии, называется поддерживающим лечением. Цель поддерживающего лечения — улучшить качество жизни пациента и максимально уменьшить дискомфорт. Поддерживающий уход является важной частью лечения МДС.
Переливания крови
Переливание эритроцитов может помочь некоторым пациентам, улучшив их количество в крови или сняв симптомы анемии, такие как одышка, головокружение, сильная усталость и боль в груди. Переливание может помочь облегчить симптомы на короткое время, но со временем может потребоваться больше переливаний.
При МДС от 60 до 80 процентов пациентов страдают анемией на момент постановки диагноза, и до 90 процентов пациентов нуждаются в одном или нескольких переливаниях в течение всей болезни.
Переливание тромбоцитов может использоваться у пациентов с тромбоцитопенией (низким количеством тромбоцитов), которая может вызывать такие симптомы, как легкие кровоподтеки или кровотечение. Переливание крови обычно требуется, когда количество тромбоцитов у пациента падает ниже 10000/мкл.
Аминокапроновая кислота, антифибринолитическое средство, рекомендуется при кровотечениях, которые не реагируют на переливание тромбоцитов, и в случаях тяжелой тромбоцитопении. Это лекарство работает, предотвращая слишком быстрое разрушение сгустков крови.
Хелатная терапия железом
Железо содержится в эритроцитах. Когда человек получает большое количество переливаний эритроцитов, слишком много железа может накапливаться в организме. Это называется передозировка железом, и со временем она может повредить жизненно важные органы.
При хелатной терапии железом применяются препараты, называемые «хелаторами», которые связывают избыток железа и выводят его из организма. Эта терапия может быть подходящей для пациентов с анемией, которые нуждаются в частых переливаниях крови (более 4 единиц эритроцитов в течение 8 недель). Наиболее распространенные препараты, используемые при этой терапии, включают:
- Деферазирокс (Эксиджад®);
- Дефероксамина мезилат (Десферал®).
Для пациентов, которым необходимо частое переливание эритроцитов, рекомендуется, чтобы врачи следили за уровнем ферритина (железа) в сыворотке и часто проверяли наличие признаков повреждения органов.
Факторы роста клеток крови
Агенты, называемые «факторами роста», способствуют выработке клеток крови в костном мозге. Эти агенты используются для лечения некоторых пациентов, у которых количество клеток крови уменьшено.
Факторы роста красных кровяных клеток.
Эритропоэтин (ЭПО) — это гормон, созданный в почках. Он стимулирует выработку эритроцитов в ответ на низкий уровень кислорода в организме. Нехватка ЭПО также может вызвать анемию.
Стимуляторы эритропоэза — это факторы роста эритроцитов, которые являются фармацевтическими аналогами природного ЭПО. Они используются для пациентов с МДС, у которых анемия связана с низким уровнем ЭПО. Лечение с помощью стимуляторов эритропоэза может снизить потребность в переливании крови и, возможно, улучшить выживаемость.
- Эпоэтин альфа (Эпокрин®) и дарбэпоэтин альфа (Аранесп®) являются типами стимуляторов эритропоэза. Их назначают инъекцией под кожу. Дарбепоэтин альфа является более длительно действующей формой ЭПО, чем дарбэпоэтин альфа.
Большинство пациентов с МДС не имеют низких уровней ЭПО, поэтому введение стимуляторов не является полезным лечением их анемии. Тем не менее, все пациенты с миелодиспластическим синдромом должны проверить уровень ЭПО.
Некоторые пациенты с МДС и низким уровнем ЭПО могут не получать пользу от терапии только стимуляторами; однако стимуляторы эритропоэза, данный вместе с Г-КСФ, может увеличить концентрацию гемоглобина (см. ниже).
Факторы роста лейкоцитов.
Факторы роста лейкоцитов естественным образом вырабатываются организмом и помогают увеличить выработку лейкоцитов. Синтетические версии этих веществ могут быть использованы для лечения пациентов с частыми инфекциями, вызванными нейтропенией, но они, как известно, не помогают пациентам жить дольше.
- Гранулоцитарный колониестимулирующий фактор (Г-КСФ), который помогает организму увеличить производство лейкоцитов. Филграстим (Нейпоген®) и Пегфильграстим (Неуластим®) являются примерами препаратов Г-КСФ.
- Гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) помогает организму вырабатывать много разных типов лейкоцитов. Сарграмостим (Лейкин®) является препаратом ГМ-КСФ.
Факторы роста тромбоцитов.
Тромбопоэтин (ТПО) — это вещество, которое помогает организму вырабатывать тромбоциты.
- Ромиплостим (Энплейт®) и элтромбопаг (Револейд®) являются препаратами, которые действуют как TPO. Эти агенты исследуются в качестве лечения пациентов с миелодиспластическим синдромом, у которых низкий уровень тромбоцитов. В настоящее время эти препараты одобрены FDA для лечения тромбоцитопении (низкое количество тромбоцитов) у пациентов с хронической иммунной тромбоцитопенической пурпурой (ИТП) и имеющих недостаточный ответ на кортикостероиды, иммуноглобулины или спленэктомию.
- Хотя ромиплостим и элтромбопаг не одобрены специально для лечения МДС, иногда они могут быть полезны пациентам с очень низким количеством тромбоцитов.
Управление инфекциями
Низкое количество лейкоцитов может увеличить риск заражения. В некоторых случаях инфекция может быть частой или тяжелой. Команда по лечению будет уделять пристальное внимание любой инфекции или необъяснимой лихорадке. Если идентифицирована или подозревается бактериальная инфекция, могут назначить антибиотики. Антивирусные препараты могут использоваться для лечения определенных вирусных инфекций.
Химиотерапия и медикаментозная терапия

Существует много разных видов лекарств, используемых при лечении миелодиспластического синдрома:
Гипометилирующие агенты
Препараты с меньшей вероятностью вызывают серьезные побочные эффекты и часто назначаются амбулаторно. Для лечения МДС утверждены два препарата для химиотерапии низкой интенсивности:
- Азацитидин (Видаза®);
- Децитабин (Дакоген®).
Иммунодепрессивная терапия
Этот тип терапии использует лекарства, которые подавляют определенные части иммунной системы. Например, при некоторых типах МДС лимфоциты могут поражать костный мозг, что приводит к тому, что он перестает вырабатывать достаточно здоровых клеток крови. Основными препаратами иммунодепрессивной терапии, используемыми для лечения МДС, являются:
- Антитимоцитарный глобулин (АТГ [Тимоглобулин®]);
- Циклоспорин (Неорал®);
- Такролимус (Програф®).
Этот тип терапии не подходит для всех типов МДС; оно наиболее эффективно, когда миелодиспластический синдром обладает функциями, связанными с атакой иммунной системы, такими как:
- наличие белка HLA-DR15;
- низкое количество клеток в костном мозге;
- младшие пациенты с МДС низкого риска.
Иммуномодуляторы
Иммуномодуляторы модифицируют различные части иммунной системы. Следующее лекарственное средство одобрено для лечения МДС низкого риска с удалением 5q [del (5q)]:
- Леналидомид (Ревлимид®).
Лечение этим препаратом может снизить необходимость переливания эритроцитов у некоторых пациентов.
Высокоинтенсивная терапия
Этот тип терапии включает в себя использование препаратов интенсивной химиотерапии или трансплантации стволовых клеток. Высокоинтенсивная химиотерапия включает лекарственные препараты и схемы лечения, обычно используемые для лечения ОМЛ (острый миелоидный лейкоз).
Поскольку эти агенты имеют тенденцию вызывать более серьезные побочные эффекты, они обычно используются только для МДС, который может прогрессировать до острого миелоидного лейкоза (заболевание высокого риска). Пациентам с МДС в промежуточной категории – 2 и IPSS высокого риска может потребоваться лечение с помощью высокоинтенсивной химиотерапии. Используемые лекарства могут включать
- Цитарабин (Цитозина арабинозид, Цитозар®);
- Идарубицин;
- Даунорубицин (Церубидин®);
- Митоксантрон (Новантрон®).
Химиотерапия может проводиться отдельно или в комбинации двух или трех различных препаратов (комбинированная химиотерапия). При лечении комбинированной терапией:
- могут быть использованы низкие дозы препаратов;
- количество клеток крови пациента может ухудшиться. Если количество клеток ухудшается, врач оценит состояние пациента, чтобы решить, можно ли продолжать интенсивную химиотерапию.
Ингибиторы тирозинкиназы
Ингибиторы тирозинкиназы — это лекарства, которые нацелены на аномальные белки, вызывающие неконтролируемый рост клеток. Следующее лекарственное средство одобрено для взрослых пациентов с миелодиспластическими синдромами/миелопролиферативными новообразованиями (МДС/МПН), связанными с перестройками генов PDGFR (тромбоцитарного фактора роста):
- Иматиниба мезилат (Гливек®).
Аллогенная трансплантация стволовых клеток
Аллогенная трансплантация стволовых клеток используется иногда для лечения пациентов с МДС. Однако из-за высокого и часто опасного для жизни риска, связанного с трансплантацией стволовых клеток, это лечение в основном рассматривается для:
- пациентов моложе 60 лет;
- пациентов до 75 лет, у которых хорошее здоровье;
- пациентов, которые относятся либо к промежуточному классу IPSS – 2, либо к категории высокого риска IPSS, либо имеют (вторичную) МДС, связанную с терапией рака в прошлом;
- пациентов, у которых есть донор стволовых клеток, сопоставленный с лейкоцитарным антигеном (HLA) человека (одноуровневое или несвязанное совпадение).
Аллогенные трансплантации стволовых клеток могут также рассматриваться для выборочных пациентов с МДС низкого риска с тяжелой цитопенией. Аутологичная трансплантация с использованием собственных стволовых клеток пациента используется при некоторых других заболеваниях, но не применяется при миелодиспластическом синдроме, поскольку собственные стволовые клетки пациента являются ненормальными из-за заболевания.
Прививка против болезни хозяина. Серьезным риском аллогенной трансплантации стволовых клеток является болезнь “трансплантат против хозяина“, которое развивается, если иммунные клетки донора атакуют вашу нормальную ткань. Побочные эффекты этой болезни могут варьироваться от незначительных до угрожающих жизни.
Трансплантация аллогенных стволовых клеток пониженной интенсивности
Пациенты, которые не переносят аллогенную трансплантацию с помощью высокоинтенсивной химиотерапии, могут иметь право на трансплантацию стволовых клеток пониженной интенсивности (иногда называемую немиелоабляционным трансплантатом).
При таком типе трансплантации пациенты получают более низкие дозы химиотерапевтических препаратов и/или облучения. Они получают иммунодепрессанты для предотвращения отторжения трансплантата (донорских клеток), чтобы иммунные клетки донора могли атаковать раковые клетки. Эту атаку называют эффект “трансплантат против лейкоза” (ТПЛ).
Исследования изучают возможность использования этого типа трансплантата у пожилых людей с рецидивом и/или с рефрактерным заболеванием. Трансплантация стволовых клеток пониженной интенсивности обычно используется пациентам старше 55–60 лет.
Вакцинотерапия
В настоящее время проводятся клинические испытания для определения эффективности вакцины против миелодиспластического синдрома при лечении пациентов с МДС высокого риска. Вакцина изготовлена из белковых строительных блоков, называемых «пептидами», которые могут помочь организму создать эффективный иммунный ответ против клеток МДС.
Источник: tvojajbolit.ru
Миелодиспластический синдром
Миелодиспластический синдром – группа заболеваний и состояний с нарушениями миелоидного кроветворения и высоким риском развития острого лейкоза. Вероятность развития увеличивается с возрастом, в 80% случаев данный синдром диагностируется у людей старше 60 лет. Мужчины страдают несколько чаще женщин. У детей миелодиспластический синдром практически не встречается. В последние десятилетия гематологи отмечают увеличение заболеваемости среди лиц трудоспособного возраста. Предполагается, что причиной «омоложения» болезни могло стать существенное ухудшение экологической обстановки.
До недавнего времени лечение миелодиспластического синдрома было только симптоматическим. Сегодня специалисты разрабатывают новые методы терапии, однако эффективное лечение этой группы болезней все еще остается одной из самых сложных проблем современной гематологии. Пока прогноз при миелодиспластическом синдроме, в основном, зависит от особенностей течения болезни, наличия или отсутствия осложнений. Лечение осуществляют специалисты в сфере онкологии и гематологии.
Причины и классификация миелодиспластического синдрома
С учетом причин развития различают два типа миелодиспластического синдрома: первичный (идиопатический) и вторичный. Идиопатический вариант выявляется в 80-90% случаев, диагностируется преимущественно у пациентов старше 60 лет. Причины возникновения установить не удается. В числе факторов риска первичного миелодиспластического синдрома – курение, повышенный уровень радиации при выполнении профессиональных обязанностей или проживании в неблагоприятной экологической зоне, частый контакт с бензином, пестицидами и органическими растворителям, некоторые наследственные и врожденные заболевания (нейрофиброматоз, анемия Фанкони, синдром Дауна).
Вторичный вариант миелодиспластического синдрома наблюдается в 10-20% случаев, может возникать в любом возрасте. Причиной развития становится химиотерапия или радиотерапия по поводу какого-то онкологического заболевания. В число лекарственных средств с доказанной способностью вызывать миелодиспластический синдром включают циклофосфан, подофиллотоксины, антрациклины (доксорубицин) и ингибиторы топоизомеразы (иринотекан, топотекан). Вторичный вариант отличается более высокой резистентностью к лечению, более высоким риском развития острого лейкоза и более неблагоприятным прогнозом.
В современной редакции классификации ВОЗ различают следующие типы миелодиспластического синдрома:
- Рефрактерная анемия. Сохраняется более полугода. В анализе крови бласты отсутствуют либо единичные. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная анемия с кольцевыми сидеробластами. Сохраняется более полугода. В анализе крови бласты отсутствуют. В костном мозге дисплазия эритроидного ростка.
- Рефрактерная цитопения с многолинейной дисплазией. В анализе крови тельца Ауэра отсутствуют, бласты отсутствуют либо единичные, выявляются панцитопения и увеличение количества моноцитов. В костном мозге диспластические изменения менее 10% клеток в 1 миелоидной клеточной линии, бластов менее 5%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-1. В анализе крови тельца Ауэра отсутствуют, бластов более 5%, цитопения и увеличение количества моноцитов. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 5-9%, телец Ауэра нет.
- Рефрактерная анемия с избытком бластов-2. В анализе крови увеличение количества моноцитов, цитопения, бластов 5-19%, могут выявляться тельца Ауэра. В костном мозге дисплазия одной либо нескольких клеточных линий, бластов 10-19%, обнаруживаются тельца Ауэра.
- Неклассифицируемый миелодиспластический синдром. В анализе крови цитопения, бласты отсутствуют либо единичные, тельца Ауэра отсутствуют. В костном мозге дисплазия одного мегакариоцитарного либо гранулоцитарного ростка, бластов более 5%, тельца Ауэра отсутствуют.
- Миелодиспластический синдром, ассоциированный с изолированной делецией 5q. В анализе крови анемия, бластов более 5%, возможен тромбоцитоз. В костном мозге более 5% бластов, тельца Ауэра отсутствуют, изолированная делеция 5q.
Симптомы миелодиспластического синдрома
Клиническая симптоматика определяется степенью нарушений миелопоэза. При мягко протекающих расстройствах возможно длительное бессимптомное или стертое течение. Из-за слабой выраженности клинических проявлений некоторые больные не обращаются к врачам, и миелодиспластический синдром обнаруживается во время проведения очередного медицинского осмотра. При преобладании анемии наблюдаются слабость, одышка, плохая переносимость физических нагрузок, бледность кожных покровов, головокружения и обморочные состояния.
При миелодиспластическом синдроме с тромбоцитопенией возникает повышенная кровоточивость, отмечаются десневые и носовые кровотечения, на коже появляются петехии. Возможны подкожные кровоизлияния и меноррагии. Миелодиспластический синдром с выраженными нейтропенией и агранулоцитозом проявляется частыми простудами, стоматитом, синуситом или стрептодермией. В тяжелых случаях возможно развитие пневмонии или сепсиса. Инфекционные заболевания нередко вызываются грибками, вирусами или условно-патогенными микробами. У каждого пятого пациента с миелодиспластическим синдромом выявляется увеличение лимфоузлов, селезенки и печени.
Диагностика миелодиспластического синдрома
Диагноз выставляется с учетом данных лабораторных исследований: анализа периферической крови, биопсии костного мозга с последующим цитологическим исследованием, цитохимических и цитогенетических тестов. В анализе периферической крови больных миелодиспластическим синдромом обычно обнаруживается панцитопения, реже выявляется дву- или одноростковая цитопения. У 90% пациентов наблюдается нормоцитарная либо макроцитарная анемия, у 60% — нейтропения и лейкопения. У большинства больных миелодиспластическим синдромом отмечается тромбоцитопения.
При исследовании костного мозга количество клеток обычно нормальное либо повышенное. Уже на ранних стадиях обнаруживаются признаки дизэритропоэза. Количество бластов зависит от формы миелодиспластического синдрома, может быть нормальным либо увеличенным. В последующем наблюдаются дисгранулоцитопоэз и дисмегакариоцитопоэз. У некоторых больных признаки дисплазии костного мозга выражены очень слабо. В процессе цитогенетического исследования у ¾ больных выявляются хромосомные нарушения. Дифференциальный диагноз миелодиспластического синдрома проводят с В12-дефицитной анемией, фолиево-дефицитной анемией, апластической анемией, острым миелолейкозом и другими острыми лейкозами.
Лечение и прогноз при миелодиспластическом синдроме
Тактика лечения определяется выраженностью клинической симптоматики и лабораторных изменений. При отсутствии явных признаков анемии, геморрагического синдрома и инфекционных осложнений осуществляется наблюдение. При миелодиспластическом синдроме с выраженной анемией, тромбоцитопенией и нейтропенией, а также при высоком риске возникновения острого лейкоза назначают сопроводительную терапию, химиотерапию и иммуносупрессивную терапию. При необходимости осуществляют пересадку костного мозга.
Сопроводительная терапия является самым распространенным методом лечения миелодиспластического синдрома. Предусматривает внутривенные инфузии компонентов крови. При длительном применении может провоцировать повышение уровня железа, влекущее за собой нарушения деятельности жизненно важных органов, поэтому переливания гемокомпонентов производят при одновременном приеме хелаторов (лекарственных средств, связывающих железо и способствующих его выведению).
Иммуносупрессоры эффективны при лечении миелодиспластического синдрома с отсутствием хромосомных аномалий, наличием гена HLA-DR15 и гипоклеточном костном мозге. Химиотерапию применяют при невозможности трансплантации костного мозга. Высокие дозы препаратов используют при трансформации миелодиспластического синдрома в острый лейкоз, а также при рефрактерных анемиях с избытком бластов при нормоклеточном и гиперклеточном костном мозге, низкие – при невозможности пересадки костного мозга. Наряду с перечисленными средствами пациентам назначают гипометилирующие средства (азацитидин). Наиболее надежным способом достижения полноценной длительной ремиссии является трансплантация костного мозга.
Прогноз зависит от типа миелодиспластического синдрома, количества хромосомных аномалий, необходимости в регулярных переливаниях компонентов крови, выраженности клинических проявлений и наличия осложнений. Различают 5 групп риска. Средняя выживаемость больных миелодиспластическим синдромом, входящих в группу с самым низким уровнем риска, составляет более 11 лет; с самым высоким – около 8 месяцев. Вероятность отторжения костного мозга после трансплантации – около 10%.
Источник: yandex.ru
Классификация синдрома
Принято разделять первичную и вторичную патологии. Последняя отличается худшим прогнозом и большей устойчивостью к лечению. Это связано с тем, что дисплазия в таких случаях возникает в ответ на применение цитостатиков и других химиотерапевтических агентов, имеющих среди побочных эффектов угнетение функции костного мозга. Первичный синдром лучше поддается терапии и возникает идиопатически.

Принята классификация, которая делит миелодисплазию на несколько типов:
- Рефрактерная анемия представляет собой явление, сопровождающееся снижением количества красных клеток крови, которое имеет устойчивый характер. При этом бласты в анализе отсутствуют либо определяются в небольшом количестве. Подобное состояние сохраняется до полугода.
- Рефрактерная анемия с кольцевыми сидеробластами также отличается устойчивостью. При данной проблеме в анализах крови определяются клетки с аномальным расположением гранул железа. В костном мозге выявляют изменение эритроидного отростка.
- Малокровие с многолинейной дисплазией сопровождается только увеличением содержания моноцитов – специфических клеток иммунной системы. Количество бластов в анализах крови незначительное, растущие структуры появляются и в костном мозге. При этом дисплазия отмечается только в одной миелоидной линии.
- Рефрактерная анемия с избытком бластов-1 характеризуется наличием в анализах палочек Ауэра – своеобразных белковых включений в моноцитах. Они имеют красный цвет при специфическом окрашивании. Количество бластов превышает 5%. В костном мозге отмечается дисплазия нескольких клеточных линий. Тельца Ауэра при этом обнаруживаются только в образцах крови.
- При устойчивом малокровии с избытком бластов-2 отмечается цитопения. Количество растущих несозревших клеток достигает 19%. При данной проблеме палочки Ауэра выявляются уже в костном мозге.
- Миелодиспластический синдром, ассоциированный с патологией 5 хромосомы, характеризуется тромбоцитозом на фоне анемии. Отмечается также наличие миелобластных клеток, количество которых превышает 5%. Специфическая черта – перестройка генетического материала, сопровождающаяся частичной его утратой.
- Неклассифицируемый миелопатический синдром не отличается специфическими признаками. Выявляется лишь дисплазия гранулоцитарного ростка.
Симптомы патологии
Клиническая картина заболевания зачастую нехарактерна. Для нарушения гемопоэза характерно долгое латентное течение. Панцитопения, или снижение концентрации клеток крови, во многих случаях является случайной находкой при прохождении пациентом диспансеризации. Проявления МДС зависят от степени выраженности нарушений синтеза клеток костным мозгом. Классические симптомы болезни:
- Общая слабость и плохая переносимость физических нагрузок.
- Появление одышки сначала во время активности, а позднее и в покое. Это обусловлено снижением концентрации эритроцитов, одна из функций которых заключается в переносе кислорода к тканям.
- Развитие головокружения и обморочные состояния. Обусловлены как общей слабостью и истощенностью организма, так и дыхательной недостаточностью.
- На более поздних стадиях у пациентов выявляется повышенный риск кровотечений. Формируются петехии, а также гематомы на месте незначительных травм.
- Когда происходит развитие панцитопении, снижается и иммунная защита. Это сопровождается постоянными вирусными заболеваниями, возникновением инфекционных поражений ротовой полости, гортани и легких. В самых тяжелых случаях процесс приобретает генерализованный характер и развивается сепсис.
Причины возникновения
Идиопатический тип недуга, то есть первичное заболевание, формируется в 85% случаев. Миелодиспластический синдром провоцируется следующими факторами:
- Воздействие радиации, а также контакт с канцерогенными веществами – растворителями, пестицидами и т. д. Эти соединения обладают свойством угнетать работу костного мозга.
- Наличие врожденных наследственных заболеваний, способных пагубно влиять на гемопоэз.
- Прием лекарственных средств, угнетающих работу иммунной системы. К данной категории относятся вещества, применяемые в трансплантологии и лечении ревматоидных проблем.
- Пожилой возраст также является фактором, увеличивающим вероятность развития миелодиспластического синдрома. Это связано с накоплением в течение жизни генетических ошибок, способных привести к нарушению работы костного мозга.
К причинам, вызывающим вторичный МДС, относят химиотерапевтическое лечение «Циклоспорином», «Доксорубицином» и другими препаратами, а также применение ионизирующей радиации при борьбе с новообразованиями. Угнетение миелопоэза – распространенное и опасное осложнение в онкологии.
Диагностика
Обследование начинают со сбора анамнеза. При наличии у пациента жалоб на недомогание и общую слабость потребуется проведение анализов крови. Выявление в тестах снижения концентрации эритроцитов, а также панцитопении указывает на диагноз, связанный с нарушением гемопоэза. Лабораторные исследования играют ключевую роль в подтверждении миелодиспластических процессов. Они позволяют выявить наличие бластных, то есть растущих клеток, которые и указывают на формирование проблемы. Обследование включает и физикальный осмотр, в процессе которого обнаруживаются бледность слизистых оболочек и петехии на коже.
Применяются и визуальные методы, такие как ультразвук, который позволяет сделать фото внутренних органов. В тяжелых случаях на УЗИ обнаруживают увеличение размеров печени и селезенки.

Ключевым исследованием в диагностике лейкоза и миелодиспластического синдрома является биопсия костного мозга. Это довольно болезненная процедура, которая производится при помощи специальных игл. Полученный образец подвергается морфологическому анализу. В микропрепаратах обнаруживают бласты, тельца Ауэра, изменение соотношения клеток эритроидного ряда и другие отклонения. На основании результатов данного теста болезнь классифицируют.
При этом важно учитывать, что зачастую даже стандартное гистологическое исследование не дает точного результата. Это связано с необходимостью типирования находящихся в образце клеток. Подобная дифференциация имеет важное прогностическое значение, а также влияет на тактику лечения недуга. С этой целью требуется использование наиболее современных методов, например, проточной цитометрии. Данная техника активно применяется в развитых странах для диагностики онкологических процессов в костном мозге, лимфатической системе и крови.
Иммунофенотипирование позволяет различать клоны клеток. Причем анализ способен дифференцировать как бласты, так и зрелые структуры. Специфического маркера, указывающего на возникновение миелодиспластического синдрома, на сегодняшний день нет. Однако существуют комбинации параметров, используемых при проточной цитометрии, которые позволяют с высокой точностью определить не только наличие патологического процесса, но и выявить его тип. Такой анализ полезен и тем, что обладает высокой чувствительностью. Он помогает поставить диагноз в наиболее сложных случаях, например, у пациентов, страдающих от миелопатии, лишенной специфических маркеров или лабораторных признаков.
Методы лечения
Клинические рекомендации при миелодиспластическом синдроме зависят от типа заболевания, его причины и состояния пациента на момент постановки диагноза. Тактика борьбы с недугом определяется врачом. Основной задачей является облегчение состояния человека. Поскольку классическим проявлением проблемы считается угнетение работы костного мозга, применяются средства для его стимуляции. Например, «Эритропоэтин» относится к препаратам, усиливающим кроветворение. Это способствует устранению анемии и связанных с ней гипоксических явлений. В числе рекомендаций при борьбе с МДС и такой медикамент, как «Ревлимид», который является эффективным иммуностимулятором. Он провоцирует активное производство иммунных клеток, что улучшает дальнейший прогноз заболевания.
Лечение миелодиспластического синдрома предполагает также борьбу с секундарной микрофлорой. Поскольку при панцитопении защитные силы организма ослабевают, оправдано использование антибиотиков широкого спектра действия. Это позволяет профилактировать сепсис.
Чтобы повысить содержание форменных элементов крови, применяется заместительная терапия. Она значительно улучшает лабораторные показатели и состояние пациента за короткий срок. Уменьшаются проявления малокровия или панцитопении. Переливание крови оправдано в наиболее тяжелых случаях, когда добиться выраженного эффекта при применении стимуляторов гемопоэза не удается.
На сегодняшний день методом выбора в борьбе с МДС является трансплантация стволовых клеток. Она позволяет восстановить нормальную работу костного мозга и значительно улучшает состояние пациентов. Основную проблему при этом составляет поиск доноров.
Прогноз при миелодиспластическом синдроме
Исход недуга зависит от причины его возникновения и состояния больного. Проблема опасна тем, что может трансформироваться в онкологический процесс – острый лейкоз, излечение которого не всегда возможно. Прогноз при миелодиспластическом синдроме, как правило, осторожный. Идиопатический процесс гораздо лучше отвечает на терапию, чем вторичная проблема. Чем раньше МДС обнаружен, тем выше шанс на выздоровление.
Отзывы о лечении
Руслан, 38 лет, г. Липецк
Во время плановой диспансеризации в анализах крови выявили панцитопению. Поставили диагноз миелодиспластический синдром. Назначили стимуляторы гемопоэза. Врачи говорят, что это связано с перенесенной в прошлом трансплантацией печени. Тогда долго принимал иммуносупрессоры. Сейчас анализы пришли в норму, но требуется регулярный контроль показателей крови.
Варвара, 27 лет, г. Чебоксары
Были жалобы на общую слабость и одышку, два раза падала в обморок. После проведения обследования диагностировали миелодиспластический синдром. Врачи не знают, чем он вызван. На фоне этой болезни развился лейкоз. Проходила химиотерапию, выполнили пересадку костного мозга. После трансплантации чувствую себя лучше. Надеюсь на ремиссию.
Источник: ProSindrom.ru
