Что такое токсический синдром
Токсическим синдромом является состояние, которое развивается как ответ на агрессивное воздействие токсических веществ. Эти токсические вещества поступают извне, а также могут появляться в самом организме.
Очень часто возникает данный синдром у детей в раннем возрасте. Инкубационный период длится от одной до нескольких недель.
Обычно данным синдром развивается при желудочно-кишечных заболеваниях, которые развиваются из-за инфекций – сальмонеллы, при дизентерии, стафилококки.
Токсический синдром влияет на работу центральной нервной и сердечно-сосудистой систем, что может привести даже к летальному исходу.
Причины возникновения
Причины появления и развития токсического синдрома можно поделить на несколько больших групп:
- Желудочно-кишечные заболевания инфекционной природы. Сюда относятся колиэнтериты, вторичные токсикозы, сальмонеллез, стафилококковые энтериты.
- Наследственные заболевания обмена веществ. К этой группе относятся такие заболевания как почечный тубулярный ацидоз, непереносимость дисахаридов, лактацидоз, адреногенитальный синдром с изменением водно-солевого баланса, гипоальдостеронизм;
- Прочие заболевания, которые могут стать причиной токсического синдрома: пневмония, острая респираторно-вирусная инфекция, отиты и синуситы.
Симптомы токсического синдрома
Токсический синдром прежде всего поражает центральную нервную систему, исходя из этого он начинается остро и сопровождается сильным возбуждением, которое сменяется угнетенным состоянием.
Температура поднимается до отметки 39-40 градусов. Появляется одышка.
Пульс может быть очень частым – до 180 ударов в минуту. Если состояние ухудшается, то пульс учащается до 22 ударов.
Количество мочи значительно уменьшается, вплоть до того, что может исчезнуть совсем.
Также одним из самых главных симптомов может быть рвота, понос, обезвоживание.
Диагностика заболевания Методы лечения
Методы лечения
Как только токсический синдром дает о себе знать, то больного необходимо сразу же госпитализировать. В стационарных условиях уже проводят коррекцию путем внутривенных инъекций глюкозы, а также солевых растворов.
После проведения экстренных мероприятий врач-специалист назначает лечение основного заболевания, собственно, из-за которого взял свое начало токсический синдром.
Источник: 24doctor.info
Болезнь Вильсона это:
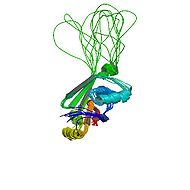

Болезнь Вильсона — Коновалова (гепатоцеребральная дистрофия, гепатолентикулярная дегенерация, болезнь Вестфаля — Вильсона — Коновалова) — врождённое нарушение метаболизма меди, приводящее к тяжелейшим наследственным болезням центральной нервной системы и внутренних органов.
Диагностируется у 5-10 % больных циррозом печени дошкольного и школьного возраста. Заболевание передается по аутосомно-рецессивному типу. Ген ATP7B, мутации которого вызывают заболевание, расположен на 13-й хромосоме (участок 13q14-q21).
История
Английский невролог Сэмюель Вильсон (англ. S. Wilson — более нормативная передача Уилсон)(1878 — 1937) в 1912 году описал типичные для гепато-церебральной дистонии изменения в головном мозге, установил постоянное наличие цирроза печени и дал описание клиники нового заболевания, названного им прогрессивной лентикулярной дегенерацией (лат. lenticularis чечевицеобразный).
В качестве основных симптомов заболевания были отмечены разнообразные непроизвольные движения в конечностях и туловище, мышечная ригидность, приводящая к скованности, дисфагия и дизартрия, аффектные вспышки, иногда психические расстройства, но признаки поражения пирамидных путей отсутствовали. Ещё раньше К. Вестфалем (1883) и А. Штрюмпелем (1898) было описано заболевание, которое по клиническому сходству с рассеянным склерозом получило название «псевдосклероз». Заболевание характеризовалось распространёнными, размашистыми, ритмичными непроизвольными движениями, повышением мышечного тонуса, амимией, дизартрией и выраженными психическими нарушениями вплоть до такого расстройства интеллекта, как слабоумие.
В дальнейшем оказалось, что прогрессивная лентикулярная дегенерация и псевдосклероз являются разными формами одного и того же заболевания, которое Галль (1921) назвал гепато-лентикулярной дегенерацией. Однако изменения в мозге при нём никогда не ограничиваются лентикулярными ядрами и нередко бывают даже сильнее выражены в других отделах мозга. Поэтому советский невропатолог Н. В. Коновалов в 1960 году предложил название «гепато-церебральная дистрофия». Он значительно расширил представления о патофизиологии, патогенезе и клинике этой болезни и выделил новые её формы.
Встречается в среднем в популяции 3:100000. Распространённость выше среди народностей где распространены близкородственные браки. Чаще болеют мужчины, средний возраст дебюта 11-25 лет. Для проявления заболевания имеют значение экзогенные воздействия, поражающие печень — интоксикация и инфекция.

Ген болезни Вильсона — Коновалова (ATP7B) расположен в длинном плече 13-й хромосомы (13q14.3). Ген кодирует P-тип АТФазы, которая транспортирует медь в жёлчь и включает её в церулоплазмин [1] . В 10 % случаев мутация не обнаруживается [2] .
Хотя описано почти 300 мутаций ATP7B, в большинстве популяций болезнь Вильсона возникает в результате небольшого количества мутаций, специфичных для этих популяций. Например, для западных популяций мутация H1069Q (замена гистидина на глутамин в позиции 1069 белка) присутствует в 37-63 % случаев заболевания, в то время как в Китае эта мутация очень редка и R778L (замена аргинина на лейцин в позиции 778) встречается чаще. Относительно мало известно о влиянии мутаций на течение заболевания, хотя по данным некоторых исследований мутация H1069Q предполагает более позднее начало неврологических симптомов [1] [3] .
Нормальные вариации в гене PRNP могут изменить течение болезни, увеличивая возраст появления заболевания и влияя на тип симптомов, которые развиваются. Этот ген кодирует прионный белок, который активен в головном мозге и других тканях, а также, как полагают, участвует в транспорте меди [4] .
У заболевания аутосомно-рецессивный тип наследования. То есть больной должен получить дефектный ген от обоих родителей (см. на рисунке). Люди только с одним мутантным геном называются носителями (гетерозиготы). У них могут возникать слабовыраженные нарушения метаболизма меди [5] .
Медь выполняет множество функций в организме. В основном она выступает в качестве кофактора для некоторых ферментов, таких как церулоплазмин, цитохром с-оксидаза, дофамин бета гидроксилаза, супероксиддисмутаза и тирозиназа [3] .
Медь всасывается из желудочно-кишечного тракта. Транспортный белок на клетках тонкой кишки CMT1 (англ. Copper Membrane Transporter 1) перемещает медь внутрь клеток. Часть меди связывается с металлотионеином, а другая — перемещается в сеть Гольджи с помощью транспортного белка ATOX1. В аппарате Гольджи в ответ на повышение концентрации меди фермент ATP7A (англ. Copper-transporting ATPase 1) высвобождает этот элемент через воротную вену в печень. В печёночных клетках белок ATP7B связывает медь с церулоплазмином и высвобождает его в кровь, а также удаляет избыток меди с выделяющейся жёлчью. Обе функции ATP7B нарушены при болезни Вильсона. Медь накапливается в ткани печени; церулоплазмин продолжает выделяться, но с недостатком меди (апоцерулоплазмин) и быстро разрушается в кровотоке [3] .
Когда меди в печени становится больше, чем белков её связывающих, происходит их окислительное повреждение за счёт реакции Фентона. Это приводит к воспалению печени, её фиброзу и в итоге к циррозу. Также из печени в кровоток выделяется медь, которая не связана с церулоплазмином. Эта свободная медь оседает по всему организму, особенно в почках, глазах и головном мозге.
Основную роль в патогенезе играет нарушение обмена меди, её накопление в нервной (особенно поражены базальные ганглии), почечной, печёночной ткани и роговице, а также токсическое повреждение медью данных органов. Нарушение метаболизма выражается в нарушении синтеза и снижении в крови концентрации церулоплазмина. Церулоплазмин участвует в процессе выведения меди из организма. В печени формируется крупноузловой или смешанный цирроз. В почках в первую очередь страдают проксимальные канальцы. В головном мозге поражаются в большей степени базальные ганглии, зубчатое ядро мозжечка и черная субстанция. Отложение меди в десцеметовой мембране глаза приводит к формированию кольца Кайзера-Флейшера.
Гепато-церебральная дистрофия начинается в детском или молодом возрасте и имеет хроническое прогрессирующее течение. Во многих случаях появлению симптомов поражения нервной системы предшествуют висцеральные расстройства в виде нарушения деятельности печени и желудочно-кишечных расстройств (желтуха, боли в правом подреберье, диспептические явления). Порой развивается выраженный гепато-лиенальный синдром.
Со стороны нервной системы на первый план выступают экстрапирамидные симптомы в виде мышечной ригидности, гиперкинезов и расстройств психики. Пирамидные симптомы могут быть, но чаще отсутствуют. Чувствительность обычно не расстроена.
Типичным симптомом болезни является кольцо Кайзера-Флейшера — отложение по периферии роговой оболочки содержащего медь зеленовато-бурого пигмента; оно более выражено при поздних формах заболевания. Иногда отмечается желтовато-коричневая пигментация кожи туловища и лица. Часты геморрагические явления (кровоточивость дёсен, носовые кровотечения, положительная проба жгута), мраморность кожи, акроцианоз. Капилляроскопия обнаруживает атонию капилляров и застойность кровотока. Отмечаются суставные боли, профузные поты, остеопороз, ломкость костей. Патология печени клинически выявляется примерно у 30 % больных, а в ряде случаев она может быть обнаружена только функциональными пробами, например пробой с нагрузкой галактозой, пробой Квинка, пробой Бергмана-Эльботта, бромсульфофталеиновой пробой; количество билирубина в крови и уробилина в моче обычно увеличено; изменены осадочные реакции Таката-Ара и Грея, обычны лейкопения, тромбоцитопения, гипохромная анемия.
Распознают 5 форм гепато-церебральной дистрофии:
Брюшная форма— тяжёлое поражение печени, приводящее к смерти раньше появления симптомов со стороны нервной системы; заболевают дети. Её продолжительность от нескольких месяцев до 3-5 лет.
Ригидно-аритмогиперкинетическая, или ранняя форма отличается быстрым течением; начинается также в детском возраста. В клинической картине преобладают мышечная ригидность, приводящая к контрактурам, бедность и замедленность движений, хореоатетоидные или торсионные насильственные движения. Характерны дизартрия и дисфагия, судорожный смех и плач, аффективные расстройства и умеренное снижение интеллекта. Заболевание длится 2-3 года, заканчивается летально.
Дрожательно-ригидная форма встречается чаще других; начинается в юношеском возраста, течёт медленнее, порой с ремиссиями и внезапными ухудшениями, сопровождающимися субфебрильной температурой; характеризуется одновременным развитием тяжёлой ригидности и дрожания, дрожание очень ритмичное (2-8 дрожаний в секунду), резко усиливается при статическом напряжении мышц, движениях и волнении, в покое и во сне исчезает. Иногда обнаруживаются атетоидные хореоформные насильственные движения; наблюдаются также дисфагия и дизартрия. Средняя продолжительность жизни около шести лет.
Дрожательная форма начинается в возраста 20-30 лет, течёт довольно медленно(10-15 лет и больше); дрожание резко преобладает, ригидность появляется лишь в конце болезни, а порой наблюдается гипотония мышц; отмечается амимия, медленная монотонная речь, тяжёлые изменения психики, часты аффективные вспышки. Наблюдаются эпилептиформные припадки.
Экстрапирамидно-корковая форма встречается реже других форм. Типичные для гепато-церебральной дистрофии нарушения в дельнейшем осложняются апоплектиформно развивающимися пирамидными парезами, эпилептиформными припадками и тяжёлым слабоумием (обнаруживаются обширные размягчения в коре больших полушарий). Длится 6-8 лет, заканчивается летально.
В головном мозге при гепато-церебральной дистрофии размягчается чечевицеобразное ядро, особенно скорлупа, с образованием мелких кист. Поражаются и другие образования: хвостатое ядро, глубокие слои коры, мозжечок, в частности зубчатые ядра, подбугорные ядра; в остальных отделах головного мозга изменения выражены меньше.
Все изменения делятся на ангиотоксические и цитотоксические. Первые выражаются в атонии сосудов, особенно мелких, и изменении их стенок. В результате возникают стазы, распространённый периваскулярный отек с аноксией нервной ткани и её гибелью; часты геморрагии и следы их в виде скоплений гемосидерина.
Цитотоксический компонент заключается в распространённых дистрофических изменениях макроглии нервных клеток, часто заканчивающихся их гибелью. Характерно появление глии Альцгеймера, которая образуется из обычных астроцитов. Нередко встречаются изменённые нервные клетки, очень похожие на глию Альцгеймера; сходные клетки обнаруживаются также в печени и почках. В основе этих клеточных изменений лежит один и тот же фактор — однотипное нарушение клеточного обмена, вероятно, обмена нуклеиновых кислот.
Чем позднее начинается заболевание, тем медленнее оно протекает, тем более диффузны изменения в головном мозге и тем более цитотоксический компонент преобладает над ангиотоксическим. Печень вследствие атрофического цирроза уменьшена и бугристая; участки нормальной ткани чередуются с участками некротическими, дегенерирующими и с островками регенерации; обильное новообразование сосудов приводит к появлению анастомозов между ветвями воротной и нижней полой вены.
Поражение печени протекает по типу хронического гепатита либо цирроза и клинически характеризуется гепатомегалией, гемолитической анемией, тромбоцитопенией, лейкопенией. Также наблюдается поражение нервной системы (гиперкинезы, повышенный мышечный тонус иили параличи, атетоз, эпилептические припадки, слюнотечение, дизартрия, нарушения поведения, речи).
Также наблюдается почечный тубулярный ацидоз — глюкозурия, аминоацидурия, фосфатурия, уратурия, протеинурия.
Течение прогрессирующее, с периодами ремиссий и обострений. Наибольшая летальность (50 %) отмечается при печёночной форме с массивным некрозом и гемолизом у детей до 6 лет. Смерть больных от неврологических нарушений при отсутствии лечения наступает через 5-14 лет. Основная причина при этом интеркуррентные заболевания или желудочно-кишечные кровотечения, портальная гипертензия
Основой диагностики является картина болезни. Диагноз заболевания подтверждается:
- Наличием кольца Кайзера-Флейшера или его «обломков».
- Снижение содержания меди в сыворотке крови ниже 80 мкг на 100 мл
- Снижение концентрации церулоплазмина ниже 20 мг на 100 мл
- Повышение экскреции меди с мочой более 100 мкг в сутки
Для диагностики используют:
- осмотр с помощью щелевой лампы (зелёное кольцо Кайзера-Флейшера на роговице у лимба)
- определение уровня церулоплазмина (типично снижение менее 1 мкмольл)
- определение уровня меди в сыворотке крови (снижение менее 9,4 мкмольл)
- определение меди в суточной моче (повышение более 1,6 мкмоль или 50 мкг в сутки)
- Диета № 5 — с ограничением меди до 1 мг в сутки — исключение шоколада, орехов, сухофруктов, раков, печени, цельной пшеницы.
- Препаратом выбора является купренил (пеницилламин), который эффективен в 90 % случаев. Д-пеницилламин или унитиол.
- Унитиол
- Витамин В6
Патогенетическое лечение при гепатолентикулярной дегенерации направлено на увеличение выведения меди из организма. Для этого применяются комплексоны (тиоловые соединения). Наиболее эффективным оказался пеницилламин. Его следует принимать постоянно по 1,5-2 г внутрь ежедневно.
Лечение пеницилламином сопровождается заметным улучшением состояния больных или даже приводит к полной ликвидации симптомов. Вполне удовлетворительные результаты получены и при применении унитиола.
- ^ 12 Ala A, Walker AP, Ashkan K, Dooley JS, Schilsky ML (2007). «Wilson’s disease». Lancet369 (9559): 397–408. DOI:10.1016/S0140-6736(07)60196-2. PMID 17276780.
- ^ Merle U, Schaefer M, Ferenci P, Stremmel W (2007). «Clinical presentation, diagnosis and long-term outcome of Wilson’s disease: a cohort study». Gut56 (1): 115–20. DOI:10.1136/gut.2005.087262. PMID 16709660.
- ^ 123 de Bie P, Muller P, Wijmenga C, Klomp LW (November 2007). «Molecular pathogenesis of Wilson and Menkes disease: correlation of mutations with molecular defects and disease phenotypes». J. Med. Genet.44 (11): 673–88. DOI:10.1136/jmg.2007.052746. PMID 17717039.
- ^ Grubenbecher S, Stuve O, Hefter H, Korth C (2006). «Prion protein gene codon 129 modulates clinical course of neurological Wilson disease». Neuroreport17 (5): 549–52. DOI:10.1097/01.wnr.0000209006.48105.90. PMID 16543824.
- ^ Roberts EA, Schilsky ML (2003). «A practice guideline on Wilson disease» (PDF). Hepatology37 (6): 1475–92. DOI:10.1053/jhep.2003.50252. PMID 12774027.
- Болезни нервной системы под ред. Н. Н. Яхно, Д. Р. Шультмана, П. В. Мельничука. Москва «Медицина» 1995.
- С. Д. Подымова. Болезни печени Руководство для врачей. Москва. Медицина, 1993 г.
- Н. П. Шабалов — Детские болезни, СпБ, 2000, стр. 550
- В. Л. Пайков, С. Б. Хацкель, Л. В. Эрман — Гастроэнтерология детского возраста, СпБ, 1998, стр.198-203
- И. А. Иванова-Смоленская «Болезнь Вильсона-Коновалова» Журнал «Нервы», 2006, № 4
Ссылки


Wikimedia Foundation . 2010 .
Смотреть что такое «Болезнь Вильсона» в других словарях:
болезнь Вильсона — болезнь Вильсона. См. гепато церебральная дистрофия. (Источник: «Англо русский толковый словарь генетических терминов». Арефьев В.А., Лисовенко Л.А., Москва: Изд во ВНИРО, 1995 г.) … Молекулярная биология и генетика. Толковый словарь.
болезнь Вильсона — гепато церебральная дистрофия НЗЧ, характеризующееся нарушением экскреции ионов меди с желчью и их включения в церулоплазмин, сопровождающимся циррозом печени и дистрофическими процессами в головном мозге; наследуется по аутосомно рецессивному… … Справочник технического переводчика
Болезнь Вильсона — Коновалова — Структура белка ATP7B, в гене которого у больных обнаруживаются мутации МКБ 10 … Википедия
Болезнь Вильсона-Коновалова — Кольцо Кайзера Флейшера у пациента с симптомами Болезни Вильсона Коновалова Болезнь Вильсона Коновалова гепато лентикулярная дегенерация, гепатоцеребральная дистрофия, болезнь Вестфаля Вильсона Коновалова) врожденное нарушение метаболизма меди,… … Википедия
болезнь Вильсона-Коновалова — hepato cerebral dystrophy гепато церебральная дистрофия, болезнь Вильсона Коновалова. НЗЧ, характеризующееся сочетанием цирроза печени и дистрофических процессов в головном мозге, обусловлено нарушением обмена белков (гипопротеинемия) и меди;… … Молекулярная биология и генетика. Толковый словарь.
Болезнь Вильсона, Болезнь Вильсона-Коновалова (Wilson’S Disease) — врожденное нарушение метаболизма меди, характеризующееся недостаточным содержанием в организме церулоплазмина (в норме образующего нетоксичное соединение с медью). Свободная медь может оседать в клетках печени, вызывая развитие желтухи и цирроза… … Медицинские термины
БОЛЕЗНЬ ВИЛЬСОНА, БОЛЕЗНЬ ВИЛЬСОНА-КОНОВАЛОВА — (Wilsons disease) врожденное нарушение метаболизма меди, характеризующееся недостаточным содержанием в организме церулоплазмина (в норме образующего нетоксичное соединение с медью). Свободная медь может оседать в клетках печени, вызывая развитие… … Толковый словарь по медицине
Болезнь Вильсона–Коновалова — См. Дистрофия гепатоцеребральная … Энциклопедический словарь по психологии и педагогике
Болезнь Менкеса — Восьмимесячный мальчик с болезнью Менкеса из сельской местности … Википедия
Болезнь Коновалова-Вильсона — Кольцо Кайзера Флейшера у пациента с симптомами Болезни Вильсона Коновалова Болезнь Вильсона Коновалова гепато лентикулярная дегенерация, гепатоцеребральная дистрофия, болезнь Вестфаля Вильсона Коновалова) врожденное нарушение метаболизма меди,… … Википедия
Патофизиология печени
В патогенезе поражений печени различной этиологии следует отметить две разновидности поражений:
1) Прямое повреждение печени этиологическим фактором (вирусы, химические вещества).
2) Иммунное повреждение печени вследствие развития аллергических реакций гуморального и клеточного типа.
Следует отметить наиболее общие закономерности в патогенезе печеночной патологии:
1) Определенная последовательность патологических процессов в печени: первичное нарушение обмена веществ в печени (гепатоз)- гепатит — цирроз.
2) Поражение печени довольно часто сочетается с поражениями других органов (гепатолиенальный, гепатоцеребральный, гепаторенальный и др. синдромы).
3) Все первичные и вторичные поражения печени сопровождаются функциональной недостаточностью ее. Высокая регенераторная способность печени снижает проявления этой недостаточности.
4) Печень активно включается в адаптивные реакции при заболеваниях различных органов и систем. В то же время функциональная недостаточность печени может усугубить печение патологического процесса в других органах, повлиять на эффективность лекарственной терапии.
Печеночная недостаточность — состояние, при котором функциональная деятельность печени не обеспечивает гемеостаз. В зависимости от основных патогенетических механизмов возникновения выделяют следующие виды ПН:
1) Печеночно — клеточную (при дистрофических и некротических поражениях гепатоцитов).
2) Экскреторную или холестатическую (в результате нарушения желчеобразовательной и желчевыделительной функций печени).
3) Сосудистую (при нарушении кровообращения в печени).
По клиническому течению различают острую и хроническую ПН.
Причины ПН объединяются в 6 групп:
1. Острый и хронический гепатиты, цирроз, первичные и метастатические опухоли печени.
2. Нарушение внутрипеченочной гемодинамики.
3. Заболевания, осложняющиеся развитием внепеченочного холестаза: желчнокаменная болезнь, опухоль общего печеночного или общего желчного протока, опухоль или стеноз фатерова соска, хронический панкреатит с обтурацией общего желчного протока, повреждение желчных протоков.
4. Отравления гепатотропными, токсическими веществами: фосфор, черыреххлористый углерод, тринитротолуол, свинец, хлороформ, яды грибов (строчки, бледная поганка), ряд лекарственных веществ (антибиотики, сульфаниламиды, противотуберкулезные и противодиабетические препараты).
5. Экстремальные воздействия на организм: травмы, ожоги, тяжелые оперативные вмешательства, сопровождающиеся образованием обширной раневой поверхности, массивным кровотечением, переливанием крови.
6. Заболевания других органов и систем — системные заболевания соединительной ткани, эндокринные, сердечно-сосудистые заболевания.
Наряду с этиологическими факторами особо выделяют факторы, провоцирующие развитие ПН, или усугубляющие ее развитие, течение. К ним относятся: злоупотребление алкоголем, лекарственные интоксикации, особенно большими дозами барбитуратов, наркоз, операции, нервные потрясения, желудочно-кишечные кровотечения, перегрузки пищевым белком, применение диуретических средств, острые нарушения кровообращения.
Патогенез хронической печеночно-клеточной недостаточности
При ПН нарушается обмен углеводов, жиров, белков. Глюкоза поступает в клетки печени в результате пассивной диффузии (в отличии от других тканей) и внутриклеточная концентрация глюкозы в печени соответствует ее концентрации в крови. Поэтому при поражении гепатоцитов глюкоза не утилизируется при повышении ее в крови и легко возникает гипергликимия. Снижается глюконеогенез, не образуется гликоген, т.е. исчезает депо глюкозы.
Нарушение метаболизма жиров, поступающих в печень с током крови приводит к ее инфильтрации избытком жиров и ее жировому перерождению. Нарушается и липогенез. В крови возникает избыток кетоновых тел, т.к. в пораж. печени окисления кетоновых тел не происходит. Нарушается синтез холестерина, фосфолипидов и липопротеидов. Нарушение синтеза альбуминов в печени приводит к снижению способности плазмы крови переносить жирные кислоты, освобождаемые из жировых депо, что приводит к накоплению триацилглицеринов в клетках печени и ее жировому перерождению.
Печень поддерживает постоянный уровень белков и свободных аминокислот в плазме. Снижение уровня дезаминирования приводит к повышению содержания свободных аминокислот в сыворотке крови и моче.
При печеночной недостаточности наиболее наглядно отмечается нарушение взаимодействия печени с другими органами.
Нарушения взаимодействия печени с другими органами
Взаимодействие печени с другими органами настолько тесное, что выделяют гепато-церебральный, гепато-пульмональный, гепато-ренальный и другие синдромы.
При острых и хронических заболеваниях печени могут поражаться все отделы нервной системы. Поражение мозга связывают с действием многих факторов: нарушением метаболизма аммиака, увеличением в крови аминокислот и продуктов их окисления (фенолов, индолов). Другие факторы, действующие на нервную систему будут изложены в разделе «Печеночная кома». Действие всех этих факторов на мозг связано с недостаточностью печени вследствие ее поражения, а также с образованием как естественных, так и искусственных (хирургических) обходных коллатералей из системы воротной вены в систему полых вен.
Имеет место тесное взаимодействие между этими двумя органами в норме и в патологии. Общими для печени и легких является барьерная функция, дезинтоксикация (индола, скотола, микробных токсинов), участие в межуточном обмене веществ (холестерина, полипептидов, кетоновых тел). При патологии печени за счет изменения хим. состава крови нарушается функция внешнего дыхания.
Печень и почки являются важнейшими органами экскреции со взаимодополняющими деятельность друг друга функциями. Нередко заболевание одного органа вовлекает в болезнь второй орган. При инфекционных желтухах часто отмечается поражение извитых канальцев почек, в моче обнаруживается белок, гиалиновые цилиндры. При циррозе печени отмечаются поражения клубочков нефрона. Повреждение нефрона происходит потому, что токсические вещества не обезвреживаются поврежденной печенью, поступают в большой круг кровообращения и почки.
Связь органов ЖКТ и печени особенно наглядно просматривается при ахолическом синдроме. При непоступлении желчи в кишечник в нем не активируется липаза, не эмульгируются жиры, не образуются растворимые комплексы желчных кислот с жирными кислотами. В связи с этим 70% жиров не переваривается, не всасывается и удаляется из организма с калом. Нарушается всасывание жирорастворимых витаминов (ретинола, токоферола, К). Без витамина К образуется протромбин, снижается свертывание крови. Отсутствие желчных кислот приводит к ослаблению тонуса и перистальтики кишечника.
Острая печеночная недостаточность
Это синдром, обусловленный токсическим поражением ЦНС и характеризующийся глубокими нервно-психическими нарушениями, судорогами, потерей сознания.
Этиология. Причиной ПК может быть любое заболевание печени, но чаще всего вирусный гепатит, токсическая дистрофия печени, цирроз, острое расстройство печеночного кровообращения, синдром
По патогенезу выделяют три разновидности печеночной комы:
Главным звеном в патогенезе печеночной комы является увеличение в крови содержания церебротоксических веществ, поступающих из кишечника в печень и не обезвреживаемых в ней при нарушении антитоксической функциии гепатоцитов или образующихся в печени при разрушении паренхимы.
К церебротоксичеиским веществам относятся прежде всего аммиак, наибольшее количество которого образуется в кишечнике из азотсодержащих соединений под влиянием ферментов кишечной палочки и протея. При патологии печени аммиак не включается в ней в орнитиновый цикл и не превращается в мочевину, а соединяется с альфа-кетоглутаровой кислотой, образуя глутаминовую кислоту и глутамин. Выключение альфа-кетоглутаровой кислоты из цикла трикарбоновых кислот влечет за собой снижение продукции АТФ и угнетение АТФ-зависимых реакций. Вследствие снижения энергетического обмена в нейронах нарушаются функции нервных клеток.
Кроме аммиака церебротоксическим действием обладают и другие вещества, образующиеся в кишечнике:
1) Белковые метаболиты (фенолы, индол, скатол, производные метионина).
2) Низкомолекулярные жирные кислоты (масляная, капроновая, валериановая)
3) Производные пировиноградной и молочной кислоты (ацетоин, бутиленгликоль).
Интоксикацию усиливают желчные пигменты. Токсически действует на клеточные мембраны свободный билирубин. При печеночной коме возникает нарушение белкового обмена. Оно выражается в дисбалансе аминокислотного содержания в крови: увеличение фенилаланина, триптофана, тирозина, метионина; уменьшение валина, лейцина. Это приводит к синтезу ложных нейромедиаторов (октопамина), которые вытесняют такие медиаторы, как норадреналин и допамин, перерывают передачу возбуждения в синапсах ЦНС.
Важнейшими звеньями в патогенезе печеночной комы является гипогликемия. Она возникает вследствие снижения гликонеогенеза в патологически измененных гепатоцитах и усиливает дефицит энергии в клетках мозга. Важным звеном в патогенезе ПК является гипоксия и сдвиги водно-электролитного обмена и кислотно-щелочного равновесия.
Изменение водно-электролитного обмена проявляется в развитии гипокалиемии. Она возникает вследствие вторичного гиперальдостеронизма, возникающего вследствие снижения метаболизма альдостерона в печени. Идет выход калия из клеток, в том числе и головного мозга и поступление ионов натрия ии водорода в клетки. В связи с нарушением обмена веществ в клетке, развивается ацидоз, а вне клетки — алкалоз. Эти изменения способствуют проникновению церебротоксических веществ в клетки мозга и усиливают их действие.
В связи с общей интоксикацией организма нарушается системная гемодинамика: снижается сердечный выброс, развивается артериальная гипотензия, падает объем циркулирующей крови. Нарушение в системе свертывания крови (дефицит протромбина, фибриногена) создает условия кровотечений, кровоизлияний. Возникает прогрессирующая общая гипоксия смешанного характера.
Портокавальная ПК встречается часто у больных с синдромом портальной гипертензии.
Портальная гипертензия — комплекс изменений, возникающих при нарушении оттока крови из системы воротной вены. Эти изменения сводятся к резкому повышению давления в системе воротной вены с замедлением тока крови, к возникновению спленомегалии, варикозного расширения вен пищевода, желудка и кровотечения из них, расширения вен передней брюшной стенки, асцита и др. По этиологии различают внутрипеченочную, внепеченочную, смешанную пор тальные гипертензии. Внепеченочная портальная гипертензия обусловлена врожденной патологией сосудов портальной системы, тромбозом воротной системы. Внутрипеченочная портальная гипертензия чаще обусловлена циррозом или опухолевыми процессами в печени.
Причина смешанной формы портальной гипертензии — цирроз печени с вторичным тромбозом портальной системы.
В образовании асцитической жидкости значительная роль принадлежит избыточному лимфообразованию в печени, усилению экстравазации в ее сосудах. Интенсивность экстравазации определяется также уменьшением онкотического давления плазмы вследствие гипопротеинемии. Интенсивность выхода жидкости из сосудов определяется также задержкой натрия (вторичный гиперальдостеронизм) и повышением осмотического давления в ткани печени за счет возрастания молярной концентрации в результате обменных нарушений, вызванных гипоксией.
ПРЕДМЕТЫ
«Dendrit» — портал для студентов медицинских ВУЗов, включающий в себя собрание актуальных учебных материалов (учебники, лекции, методические пособия, фотографии анатомических и гистологических препаратов), которые постоянно обновляются.
Токсический синдром
Токсический синдром у детей — тяжелая общая неспецифическая реакция организма ребенка раннего (грудного и ясельного) возраста на внедрение микробных токсинов или вирусов, а также на введение пищи, не соответствующей в качественном и количественном отношении данному состоянию организма.
Токсический синдром может возникать при самых разнообразных заболеваниях, наиболее часто при болезнях инфекционной природы — дизентерии, колиэнтерите, стафилококковом энтерите, сальмонеллезах, а также заболеваниях, не связанных с первичной инфекцией,— диспепсии (см.), наследственных болезнях обмена. С токсикозом часто протекают респираторные вирусные инфекции, пневмония, отиты и другие заболевания детей раннего возраста.
В основе токсического синдрома лежит нервнорефлекторная реакция на раздражение нервной системы, ее вегетативных отделов, бактериальными токсинами, вирусами, продуктами тканевого распада. Реакция эта не адекватна раздражителю и характеризуется как гиперергическая. В результате нейрогуморальных нарушений наступают патологические изменения в организме: спазм и расширение сосудов, увеличивается порозность их клеточных мембран, происходят диапедезные микро- и макрокровоизлияния (см. Диапедез), нарушается внутриклеточный солевой баланс. Токсический синдром может протекать с обезвоживанием (с эксикозом) и без обезвоживания организма ребенка.
Тяжесть клинической картины токсикоза с эксикозом связана с большой потерей воды и соли.
У ребенка может остро развиваться интоксикация, нарушиться гемодинамика и наступить шок. При этом клинически отмечают неподвижное лицо, застывший (без мигания), устремленный в пространство взгляд, глубоко ввалившиеся глаза, запавший большой родничок. Ребенок находится в сопорозном или коматозном состоянии (см. Сознание, расстройства). Относительные границы сердца уменьшены, пульс учащенный, тоны сердца глухие. Возможно развитие острой сердечной слабости. Рентгенологически отмечается вздутие легочной ткани.
Бурное развитие токсикоза с эксикозом сопровождается рвотой, поносом. Стул частый, кал жидкий, водянистый; каловые массы выделяются струей, примесь отделившегося эпителия придает им белесый вид. Развившееся обезвоживание сопровождается повышением температуры, большой потерей веса. Тургор тканей быстро понижается, кожа становится серовато-землистого цвета, сухая, морщинистая, легко собирается в складки. Мочеиспускание редкое, может быть олигурия. При прогрессировании заболевания наблюдаются пониженный или повышенный тонус мышц, подергивания лицевой мускулатуры, беспорядочные автоматические движения, конечности становятся синюшными и холодными.
Что такое гепато токсемический синдром?

Несколько лет назад видел в новостях, кажется по НТВ , как в Италии, человеку, у которого был рак печени в крайне тяжёлой стадии (насколько я помню, в ней было около 80 опухолей), вылечили печень новым способом: ему удалили печень, в течение года лечили её радиотерапией, потом пересадили обратно и больной вылечился. Помогите, пожалуйста, найти ссылку на этот сюжет, или подскажите, как можно найти клинику, где лечят печень таким образом (в России или за рубежом)
Такой диагноз папе подружки написали и выписали домой умирать((((. Хоть что это такое — в интернете найти не могу, там другие виды перечисляются.
Как и 50 лет назад, лечат по сути теми же методами, но требуют десятки тысяч евро (пожертвуйте на лечение ребенка). Мне не понятна стратегия излечения, но понятна стратегия выкачки денег.Господа химики, медики, стоят ли предлагаемые методы лечения тех денег? Ведь можно это поставить на поток не только в европе. Какого дьявола на людском горе делаются деньги?
«поток» — имею в виду те методы, которые используются. Аппаратуру китайцы сделают, хирурги найдутся, доноры костного мозга тоже, .
В словарях пишут, что «гепатотоксемия (hepatotoxeaemia; гепато- + греч. toxikon яд + haima кровь) наличие в крови токсических веществ, обусловленное нарушением антитоксической функции печени.» В медицине такой термин не употребляется в виду крайней размытости этого понятия.
Источники:
Болезнь Вильсона это
Болезнь Вильсона это: Болезнь Вильсона — Коновалова ( гепатоцеребральная дистрофия , гепатолентикулярная дегенерация , болезнь Вестфаля — Вильсона — Коновалова
http://dic.academic.ru/dic.nsf/ruwiki/815522
Патофизиология печени
Патофизиология печени
http://dendrit.ru/page/show/mnemonick/patofiziologiya-pecheni
Токсический синдром
Токсический синдром Токсический синдром у детей — тяжелая общая неспецифическая реакция организма ребенка раннего (грудного и ясельного) возраста на внедрение микробных токсинов или вирусов, а
http://www.medical-enc.ru/18/toxic-syndrome.shtml
Что такое гепато токсемический синдром
что такое гепато токсемический синдром? Несколько лет назад видел в новостях, кажется по НТВ , как в Италии, человеку, у которого был рак печени в крайне тяжёлой стадии (насколько я помню, в
http://rak.moi-vopros.ru/answer/256633/chto-takoe-gepato-toksemicheskiy-sindrom
Source: medtechdom.ru
Источник: gepasoft.ru
Метаболизм токсичных веществ
Печень является одним из органов, принимающих участие в преобразовании и экскреции токсиканта.
Превращение химических веществ состоит из двух этапов:
- образование промежуточного продукта;
- образование конъюгата, удобного для экскреции.
В ходе первого этапа метаболизма гепатотоксические препараты и вещества присоединяют к себе полярную функциональную группу, что делает их более водорастворимыми. Далее происходит конъюгация полученных соединений с эндогенными молекулами, после чего возникшие полярные соединения захватываются гепатоцитами и с помощью мультифункциональных транспортных белков выделяются в желчь. После этого токсикант попадает в кишечник и выводится со стулом.
В процессе преобразования токсичность ксенобиотиков может изменяться. Одни вещества нейтрализуются и становятся безвредными, опасные свойства других только увеличиваются. В некоторых случаях активные метаболиты становятся инициаторами патологического процесса или изменяют тип негативного воздействия.
Гепатотоксические вещества наиболее сильно влияют на ткани печени. В процессе их превращения гепатоциты подвергаются крайне негативному воздействию. При этом может нарушаться функция как самих клеток органа (воздействие на клеточном уровне), так и механизмов выделения желчи (функциональные нарушения).
Основные виды воздействия
Токсическая гепатопатия может проявляться в цитотоксической или холестатической форме.
Цитотоксическое воздействие может иметь следующие проявления:
- Стеатоз (токсический гепатоз) – жировое перерождение гепатоцитов, накопление в них избыточного количества липидов. Одно из первых проявлений токсического воздействия химических веществ. Как правило, развивается при регулярном приеме этилового спирта, стероидных гормонов, тетрациклина. Причиной стеатоза является нарушение липидного обмена в клетках органа, а также усиленное поступление в печень жирных кислот.
- Некроз – отмирание клеток печени. Развивается под воздействием ацетоминофена, четыреххлористого углерода. Может носить фокальный или тотальный характер. В первом случае поражается ограниченный участок органа, во втором – весь или почти весь его объем.
- Фиброз – формирование в печени коллагеновых тяжей взамен здоровых тканей. При этом нарушается печеночный кровоток, процесс отделения желчи. Одним из веществ, вызывающих фиброз, является трихлорэтан.
- Токсический гепатит – воспаление печеночных тканей, являющееся результатом раздражающего действия ядов.
- Цирроз – структурно-функциональные изменения в печени, вызванные воздействием токсиканта и сопровождающиеся формированием фиброзных септ, узлов регенерации и перестройкой сосудистой системы.
- Канцерогенез – малигнизация гепатоцитов с формированием злокачественной опухоли. Развивается на фоне цирроза при регулярном употреблении этилового спирта, метотрексата, мышьяка (см. Отравление мышьяком – чрезвычайно опасно), диоксида тория.
Холестатические эффекты гепатотоксичных веществ проявляются в следующих формах:
- Нарушение секреции желчи за счет блокирования механизмов ее образования.
- Нарушение оттока желчи вследствие закупорки желчевыводящих протоков, снижения их тонуса или дисфункции микроворсинок.
В отличие от цитотоксических эффектов, гепатотоксические реакции холестатического типа обычно являются обратимыми. Функция печени, желчного пузыря и желчевыводящих путем восстанавливается через некоторое время после окончания действия токсиканта.
Интересно знать: гепатотоксический эффект развивается и при некоторых аллергических реакциях. При этом происходит формирование эозинофильного инфильтрата в тканях печени. Патология возникает через 1-5 недель после повторного контакта с аллергеном.
Клинические проявления гепатотоксических процессов
Клиническая картина при токсических поражениях гепатоцитов зависит от конкретной разновидности патологического процесса и тяжести его течения. Помимо этого, имеет значение степень поражения органа и длительность заболевания.
Стеатоз
Стеатоз является одной из наиболее безопасных форм поражения печени. Отличается стабильным течением и отсутствием выраженной клинической картины. У пациентов, страдающих токсическим гепатозом, врач отмечает тяжесть в области больного органа, слабую тянущую боль после физических нагрузок и обильной еды, повышенную утомляемость, тошноту, слабость.
При объективном обследовании у пациентов выявляют слабо выраженную гепатомегалию, яркость печеночной ткани вследствие ее жировой диффузной инфильтрации. Клиника усиливается при развитии стеатогепатитов (воспалительный процесс) и фиброзных изменений. При продолжающемся поступлении токсиканта в печень возможен переход стеатоза в цирроз.
Некроз
Первичными симптомами развивающегося некроза печеночной ткани и фокального некроза является:
- тошнота;
- рвота;
- горечь во рту;
- боль в подреберье справа;
- желтуха.
По мере развития процесса усиливается и симптоматика болезни. Гепатотоксичные препараты, вызывающие некроз печени, являются причиной развития острой печеночной недостаточности, печеночной энцефалопатии, комы и смерти пациента.
До момента впадения в кому у больного отмечается неадекватное поведение, тремор конечностей, боли усиливаются и начинают иррадиировать в поясницу. Развивается отек печени, орган увеличивается в размерах и начинает сдавливать окружающие ткани. Вследствие накопления в организме токсических продуктов метаболизма происходит раздражение тканей головного мозга, что приводит к его отеку.
Фиброз
На начальной стадии формирования коллагеновых тяжей у больного отмечается повышенная утомляемость, неспособность переносить высокие психологические и физические нагрузки, общее ухудшение самочувствия. Далее клиника прогрессирует.
У пациента снижается уровень иммунной защиты, формируются сосудистые звездочки на коже, развивается анемия. Отмечаются нарушения пищеварительных процессов.
Диагноз ставится на основании данных УЗИ, гастроскопии, копрограммы. Ультразвуковое исследование позволяет выявить наличие тяжей. При гастроскопии становятся видны расширенные вены пищевода. Данные копрограммы свидетельствуют о снижении качества переработки пищи и наличии в каловых массах ее непереваренных остатков.
Токсический гепатит
Токсический гапатит развивается внезапно. Начало болезни характеризуется повышением температуры тела до 38˚С и выше, признаками интоксикации, выраженными болями в правом подреберье. Далее у пациента отмечаются сосудистые нарушения, появление на коже точечных кровоизлияний, нарушения свертываемости крови. Возможны кровотечение из носа, десен, незаживших дефектов кожи.
В тяжелых случаях у больного развивается желтуха. Кал приобретает светлый оттенок, моча по цвету напоминает темное пиво. Возможно развитие явлений токсической энцефалопатии.
Подобные пациенты не осознают окружающей действительности, не отдают себе отчета в своих действиях, агрессивны и неадекватны. Инструкция по оказанию помощи требует производить мягкую фиксацию больных с токсической энцефалопатией к кровати.
Цирроз
Пациенты с циррозом печени, длительно употреблявшие гепатотоксичные вещества, отмечают у себя повышенную утомляемость, нервозность. Объективно у них выявляется наличие сосудистых звездочек, ладонной эритемы. Склеры иктеричны, присутствует желтуха, зуд кожи, периодически возникают носовые кровотечения.
По данным УЗИ печень таких больных увеличена и выступает за край реберной дуги на 1-2 сантиметра. Также отмечается увеличение селезенки. Температура тела может быть нормальной или повышенной до субфебрильных значений. В некоторых случаях гепатоспленомегалия не развивается.
Рак
Первая стадия болезни протекает бессимптомно. Однако рак быстро прогрессирует, поэтому уже через 3-4 недели от начала заболевания печень больного увеличивается в размерах, возникают первые симптомы ее поражения:
- горечь во рту;
- боли в правом подреберье;
- желтуха;
- кровоточивость;
- нервозность;
- тремор конечностей;
- сосудистая сеточка на коже;
- нарушение пищеварения.
По мере развития опухоли усиливается и симптоматика. К имеющимся признакам присоединяется асцит, обтурация желчевыводящих путей, признаки нарушения кровоснабжения печени. Пациент истощен, быстро худеет, отказывается от пищи.
Если сравнить фото таких людей до и после начала болезни, становится заметно, как сильно они потеряли в весе за короткий промежуток времени. При наличии метастазов к имеющейся клинической картине присоединяются признаки поражения других органов и систем.
На заметку: рак печени – практически неизлечимая патология, которая в течение короткого времени приводит к смерти пациента. Современные методы цитостатической терапии позволяют несколько продлить жизнь человека, однако пятилетний порог выживаемости достигается не более чем 60% подобных пациентов.
Принципы лечения
В основе терапии патологии лежит прекращение действия токсиканта. Уже одна эта мера позволяет улучшить прогноз по заболеванию.
Например, по данным второго тома монографии «Внутренние болезни» под авторством профессора и академика РАН Н.А. Мухина, пятилетняя выживаемость пациентов с алкогольным циррозом составляет 30%, если они продолжают употреблять спиртное, и 70% — если отказываются от алкогольных напитков.
Помимо алкоголя, следует прекратить принимать гепатотоксичные антибиотики, к числу которых относят:
- амоксиклав;
- оксациллин;
- рифампицин.
При необходимости проведения антибактериальной терапии больному должны быть назначены не гепатотоксичные антибиотики, метаболизм которых происходит без участия печени:
- цефдинир;
- цефуроксим;
- цефалексин.
Помимо отказа от использования печеночных токсинов, имеет значение диета. При болезнях печени рекомендуется питание повышенной калорийности (до 3000 ккал/сут).
При этом количество белка и витаминов в пище должно быть повышено, жиров – понижено. Допустимо использовать высокобелковые энтеральные смеси типа «Nutrison protison» или «Nutrison energy», однако их цена достаточно высока (около 800 рублей за 1 литр продукта).
Лекарственная терапия зависит от вида патологии. Основные схемы лечения приведены в нижеследующей таблице:
Прогнозы
Прогнозы по токсическим гепатопатиям напрямую зависят от тяжести течения болезни, разновидности воздействия, наличия или отсутствия продолжающегося действия токсиканта. Фиброз и стеатоз – обратимые процессы. Прогноз по ним благоприятен, если пациент соблюдает рекомендации по лечению и диету. Аналогично обстоят дела и с токсическими гепатитами.
Цирроз и рак печени имеют крайне неблагоприятные прогнозы. Огромное количество пациентов, страдающих этими заболеваниями, погибают через 2-3 года от начала процесса. Стремительный вариант течения может убить больного уже через несколько недель или месяцев.
Спасти жизнь пациента, страдающего циррозом, может пересадка печени. Однако выполнить эту операцию всем, кто в ней нуждается, невозможно в силу недостатка донорских органов и высокой стоимости подобного лечения.
При раке в стадии метастазирования пересадка не имеет смысла. Несколько замедлить рост опухоли и продлить жизнь больного позволяет цитостатическая терапия. Однако и она носит лишь паллиативный характер. Подробнее узнать о том, что такое токсическое поражение печени и как оно проявляется можно из видео в этой статье.
Источник: Toksikolog.com

