Патофизиология
Развитие истинной аневризмы левого желудочка протекает в две основных фазы: ранней дилатации и позднего ремоделирования. Истинная аневризма левого желудочка (по крайней мере, в 88%) развивается обычно после трансмурального инфаркта миокарда вследствие тромбоза передней межжелудочковой ветви ( ПМЖВ) и недостаточного развития коллатерального кровообращения.
Фаза ранней дилатации у 50% пациентов начинается с момента инфаркта миокарда в течение 48 часов. У остальных пациентов формирования аневризмы происходит в течение 2 недель после инфаркта миокарда. В течение нескольких дней внутренняя поверхность развивающейся аневризмы теряет трабекулярность и становится гладкой, у 50% пациентов формируется тромб левого желудочка.
На 2-3 сутки в зону инфаркта происходит миграция лейкоцитов, что приводит к лизису некротических миоцитов на 5-10 день после инфаркта. В результате разрушения коллагена и миоцитов прочность стенки миокарда к этому времени значительно снижается и возможен разрыв миокарда. Сохранение гибернирующего миокарда в периинфарктной зоне обязательное условие предотвращения развития истинной аневризмы левого желудочка.
Потеря систолической активности в инфарцированной зоне при сохранении сократительной способности в окружающем миокарде вызывает систолическое выпячивание утончение региона миокарда. Согласно закону Лапласа (T = Pr/2h), при постоянном давлении в левом желудочке (P), увеличении радиуса искривления (r) и уменьшении толщины стенки левого желудочка (h) в инфарктной зоне увеличивается напряжение стенки (T).
По отношению к нормальному поврежденный (инфарцированный) миокард более пластичен и подвержен деформации. Таким образом, увеличенное систолическое и диастолическое напряжение стенки левого желудочка приводит к прогрессивному расширению инфарктной зоны, пока формирование рубца не уменьшает пластичность области аневризмы.

Вследствие роста диастолического напряжения и преднагрузки, а также увеличения уровня эндогенных катехоламинов, непораженные области миокарда вынуждены развивать усиление сокращения, что приводит к гипертрофии миокарда. Это в свою очередь вызывает рост потребления кислорода здоровыми отделами миокарда и левого желудочка в целом.
В дополнение к этому при формировании аневризмы происходит снижение ударного объема, так как часть его выбрасывается не в аорту, а в аневризму. Чистая механическая эффективность левого желудочка (внешняя ударная работа минус миокардиальное потребление кислорода) снижается, уменьшая внешнюю ударную работу и еще более увеличивая миокардиальное потребление кислорода.
Аневризма левого желудочка вызывает не только систолическую, но и диастолическую дисфункцию желудочка. Диастолическая дисфункция является следствием увеличенной жесткости фиброзной аневризматической стенки, которая препятствует диастолическому заполнению и увеличивает конечно-диастолическое давление левого желудочка.
Начинается спустя 2-4 недели после инфаркта миокарда, когда появляется высоко васкуляризированная грануляционная ткань, которая замещается через 6-8 недель волокнистой фиброзной тканью. Аритмии, типа желудочковой тахикардии могут развиться в любое время развития желудочковой аневризмы, так как в области периинфарктной зоны развиваются микроочаги re entry.
Терапия нитратами в течение только 2 недель после инфаркта не предотвращает формирование аневризмы. До настоящего времени неясна роль ингибиторов ангиотензин-конвертирующего фермента поскольку они подавляют развитие желудочковой гипертрофии. Реваскуляризация миокарда улучшая коронарную перфузию и перемещение фибробластов в инфарктную область миокарда, является хорошим профилактическим фактором развития аневризм левого желудочка. Применение стериодов, наоборот, может увеличить вероятность формирования аневризмы.
Несмотря на значительные достижения в молекулярной, биомеханической, генетической, нейро-гуморальной и фармакологической областях, понимания строения и функции кардиомиоцита, не следует, однако, забывать тот фундаментальный факт, что высокоспециализированные клетки могут эффективно функционировать лишь в окружении коллагенового остова, который не только располагает их друг относительно друга, но и связывает кардиомиоциты.
Таким образом, создается совокупность морфологических единиц, способных к генерации силы в пределах определенного структурного расположения – мышечной ленты, и к трансформации простого укорочения сократительных единиц в механически эффективное сокращение и расслабление спиральной структуры целого миокарда левого желудочка сердца.
Любое улучшение функции миоцитов в отсутствие адекватного коллагенового каркаса, и, соответственно, улучшение систолической и диастолической функции всего сердца, невозможно. Существует общепринятое мнение, что коллаген играет важную роль в поддержке размеров и формы сердца, а также в постинфарктном ремоделировании.
Он составляет от 1% до 4% всех сердечных белков. Коллагеновые волокна – это надмолекулярные образования, которые состоят из молекул коллагена, уложенных зигзагообразно и перекрещенных для увеличения прочности. Внеклеточный матрикс представлен вязкоупругим окружением из коллагена типа I и III, который связывает миоциты, определяет взаимодействие между миофиламентами и поддерживает взаимоотношение капилляров и миоцитов.
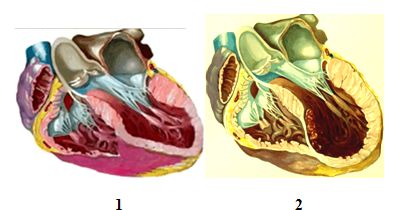
Коллагеновый остов состоит из сети миофибрилл и межклеточных «распорок», которые связывают соседние миоциты, что позволяет миофибриллам оптимизировать развитие мышечного усилия, распределить его внутри желудочковых стенок и предотвратить деформацию саркомеров. Внутри вышеописанной структуры межклеточное пространство заполнено протеогликанами.
Ремоделирование миокарда представляет адаптивный ответ сердца на длительное воздействие физиологических и патогенных факторов. При этом изменяется структура миоцитов и внеклеточного матрикса. Уменьшение перекрестных связей миокардиального коллагена было показано на животных моделях. Так как структурная поддержка, которая обеспечивается фибриллярным внутриклеточным коллагеном, является важной детерминантой формы миоцита и распределения масс, а также составляющей превращения сокращения миоцита в общий сердечный выброс, то ее потеря, из-за деградации зрелого коллагена с заменой его на вновь синтезированный со сниженным количеством перекрестных связей, может непосредственно влиять на систолическую дисфункцию и расширение полостей сердца.
Изменения внеклеточного матрикса необходимы для формирования нового устройства камер сердца. Развитию фиброза, а именно увеличения количества белков внеклеточного матрикса – коллагена I и III типов, обязательно должна предшествовать деструкция коллагеновой сети. Коллаген I типа принимает участие в формировании внеклеточного матрикса фазу позднего ремоделирования, в то время как коллаген III типа – в фазу ранней экспансии.
Всякое изменение внеклеточного матрикса по сути своей означает нарушение баланса между скоростями синтеза и распада белка. Будучи организованным в фибриллярную форму, внеклеточный коллаген является крайне устойчивым к разрушению протеазами, за исключением специфических коллагеназ – матриксных металлопротеиназ (ММП), основным источникам которых в сердце являются фибробласты.
Изменения в структуре коллагена, его распределение в процессе ремоделирования зависит от регуляции ММП на трех уровнях: транскрипции, активации и ингибирования тканевыми ингибиторами металлопротеиназ (TИMMП). TИMMП представляют собой низкомолекулярные белки, которые имеют высокое сродство к каталитическому домену ММП.
Таким образом TИMMП нейтрализуют деградацию коллагена. Гены, кодирующие ММП и ТИММП, расположены совместно и совместно же экспрессируются. Данная система индукции/активации ММП была найдена в сарколемме миоцитов. Она некорректно работает у пациентов с ишемической кардиомиопатией. Коллагеназы могут быть активированы посредством множества механизмов, включая фактор некроза опухолей – альфа (альфа-ФНО), свободные радикалы, инсулино-подобный фактор роста-1, трансформирующий фактор роста-1, который стимулирует пролиферацию фибробластов, катехоламины – то есть все факторы, которые имеют место при ишемии.
Одним из эндогенных активаторов ММП может являться химаза (единственный фермент в ткани миокарда, конвертирующий ангиотензин I в ангиотензин II), повышенный уровень которой определялся при состояниях перегрузки давлением или объемом. Один из донаторов сульфгидрильных групп – окисленный глутатион, встречающийся в зоне миокардиальной ишемии, – тоже активирует латентные коллагеназы и вызывает быстрое разрушение коллагеновых мостиков в «ошеломленном» миокарде и в зоне инфаркта в течение 2-3 часов после окклюзии артерии, когда еще не развивается воспалительный инфильтрат.
Местный синтез альдостерона миофибробластами вызывает аутокринную стимуляцию системы ренин-ангиотензин-альдостерон. Вместе с ангиотензином II и предсердным натрийуритическим фактором альдостерон стимулирует трансляцию m-РНК коллагена I и III типов.
Еще одним моментом, требующего пристального внимания, является возможная обратимость ремоделирования внеклеточного матрикса. Недавние исследования показали, что длительное использование систем вспомогательного кровообращения обращает вспять сократительную дисфункцию и влияет на экспрессию генов на конечной стадии хронической сердечной недостаточности.
Также было отмечено улучшение эхокардиографических параметров. Таким образом становиться понятно, что прекращение действия фактора, нагрузки, запускающего патологическое ремоделирование и развитие сердечной недостаточности, может привести к обратному развитию структурных и архитектурных изменений. Так как основой активации и модуляции внутриклеточных цепных реакций является механический стресс, то уменьшение последнего, соответственно, достижение контроля над экспрессией и активностью ММП, возможно лишь при использовании объем-редуцирующей хирургии и модификации желудочковой геометрии.
Симптомы, связанные с акинезией
- Трудности при ходьбе;
- Мышечная скованность, которая начинается в шее и ногах. Мышцы на лице могут стать жесткими, похожими на маску;
- Неспособность правильно передвигать ноги, особенно при повороте или приближении к месту в покое;
- Скованность мышц;
- Постуральная нестабильность.
Но человек может испытывать акинезию без каких-либо основных признаков болезни Паркинсона.
Естественное течение
Относительно новые исследования выявили 47-70% 5-летнюю выживаемость пациентов с аневризмами левого желудочка. Причины смерти включают аритмию в 44%, остановку сердца – 33%, инфаркт миокарда – 11% и несердечные причины – 22%.
Факторами, влияющим на выживаемость являются возраст, степень коронарной болезни, продолжительность стенокардии до предшествующего инфаркта, ишемическая митральная недостаточность, желудочковые аритмии, размер аневризмы, сократительной функции жизнеспособного миокарда, КДД левого желудочка. Раннее развитие аневризмы в течение 48 часов после инфаркта также уменьшает выживаемость.
Риск томбоэмболии для пациентов с аневризмами низок (0,35% пациенто-лет), и постоянный прием антикоагулянтов обычно не рекомендуется. Однако у 19% пациентов с видимыми эхокардиографически тромбами после инфаркта миокарда отмечены эпизоды тромбоэмболии. Мерцательная аритмия и большой размер аневризмы – дополнительные факторы риска томбоэмболии.

Разрыв хронических псевдоаневризм левого желудочка встречается реже, чем можно было ожидать. Разрыв левых желудочковых псевдоаневризм может быть наиболее вероятным в острой фазе инфаркта миокарда или при их большом размере. Желудочковые псевдоаневризмы имеют тенденцию вести себя подобно истинным аневризмам.
Гипокинезия, как основной синдром паркинсонизма
Гипокинетический синдром проявляется при паркинсонизме как в конечностях, так и в теле.
Это все вышеназванные разновидности расстройства двигательных функций на фоне пластической гипертонии мышц, включая парадоксальные движения, паллидарный тремор, микрографический почерк, феномены «позы восковой куклы» и «зубчатого колеса», при ходьбе – заносы тела в сторону с падениями, паркинсоновское топтание на месте, ахейрокинез.
Характерна поза с наклоном головы и корпуса вперёд с касанием груди подбородком, с руками, прижатыми к корпусу, согнутыми в лучезапястных и локтевых сочленениях, со сгибанием пальцев в пястно-фаланговых и разгибанием в межфаланговых сочленениях, с оппозицией I пальца остальным пальцам кисти, с ногами, слегка приведенными и полусогнутыми в коленях.
Гипертонус шеи заставляет больного разворачиваться на зов всем туловищем либо максимально поворачивать глаза, при этом голова остается неподвижной.
Расстроена также моторика мышц, обеспечивающих живость мимики, отсюда маскообразность лица (гипомимия) с практически немигающим взглядом, монотонность тихого голос ввиду затруднений с артикуляцией речи (гипофония).
Особенностью гипокинезии при паркинсонизме (помимо сохранения мускульной силы) является ее сочетание с высокой степенью ригидности мышц.
В отличие от спастичности ригидность проявляется:
- положительным симптомом «свинцовой трубочки» (равномерностью мышечного воскообразного сопротивления, как при сгибании свинцовой трубочки) – спастичная мускулатура отвечает феноменом отдачи и «складного ножа»;
- неизменностью сухожильных рефлексов – при спастичности они возрастают.
Иллюстрацией ригидности служит симптом «зубчатого колеса», не свойственный спастичности.
Схожесть двигательных расстройств делает больных паркинсонизмом схожими друг с другом, отличающимися только выражением взгляда.
Последовательность деформирования при акинезии плода включает в себя тип акинезии, которая вызывает сочетание патологии в утробе матери, когда ребенок развивается. Примеры таких симптомов:
- Различные контрактуры;
- Лицевые аномалии;
- Внутриматочное ограничение роста;
- Гипоплазия (недоразвитие) легких.
Примерно 30% детей с последовательностью деформации при акинезии плода рождаются мертвыми. Другие не могут долго жить из-за проблем, связанных с гипоплазией легких.
Клиническая картина
Стенокардия наиболее частое клиническое проявление у большинства пациентов аневризмой левого желудочка, так как более 60% из них имеют многососудистое поражение. Одышка – второй по частоте симптом. Она характерна для пациентов, когда в инфаркт миокарда вовлекается более 20% массы миокарда левого желудочка.
Диагностика
На электрокардиограмме присутствует зубец Q и подъем сегмента ST. Рентгенограмма грудной клетки может выявить увеличение тени сердца, что не является патогномоничным для аневризмы левого желудочка. Левая вентрикулография до недавнего времени была золотым стандартом для установления диагноза аневризмы левого желудочка.
Двумерная эхокардиография – также чувствительный метод для диагностики аневризм, позволяющий не только выявить саму аневризму, но и наличие в ней тромба, а также рассчитать по сегментам локальную и глобальную фракцию выброса. Стресс ЭхоКГ дополнительно способна определить наличие и объем гибернирующих участков миокарда.
Факторы риска акинезии
Болезнь Паркинсона — заболевание, при котором происходит снижение продукции дофамина головным мозгом, что влияет на способность человека контролировать свои мышцы.
Лекарственный паркинсонизм — развивается в результате того, что человек принимает слишком много препаратов, которые ингибируют дофамин.
Прогрессирующий супрануклеарный паралич — это состояние, постепенно повреждающее мозг, при этом сначала нарушается баланс во время ходьбы.

Гормоны — гипотиреоз или низкие уровни гормонов щитовидной железы могут привести к акинезии.
У людей с болезнью Паркинсона мужчины чаще страдают акинезией, чем женщины.
Другие факторы риска:
- брадикинезия или замедленное движение мышц;
- болезнь Паркинсона, которая продолжается в течение длительного времени;
- постуральная нестабильность;
- проблемы с ригидностью мышц.
Техника операции
Вследствие относительно хорошего прогноза для бессимптомной левожелудочковой аневризмы показания к операции относительны. Однако, у больных, подвергающихся АКШ необходимо восстановить геометрию левого желудочка. С другой стороны, для симптоматических (аритмии, стенокардия, застойная сердечная недостаточность) пациентов, операция предлагает лучший результат, чем медикаментозная терапия.
Оперативное лечение абсолютно показано больным с дискинетическими (акинетическими) аневризмами при увеличении конечно-систолического индекса {amp}gt; 80 мл/м2 и конечно-диастолического индекса {amp}gt; 120 мл/м2 ) , а также угрозе разрыва или развития ложной аневризмы, точно так же как и при врожденных аневризмах левого желудочка.
Согласно последним исследованиям, миокард представляет мышечную ленту, завернутую в спираль с определенным углом. Межжелудочковая перегородка состоит из трех мышечных слоев и вносит колоссальный вклад в выброс и присасывание крови. Диастола, как и систола, обеспечивается активным мышечным сокращением.
Принимая во внимание описанные выше патологические изменения, вызванные постинфарктной аневризмой, становится ясно, что ее пластика является патогенетически оправданной. Теоретически, такой подход обеспечит снижение напряжения в стенке левого желудочка и снижение потребности миокарда в кислороде (на основании закона Лапласа), нивелирует перегрузку объемом и переориентирует направление мышечных волокон в более физиологическую сторону с усилением механической эффективности выброса и присасывания.

Исключение из сокращения нефункционирующих сегментов и восстановление правильной ориентации миофибрилл может повысить коэффициент полезного действия базальных и средних сегментов интактного миокарда. В этой связи важным моментом операции является формирование левого желудочка в виде «готической», а не «романской» арки.
Относительные противопоказания к операции включают чрезмерный риск анестезии, отсутствие жизнеспособного миокарда вне аневризмы, низкий ({amp}lt; 2,0 л•мин/м2) сердечный индекс, выраженная митральная недостаточность. Глобальная фракция изгнания может быть менее полезной для оценки показаний к операции, чем сегментарная фракция изгнания оставшейся части миокарда левого желудочка.
Ангиопластика возможна только у пациентов с подходящей коронарной анатомией, одно- или двухсосудистом поражении и противопоказаниями к операции.
Выполняется стандартная срединная стернотомия. ИК осуществляется в режиме нормо- или умеренной гипотермии. Используется анте- и ретроградная кровяная кардиоплегия. Проводится внешняя ревизия левого желудочка для идентификации области рубца и утончения стенки. Разрез аневризмы выполняется вертикально, отступая влево от ПМЖВ на 1 см.
Выполняется резекция аневризмы по одному из методов, описанных ниже. Затем при необходимости проводится пластика или протезирование митрального клапана и полная реваскуляризация миокарда. Отключение аппарата ИК часто требует инотропной поддержки. Как правило, используется допамин (5 мкг/кг/мин.), а также нитроглицерин для предотвращения спазма коронарных артерий и нитропруссид натрия для снижения постнагрузки.

Дополнительная инотропная поддержка не увеличивает сердечный выброс и может привести к аритмии и тахикардии. Поскольку левый желудочек плохо растяжим, ударный объем фиксирован (КДО левого желудочка ≈ 150 мл), ЧСС 90-115 уд. в мин. достаточна, чтобы поддержать сердечный индекс {amp}gt; 2,0 л•мин/м2. Контрпульсация может также быть необходима у пациентов со сниженной контрактильностью миокарда.
Причины расстройств движения
Расстройства двигательной активности обусловлены расстройством функции мозговых структур, ответственных за динамику движения.
Так, наступление акинезии может быть следствием повреждения основания мозга либо его лобных долей по причине энцефалопатий, ассоциированных с:
- тяжелыми видами почечной (уремический кататонический синдром) либо печеночной недостаточности (печеночная депрессивная акинезия);
- патологией кроветворения (тяжелые вариации течения пернициозной и гемолитической анемии);
- болезнями системы дыхания (энцефалопатия на почве гипоксических расстройств).
Либо она может быть вызвана тяжелыми интоксикациями и нейроинфекциями.
Причиной гипокинезии может стать дисфункция структур, составляющих экстрапирамидную (строиопаллидарную) систему, в которую входят такие образования подкорки как паллидум и красные ядра – начало монаковского экстрапирамидного тракта, осуществляющего реализацию безусловных рефлексов, проводя импульсы от всех отделов большого мозга ниже коры к передним рогам мозга спинного.
В свою очередь, патологические изменения в экстрапирамидной системе могут быть спровоцированы различными психическими и неврологическими состояниями.
Гипокинезия может также стать следствием гиподинамии – недостатка движения либо дефицита мускульной активности локального характера с производством однообразных движений, не требующих высоких энергозатрат.
К тем же результатам приводят и хронические производственные и бытовые интоксикации и иные факторы.
Наиболее характерными являются симптомы гипокинезии при паркинсонизме.

Возможные причины акинезии включают:
- Аномалии развития нервной системы;
- Заболевания соединительной ткани, такие как хондродисплазии;
- Водянка плода;
- Заболевания матери или употребление наркотиков.
Любые изменения в утробе, которые вызывают недостаточный кровоток и уровень кислорода, могут привести к акинезии плода.
Врачи выделили две мутации генов, которые связаны с повышенными рисками для развития акинезии плода. Если у человека имеются родственники с патологией, то он должен провести тест на мутации генов DOK7 и RAPSN, которые связаны с акинезией.
Лечение
Лечение зависит от того, что вызывает симптомы акинезии. Например, при акинезии, связанной с препаратами, необходимо прекратить принимать лекарственные средства, которые вызывают проблему.
При болезни Паркинсона зачастую врачи назначают препараты, которые увеличивают количество дофамина в организме. Они могут помочь, поскольку снижение уровня дофамина вызывает нервно-мышечные симптомы, связанные с болезнью Паркинсона. Примеры таких препаратов включают леводопу и карбидопу, а также агонисты дофамина.

Люди с болезнью Паркинсона или другими расстройствами могут обратиться к врачу лечебной физкультуры, который поможет им научиться двигаться безопасно. В настоящее время нет лечения данного состояния.
В зависимости от спровоцировавшей расстройство причины лечение будет принципиально отличаться по применяемым методам.
При наличии опухоли мозга производится оперативное её иссечение, при факторе интоксикации (бытовой, производственной) необходимо принять меры по пресечению воздействия на организм токсического соединения.
Нейроинфекции лечатся применением медикаментов, эффективных в отношении вызвавшего патологию возбудителя, а последствия их воздействия устраняются использованием всего арсенала препаратов, которые улучшают кровоснабжение мозга и медикаментов-детоксикантов.
К превентивным мерам относятся мероприятия, направленные на недопущение в организм возбудителей нейроинфекций, предотвращение травм головы и риска токсического воздействия производственных и бытовых ядов.
Увеличение двигательной активности работниками умственного труда (предотвращение гиподинамии) также является существенной мерой предотвращения расстройств динамики движения.
Методы ремоделирования левого желудочка
После удаления тромбов аневризматическая стенка резецируется, оставляя 3 см края рубца, чтобы обеспечить реконструкцию нормального левожелудочкового контура. Проленом 2 на тефлоновых прокладках накладывается двухрядный (матрацный и обвивной шов) для герметизации полости левого желудочка.
Указанный способ применяется при небольших аневризмах верхушки левого желудочка. После вскрытия аневризмы по краю рубца накладывается кисетный шов 2 и затягивается. Проленом 2 на тефлоновых прокладках накладывается духрядный (матрацный и обвивной шов) для герметизации полости левого желудочка.

Нижние или задние аневризмы для сохранения адекватного объема полости левого желудочка обычно требуют пластики с помощью заплаты. После вскрытия аневризмы и дебридмента иссекается часть рубцовой ткани, оставляя 1 см от края здорового миокарда. Заплата из дакрона на 2 см больше в диаметре, чем отверстие в желудочке подшивается матрацными швами на прокладке, которые проводятся изнутри полости левого желудочка. Для дополнительной герметичности при необходимости первая линия шва дополняется вторам обвивным швом проленом 3.
В основном применяется при больших передних аневризмах левого желудочка. После вскрытия полости аневризмы и дебридмента по краю рубца накладывается кисетный шов 2 и затягивается. В дефект стенки обвивным швом 3 вшивается заплата (дакрон, ксеноперикард) 2х3 см для сохранения достаточного объема полости левого желудочка. Над заплатой простым линейным двухрядным швом сшиваются стенки аневризматического мешка.
Такой вид пластики полностью сохраняет ПМЖВ для шунтирования и исключает наличие внешнего протезного материала, вызывающего спаечный процесс в перикарде. Техника V.Door также позволяет исключить аневризматическую часть межжелудочковой перегородки и может использоваться при острых инфарктах миокарда с рыхлым краем аневризмы.
Описанные выше методы пластики аневризмы левого желудочка имеют ряд недостатков. Так при использовании линейной пластики левого желудочка формируется длинный и тонкий желудочек с нарушенной геометрией, исключается вмешательство на МЖП, а использование прокладок и сам рубец ведут к формированию своеобразной «распорки», которая существенно затрудняет сокращение. Методы A. Jatene и V.
Dor затрагивают лишь пораженный сегмент левого желудочка. A. Jatene отметил, что в некоторых случаях развивался синдром малого сердечного выброса и требовалось повторное вмешательство для увеличения объема камеры левого желудочка. M. Salati выявил развитие тяжелой диастолической дисфункции по рестриктивному типу у 8% пациентов.
V. Dor отметил, что хорошие непосредственные результаты в дальнейшем нивелировались развитием сердечной недостаточности за счет излишнего радикализма и значительного уменьшения ударного объема и диастолического наполнения, либо за счет избыточной заплаты и увеличения миокардиального стресса. В этой связи для оптимизации объема левого желудочка V.
Dor на основании изучения послеоперационных ангиограмм предложил использовать внутрижелудочковый баллон с объемом 60 мл/м2 как модель объема полости левого желудочка. Однако, такое значение может быть слишком маленьким для пациентов, у которых до операции сердце имеет значительные размеры, поэтому, если предоперационный индекс КДО {amp}gt; 150 мл/м2, то следует добавить 15% к вышеуказанной цифре (приблизительно 70 мл/м2).
В дальнейшем эта методика была развита L. Menicanti, который предложил использовать шаблон объема полости левого желудочка, представляющий собой модель левого желудочка различных типоразмеров в зависимости от площади тела пациента. После иссечения аневризмы и введения в полость левого желудочка системы, принципиальным моментом при закрытии дефекта является использование длинной и узкой заплаты (1×4 см, а не 2×3 см, как методом V. Dor).
Продольная ось вновь формируемой «шейки» при этом располагается под углом к оси вентрикулотомной раны. Фиксированная в таком положении заплата способствует восстановлению формы левого желудочка и правильной ориентации волокон миокарда. В дальнейшем, в 2002 году тот же автор предложил использовать пликацию задней стенки левого желудочка между основаниями сосочковых мышц с целью уменьшения их дисторсии и ликвидации митральной недостаточности.
В медицинской среде порой появляются противоречивые данные об оценке гипертрофии сердечной мышцы. Одни авторы расценивают ее как важный приспособительный механизм, другие утверждают, что гипертрофия опасна, поскольку является болезнью и всегда связана с патологией миокарда. Изучение причин и связи с биохимическими процессами на клеточном уровне позволило выделить стадии и формы гипертрофии.
Такое явление, как гипертрофия левого желудочка сердца, сопровождает множество заболеваний и хорошо известно врачам. Однако не секрет, что часто люди, занимающиеся физической работой и спортсмены с этим признаком живут без жалоб на сердечное здоровье до глубоко старческого возраста.
Что же такое гипертрофия? Как нужно относиться к этому симптому, если его выявили при обследовании?
Термин «гипертрофия» означает избыток ткани, увеличение органа, в данном случае можно говорить о сверхмерном утолщении стенок левого желудочка, что не исключает возможности одновременного нарастания массы предсердия, правых отделов.
^ Инфаркт миокарда – острый некроз сердечной мышцы. Он возникает в результате тромбоза или спазма коронарных артерий, измененных атеросклеротическими наложениями.

Инфаркт миокарда – одно из проявлений ИБС (см. выше).
^ Клинические проявления
В подавляющем большинстве случаев заболевание развивается внезапно. Возникает жгучая, раздирающая боль за грудиной, с иррадиацией в левую руку, плечо, левую лопатку, левую половину нижней челюсти. Если приступ стенокардии не купируется в течение 20 минут, а продолжается несколько часов, это помогает поставить диагноз инфаркта миокарда. В отличие от приступа стенокардии боль при инфаркте не снимается нитроглицерином. Часто возникает страх смерти, резкая слабость, холодный пот.
астматическая форма – с преобладанием одышки;
цереброваскулярная – с преобладанием церебральных нарушений;
аритмическая форма – с преобладанием нарушений ритма сердца;
малосимптомный ИМ – без четких клинических проявлений.
Осмотр. При осмотре кожа бледная, может быть покрыта холодным липким потом (в сочетании с уменьшением количества отделяемой мочи, слабым пульсом, гипотензией может быть признаком кардиогенного шока). Артериальная гипертензия сменяется гипотензией, возможны тахикардия, повышение температуры тела.

общий анализ крови (гемоглобин, гематокрит, содержание лейкоцитов, тромбоцитов);
биохимический анализ крови (уровень калия, оценка функции печени и почек);
определение в крови уровня сердечного тропонина Т или I, МВ-фракции КФК при поступлении в стационар; при получении нормальных значений данные показатели определяют повторно через 6—12 ч.
ЭКГ-диагностика
Мелкоочаговый ИМ (ИМ без зубца Q) характеризуется развитием в сердечной мышце мелких очагов некроза.
В отличие от крупноочагового ИМ мелкие очаги некроза не нарушают процесс распространения возбуждения по сердцу. Поэтому патологический зубец Q или комплекс QS, характерные для крупноочагового ИМ, при мелкоочаговом инфаркте отсутствуют (рис. 6).
#image.jpg#image.jpg

Рис. 6. Острый мелкоочаговый инфаркт переднеперегородочной области
1) смещение сегмента S—Т выше или (чаще) ниже изолинии;
2) разнообразные патологические изменения зубца Т (чаще отрицательный симметричный и заостренный коронарный зубец Т);
3) появление этих изменений на ЭКГ после длительного и интенсивного болевого приступа и их сохранение в течение 2—5 недель.
Крупноочаговый ИМ характеризуется появлением патологического зубца Q и снижением высоты зубца R. Каждый период инфаркта миокарда отличается определенными изменениями на ЭКГ (рис. 7).
#image.jpg
Норма.
#image.jpg

#image.jpg
#image.jpg
Острый период ИМ: патологический зубец Q,
подъем ST.
#image.jpg #image.jpg #image.jpg #image.jpg
Подострый период: увеличение зубца Q,
формирование отрицательного Т.
#image.jpg
Рубцовый период: ST на изолинии, отрицательный зубец T.
Рис. 7. ЭКГ при крупноочаговом инфаркте миокарда
При трансмуральном инфаркте миокарда сегмент ST поднимается над изолинией и плавно соединяется с зубцом Т, образуя монофазную кривую (симптом «кошачьей спинки»), исчезает зубец R, появляется патологический зубец Q (комплекс QS).
#image.jpg
Рис. 8. ЭКГ при трансмуральном инфаркте миокарда

1. переднеперегородочный ИМ: V1 – V3;
2. передневерхушечный ИМ: V3, V4;
3. переднебоковой ИМ: I, аVL, V5, V6;
4. заднедиафрагмальный (нижний) ИМ – II, III, аVF;
5. заднебоковой ИМ – V5, V6, III, аVF.
1. ИБС: крупноочаговый переднеперегородочный инфаркт миокарда, от 02.03.09 г. острая стадия. ХСН I ст, ФК II.
2. ИБС: острый мелкоочаговый инфаркт миокарда передне-перегородочной области. ПИК (2006 г). ХСН II Б ст. 3 ФК.
^ ТЕСТОВЫЕ ЗАДАНИЯ
Выберите один или несколько правильных ответов
1. БОЛИ ПРИ СТЕНОКАРДИИ СНИМАЮТСЯ
Результаты
Госпитальная летальность значительно снизилась за последние годы и составляет 3-7%. Основной причиной смерти является левожелудочковая недостаточность – 64%. Факторами риска послеоперационной летальности являются: пожилой возраст, неполная реваскуляризация миокарда, женский пол, экстренная операция, протезирование митрального клапана, фракция выброса левого желудочка {amp}lt; 30%, дооперационный сердечный индекс {amp}lt; 2,1 л.мин/м2, среднее давление в легочной артерии {amp}gt; 33 мм рт.ст., уровень креатинина {amp}gt; 180 мг/л.
Наиболее частым осложнением в госпитальном периоде является синдром малого сердечного выброса, а также желудочковые аритмии и легочная недостаточность.
В отдаленном послеоперационном периоде улучшается функция левого желудочка: возрастает фракция выброса, уменьшается КДО и КСО левого желудочка, диастолическое наполнение и комплайнс, увеличивается толерантность к физической нагрузке. Средний класс стенокардии снижается с 3,5 до 1,2, а класс сердечной недостаточности по классификации NYHA с 3,0 до 1,7. Результаты непосредственно зависят от метода ремоделирования левого желудочка, демонстрируя явное отсутствие преимуществ линейной пластики.
5-летняя выживаемость составляет 58-80%, 10-летняя – 34-57%. 57% смертельных случаев являются следствием повторных инфарктов миокарда. Дооперационными факторами риска отдаленной летальности являются возраст, фракция выброса {amp}lt; 35%, КДД Левого желудочка {amp}gt; 20 мм рт.ст., и митральная недостаточность.
Лечение аневризмы левого желудочка в Минске – европейское качество за разумную цену.
Профессор, доктор медицинских наук Ю.П. Островский
Источник: aptika.ru
Лечение миокарда направлено на восстановление кровоснабжения его поврежденных участков (перфузии) и функции их проводимости, на ограничение зоны локализованного некроза кардиомиоцитов, на активизацию клеточного метаболизма.
В клинической практике применяются лекарства нескольких фармакологических групп. При острых коронарных синдромах и окклюзионном тромбозе эпикардиальной коронарной артерии проводится реперфузионная терапия с тромболитическими препаратами (Стрептокиназой, Проурокиназой, Альтеплазой) и антиагрегантами (Тиклопидином, Клопидогрела сульфатом или Плавиксом).
При хронической сердечной недостаточности применяют препараты, которые тормозят регулирующий давление крови ангиотензинпревращающий фермент (иАПФ): Каптоприл, Эналаприл, Рамиприл, Фозиноприл. Их дозировка определяется кардиологом в зависимости от конкретного заболевания и показаний ЭКГ. К примеру, Каптоприл (Каприл, Алопресин, Тензиомин) может назначаться по 12,5-25 мг – трижды в сутки до еды (внутрь или под язык). В качестве побочных действий этого лекарства и большей части препаратов данной группы отмечают тахикардию, падение артериального давления, нарушения работы почек, недостаточность печени, тошноту и рвоту, диарею, крапивницу, повышенную тревожность, бессонницу, парестезии и тремор, сдвиги в биохимическом составе крови (в том числе лейкопению). Следует иметь в виду, что иАПФ не применяются при идеопатических патологиях миокарда, повышенном АД, стенозе аорты и сосудов почек, гиперластических изменениях коры надпочечников, асците, беременности и детском возрасте пациентов.
При ИБС и кардиомиопатиях могут назначаться антиишемические лекарственные средства группы периферических вазодилаторов, например, Молсидомин (Мотазомин, Корватон, Сиднофарм) или Адвокард. Молсидомин принимается внутрь – по одной таблетке (2 мг) трижды в течение суток; противопоказан при низком АД и состоянии кардиогенного шока; побочный эффект – головная боль.
Антиаритмический и гипотензивный препарат Верапамил (Веракард, Лекоптин) используют при ИБС с тахикардией и при стенокардии: по таблетке (80 мг) трижды в день. Могут быть побочные действия в виде тошноты, сухости во рту, проблем с кишечником, головной и мышечной болей, бессонницы, крапивницы, нарушений ЧСС. Данное средство противопоказано при выраженной сердечной недостаточности, мерцательной аритмии и брадикардии, пониженном АД.
Кардиотоническое и антигипоксическое действие оказывает лекарство Милдронат (Мельдоний, Ангиокардил, Вазонат, Кардионат и др. торговые названия). Его рекомендовано принимать по одной капсуле (250 мг) два раза в сутки. Данное средство может применяться только взрослым пациентам и противопоказано при нарушениях церебрального кровообращения и наличии структурных патологий головного мозга. При использовании Милдроната возможны такие побочные действия, как головные боли, головокружения, сердечная аритмия, одышка, сухость во рту и кашель, тошнота, расстройства кишечника.
Препараты группы β1-адреноблокаторов при ИБС (Метопролол, Пропранолол, Атенолол, Ацебутолол и др.), в первую очередь, снижают артериальное давление, а за счет действия на уменьшения симпатической стимуляции рецепторов на мембранах клеток миокарда уменьшают ЧСС, снижают сердечный выброс, повышая потребление кислорода кардиомиоцитами и облегчая боль. Например, Метопролол назначается по одной таблетке дважды в день, Атенолол достаточно принимать по одной таблетке в день. Однако препараты этой группы увеличивают риск острой сердечной недостаточности и блокады предсердий и желудочков, и их использование противопоказано при наличии застойной и декомпенсированной сердечной недостаточности, брадикардии, нарушении кровообращения. Поэтому в настоящее время антиаритмическое действие этих препаратов многие специалисты ставят под сомнение.
Облегчение боли в сердце имеет первостепенное значение, так как симпатическая активация во время боли вызывает сужение кровеносных сосудов и увеличивает нагрузку на сердце. Для купирования боли принято использовать Нитроглицерин. Подробная информация в статье – Эффективные таблетки, снимающие боль в сердце
Врачи рекомендуют принимать витамины В6, В9, Е, а для поддержания проводящей системы сердца – лекарства, содержащие калий и маний (Панангин, Аспаркам и др.).
Хирургическое лечение
При инфарктах с поражением коронарных артерий (приводящим к образованию участка ишемии миокарда и его акинезии с расширением камер сердца) показано хирургическое лечение с целью восстановления кровотока в сердце – аортокоронарное шунтирование.
При ишемической болезни сердца применяют коронарную дилатацию (расширение просвета) – стентирование.
Хирургическое лечение чаще всего применяется при дискинетической аневризме: либо путем аневризмоэктомии (резекции), либо путем ушивания аневризматической полости (аневризмопластики), либо с помощью укрепления ее стенки.
Разработан метод динамический кардиомиопластики, который подразумевает восстановление или повышение сократительной способности миокарда с использованием электрически стимулируемой скелетной мышцы (обычно лоскута края широчайшей мышцы спины), оборачиваемой вокруг части сердца (с частичной резекцией второго ребра). Мышечный лоскут пришивается вокруг желудочков, а его синхронная с сердечными сокращениями стимуляция осуществляется с помощью внутримышечных электродов имплантируемого кардиомиостимулятора.
Источник: ilive.com.ua
Сократимость миокарда нормокинез
Российский национальный конгресс кардиологов 2017 СИНДРОМ ТАКОЦУБО, СПРОВОЦИРОВАННЫЙ ПРОВЕДЕНИЕМ НАГРУЗОЧНОЙ ПРОБЫ Абдрахманова А.И.(1), Стекольщикова Н.Ю.(2), Галеев А.А.(2), Калимуллина Г.Х.(2), Сайфуллина Г.Б.(2), Ослопова Ю.В.(1), Хасанова Р.Н.(1) ФГАОУ ВО «Казанский (Приволжский) федеральный университет», Казань, Россия (1) ГАУЗ «Межрегиональный клинико — диагностический центр», Казань, Россия (2) Цель: предоставить случай синдрома такоцубо, спровоцированный проведением нагрузочной пробы. Материалы и методы: анализ медицинской документации. Результаты: Пациентка Б. 58 л., жалобы на боли ноющие в левой половине грудной клетки, длительные, не связанные с физической нагрузкой, часто в покое. Во время проведения Стресс ЭХО-КС с тредмилом (22.10. 10.00.) возникает нарушение ритма в виде НЖТ, ЖЭС, дискомфорт в груди, одышка, головокружение, «туман в голове», кратковременное синкопе. Проба не доведена до диагностических критериев. На достигнутой ЧСС глобальная сократительная функция левого желудочка осталась без изменений, явных участков нарушения локальной сократимости миокарда левого желудочка не выявлено. На ЭКГ: синусовый ритм, депрессия ST в V 4-6до 1,5 с переходом в 2-х фазный Т. Госпитализирована с подозрением на ОКС. Проведены следующие исследования: КАГ: тип коронарного кровообращения правый. ЛКА, ПКА без локальных гемодинамически значимых сужений просвета. ЭХОКС (22.10. 12.00) Нормокинез всех базальных сегментов, выраженный гипокинез всех апикальных и прилегающих к апикальным, частей медиальных сегментов левого желудочка со снижением его глобальной сократительной способности. ФВ 38%. Тропонин I (22.10. 12.00. 0,2 нг/мл, в 18.00. 5,6 нг/мл). ОФЭКТ (23.10.) Признаки обширного, от умеренного до выраженного, дефекта перфузии миокарда левого желудочка верхушечной локализации с вовлечением прилегающих медиальных отделов передней, боковой и нижней стенок — объем поражения составил 33%.Выраженное нарушение локальной сократимости сегментов верхушечной области, медиальных сегментов. Снижение глобальной сократительной функции ЛЖ. Увеличение полости левого желудочка (шарообразная конфигурация ЛЖ). ЭХОКС (30.10.) Сохраняется выраженная гипокинезия всех апикальных и частично медиальных сегментов левого желудочка. Снижение фракции выброса ЛЖ (ФВ 44%). На основании анамнеза (провоцирующий фактор — Стресс ЭХО-КС), клиники (боли ангинозного характера), инструментальных исследований: ЭКГ — глубокие отр. з. Т, нарушения ритма, удлинение QТ интервала; ЭХОКС+ОФЭКТ: акинез, гипокинез передней стенки, верхушки. при нормокинезе базальных отделов, «куполообразное» изменение конфигурации сердца; КАГ: отсутствие стенозов коронарных артерий; динамики тропонина (небольшой подъем при выраженном поражении) выставлен основной диагноз: Такоцубо-кардиомиопатия. Заключение: Синдром такоцубо обнаруживается у 1,7- 2,2% пациентов с ОКС. Знание диагностических критериев этого синдрома позволяет своевременно поставить правильный диагноз и выбрать необходимую тактику ведения пациента. [стр. 825 ⇒]
Российский национальный конгресс кардиологов 2017 ОСОБЕННОСТИ ВЛИЯНИЯ ЛЕВОКАРНИТИНА НА СИСТОЛИЧЕСКУЮ И ДИАСТОЛИЧЕСКУЮ ФУНКЦИЮ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА Аляви А.Л., Туляганова Д.К., Сабиржанова З.Т., Тошев Б.Б., Ражабова Д.И. АО «Республиканский Специализированный Научно-Практический Медицинский Центр Терапии и Медицинской Реабилитации», Ташкент, Узбекистан Целью настоящего исследования было изучение влияния левокарнитина на систолическую и диастолическую функцию левого желудочка у больных ишемической болезнью сердца. Материалы и методы: Обследованы 134 больных ИБС. Стенокардией напряжения ФК 2-3 в возрасте от 21 до 72 лет (средний возраст 51,2±5,7 лет). Все больные в анамнезе имели ранее перенесенный инфаркт миокарда. Всем больным было проведено базисное лечение, включавшее в себя назначение антиагрегантов, b-адреноблокаторов, ингибиторов АПФ, статинов. І группа (основная) — 66 больных, которым дополнительно к базисной терапии внутривенно капельно в течение 30–45 мин вводили препарат «Алмиба» (Левокарнитин, Гранд Медикал, США) на физиологическом растворе 0,9%-200 мл., внутривенн капельно в течение 5 дней, ІІ (контрольная) группа —68 больных. Все больным при поступлении была проведена ТЛБАП с последующим стентированием КА. Методом ЭхоКГ были изучены параметры систолической функции ЛЖ. Исследование проводилась на эхокардиографе Samsung medison «Accuvix.V20» (Корея). Стресс-эхокардиографию с добутамином проводили исходно для обнаружения жизнеспособного миокарда и оценки эффективности лечения после стентирования. Оценка региональной систолической функции ЛЖ проводилась по 16 сегментарному делению ЛЖ, рекомендованному Американским обществом эхокардиографистов по 4-балльной шкале: гиперкинез – 0 баллов, нормокинез –1 балл, гипокинез -2 балла, акинез –3 балла и дискинез–4 балла. Далее рассчитывался индекс нарушения регионарной сократимости (ИНРС) как соотношение суммы баллов анализируемых сегментов к общему их количеству. Критериями жизнеспособности (обратимой дисфункции) миокарда при стресс-ЭхоКГ является появление двухфазной реакции сократимости миокарда в зоне асинергии в виде повышения его сократимости на один балл и более. В группе левокарнитина выявлены 841 сегментов с асинергией, из них 796 (75,4% из общего числа сегментов) сегментов с гипокинезией и 45 (4,2%) сегментов с акинезией. В этой группе добутаминовая проба в малых дозах показала жизнеспособность миокарда в 723 (86%) сегментах из всех асинергичных сегментов, некрозу миокарда соответствовал 118 (14%) сегментов ЛЖ. В контрольной группе выявлены 882 сегмента с асинергией (зона акинезии в 34 сегментах и гипокинезии 848 сегментах). При малых дозах добутамина отмечается достоверное уменьшение количества асинергичных сегментов на 60,5% (534 сегмента), что означает наличие жизнеспособного миокарда. У остальных 39,5% (348 сегмента) систолическое утолщение стенок ЛЖ не наблюдалось, то есть в этих сегментах имел место некроз миокарда. Зоны обратимой дисфункции достоверно больше обнаружены в группе левокарнитина, по сравнению с группой контроля (86% против 60,5%). В I и II группах индекс нарушения регионарной сократимости (ИНРС) при малых дозах достоверно снижался по сравнению с исходными показателями на 36,3% и 33,3% (p>0,05) соответственно. Более значительное уменьшение ИНРС отмечено в группе левокарнитина (с 1,87±0,1 на 1,18±0,02) (p>0,05) по сравнению с контрольной группой (с 1,98±0,04 на 1,32±0,01) (p>0,05). На повторной ЭхоКГ через месяц в I группе — 694 (96%) и в группе II 491 (92%) асинергичные сегменты стали нормокинетичными. Однако, в группе II через месяц из всех выявленных жизнеспособных сегментов в 8% сократительная функция не восстановилась. Показатели глобальной систолической функции были выше в группе больных, получавших левокарнитин, по сравнению с контрольной группой. [стр. 1022 ⇒]
ИНТЕРПРЕТАЦИЯ В настоящее время для оценки очаговых нарушений сократимости используют 16-сегментарную модель деления ЛЖ с 4–5-балльной качественной шкалой оценки: 1 — нормокинез, 2 — гипокинез, 3 — акинез, 4 — дискинез, 5 — аневризма (рис. 5-101). Ухудшение показателя сократительной функции миокарда на 1 балл и более в двух соседних сегментах считают признаком вызванной ишемии. [стр. 217 ⇒]
Систолическое утолщение миокарда выражается в процентах и называется фракцией систолического утолщения (ФСУ): Ф С У = (TS — T D ) / T D х 100%, где TS толщина миокарда в конце систолы, TD — толщина миокарда в конце диастолы. В норме Ф С У составляет >30%. С учетом данных показателей выделяют различные виды сократимости: 1) нормокинез — нормальная амплитуда движения и утолщение миокарда; 2) гипокинез — снижение амплитуды движения и утолщения миокарда; 3) гиперкинез — увеличение амплитуды движения и утолщения миокарда; 4) акинез — отсутствие дв1гжения и утолщения миокарда; 5) дискинез — движение сегмента миокарда в направлении, противоположном нормальному при отсутствии систолического утолщения. Для количественной оценки нарушений локальной сократимости применяется индекс сократимости, который равен отношению суммы сократимости исследуемых сегментов к irx обшему числу. Сократимость каждого сегмента оценивается по 5-балльной системе: 1 — нормокинез; 2 — незначительный и умеренный гипокинез; 3 — значительный гипокинез; 4 — акинез; 5 — дискинез [3]. П р и этом учитываются только те сегменты, сократимость которых можно достоверно оценить. В норме данный показатель равняется 1, его увеличение свидетельствует о нарушении сократимости. Оценка ПЖ вследствие особенностей его расположения (в основном за грудиной) и анатомического строения (форма трехгранной пирамиды с основанием, обращенным к П П ) при эхокардиографическом исследова. [стр. 125 ⇒]
4.9). B- и М-режим позволяют выявить зоны нарушения локальной сократимости. Выделяют следующие варианты сократимости: 1. Нормокинез – все участки эндокарда в систолу одинаково утолщаются. 2. Гипокинез – уменьшение утолщения эндокарда в одной из зон в систолу, по сравнению с остальными участками. Локальный гипокинез, как правило, связан с мелкоочаговым или интрамуральным поражением миокарда. 3. Акинез – отсутствие утолщения эндокарда в систолу в одном из участков. Акинез, как правило, свидетельствует о наличии крупноочагового поражения. 4. Дискинез – парадоксальное движение участка сердечной мышцы в систолу (выбухание). Дискинез характерен для аневризмы. Оценка состояния миокарда и прогноз течения заболевания производится с помощью индекса сократимости – суммы индексов, поделенных на число сегментов. Для этого оценивается сократимость каждого сегмента по 5-балльной системе: 1 – нормокинез, 2 – умеренный гипокинез, 3 – выраженный гипокинез, 4 – акинез, 5 – дискинез. В том случае, когда индекс сократимости больше 2, показатель фракции выброса составляет менее 30 %. Аналогичные схемы оценки сегментарной сократительной функции используются при исследовании сердца другими методами лучевой диагностики: КТ, МРТ, ОФЭКТ. [стр. 176 ⇒]
ЭхоКГ для подтверждения синдрома коронарной недостаточности включает следующие методы: — двухмерную ЭхоКГ в В-режиме; — одномерную ЭхоКГ в М-режиме; — допплеровскую ЭхоКГ; — цветное доплеровское картирование при ЭхоКГ; — стресс-ЭхоКГ; — допплер-стресс-ЭхоКГ; — чреспищеводную ЭхоКГ. При проведении ЭхоКГ должны быть оценены следующие функции левого желудочка: — глобальные (конечный систолический объем (КСО), конечный диастолический объем (КДО), ударный объем (УО), фракция выброса (ФВ), индекс нарушений сердечных сокращений); — сегментарные — сократимость 18 сегментов левого желудочка (нормокинез, гипокинез, акинез, дискинез). Стресс-ЭхоКГ может включать: ЭхоКГ с динамической физической нагрузкой, ЭхоКГ с чреспищеводной электростимуляцией, ЭхоКГ с фармакологическими пробами, ЭхоКГ со специальными пробами (гипервентиляция, кистевой динамоманометр). Преимуществами ЭхоКГ перед ЭКГ являются возможность выявления ишемии миокарда до появления ангинозных болей и прекращение физической нагрузки до депрессии сегмента ST. Для диагностики синдрома коронарной недостаточности необходимо проведение сцинтиграфии миокарда, которая позволяет оценить локализацию и объем дефектов перфузии миокарда, уровень нарушений микроциркуляции, общую и локальную сократительную способность миокарда в покое и при физической нагрузке. В клинической практике затруднения при установлении диагноза касаются больных, в анамнезе которых присутствуют не все классические признаки коронарной недостаточности. Загрудинная боль может быть расценена врачом как нетипичная для развития этого синдрома за счет субъективизма больного в описании своего состояния. Некоторые больные используют слово «острая» в качестве синонима «тяжелая», другие могут описывать боль как ощущение болезненности или как диспепсию. Может быть нетипичной локализация боли: в области шеи, верхних конечностей, плече, нижней челюсти и зубах. Нетипичное описание активности, провоцирующей боль, может также ввести врача в заблуждение: некоторые пациенты не могут выполнить даже небольшое. [стр. 108 ⇒]
В отдаленном периоде – проанализировано 5050 сегмента. Выявлено, что зон нормокинеза стало – 4367 (86,45%) это на 242 сегментов больше, чем до операции (р>0,05), зон гипокинеза стало недостоверно меньше – 297 (6%), (р>0,05). Акинетичных и дискинетичных сегментов стало также недостоверно меньше – 297 (6%) и 77 (1,5%) (р >0,05) соответственно. Гиперкинетичных сегментов стало 12 (0,2%), (p>0,05) недостоверно больше, по сравнению с исходным периодом. Исходно нормальное значение индекса локальной сократимости составило 1,7±0,52. В группе превалировали пациенты с легкой степенью нарушения локальной сократимости – 62%. Среднею степень тяжести имели 20% пациентов и 18% – тяжелую степень нарушения индекса локальной сократимости. И только у 2 пациентов (1%) был нормальным ИНЛС. В отдаленном периоде ИНЛС достоверно уменьшился до 1,39±0,41 (р=0,000001), но при данном показателе отмечено увеличение на 4% количество пациентов с легкой степенью, на 7% и 3% уменьшилось количество пациентов со средней и тяжелой степенью (р=н/д), в то время как количество пациентов без нарушения индекса локальной сократимости достигло достоверных величин – 7%(р=0,0002). Общий вывод Таким обоазом, реваскуляризация миокарда больных хронической ишемической болезнью сердца методом транслюминальной баллонной ангиопластики и/или интракоронарного стентирования по данным эхокардиографии, приводило к недостоверному увеличению количества нормокинетичных сегментов и недостоверному уменьшению количества диссинергичных сегментов. Но, несмотря на это, достоверно увеличивалось количество пациентов с нормальным значением индекса локальной сократимости (р=0,0002). [стр. 62 ⇒]
Сократимость миокарда нормокинез
Российский национальный конгресс кардиологов 2017 СИНДРОМ ТАКОЦУБО, СПРОВОЦИРОВАННЫЙ ПРОВЕДЕНИЕМ НАГРУЗОЧНОЙ ПРОБЫ Абдрахманова А.И.(1), Стекольщикова Н.Ю.(2), Галеев А.А.(2), Калимуллина Г.Х.(2), Сайфуллина Г.Б.(2), Ослопова Ю.В.(1), Хасанова Р.Н.(1) ФГАОУ ВО «Казанский (Приволжский) федеральный университет», Казань, Россия (1) ГАУЗ «Межрегиональный клинико — диагностический центр», Казань, Россия (2) Цель: предоставить случай синдрома такоцубо, спровоцированный проведением нагрузочной пробы. Материалы и методы: анализ медицинской документации. Результаты: Пациентка Б. 58 л., жалобы на боли ноющие в левой половине грудной клетки, длительные, не связанные с физической нагрузкой, часто в покое. Во время проведения Стресс ЭХО-КС с тредмилом (22.10. 10.00.) возникает нарушение ритма в виде НЖТ, ЖЭС, дискомфорт в груди, одышка, головокружение, «туман в голове», кратковременное синкопе. Проба не доведена до диагностических критериев. На достигнутой ЧСС глобальная сократительная функция левого желудочка осталась без изменений, явных участков нарушения локальной сократимости миокарда левого желудочка не выявлено. На ЭКГ: синусовый ритм, депрессия ST в V 4-6до 1,5 с переходом в 2-х фазный Т. Госпитализирована с подозрением на ОКС. Проведены следующие исследования: КАГ: тип коронарного кровообращения правый. ЛКА, ПКА без локальных гемодинамически значимых сужений просвета. ЭХОКС (22.10. 12.00) Нормокинез всех базальных сегментов, выраженный гипокинез всех апикальных и прилегающих к апикальным, частей медиальных сегментов левого желудочка со снижением его глобальной сократительной способности. ФВ 38%. Тропонин I (22.10. 12.00. 0,2 нг/мл, в 18.00. 5,6 нг/мл). ОФЭКТ (23.10.) Признаки обширного, от умеренного до выраженного, дефекта перфузии миокарда левого желудочка верхушечной локализации с вовлечением прилегающих медиальных отделов передней, боковой и нижней стенок — объем поражения составил 33%.Выраженное нарушение локальной сократимости сегментов верхушечной области, медиальных сегментов. Снижение глобальной сократительной функции ЛЖ. Увеличение полости левого желудочка (шарообразная конфигурация ЛЖ). ЭХОКС (30.10.) Сохраняется выраженная гипокинезия всех апикальных и частично медиальных сегментов левого желудочка. Снижение фракции выброса ЛЖ (ФВ 44%). На основании анамнеза (провоцирующий фактор — Стресс ЭХО-КС), клиники (боли ангинозного характера), инструментальных исследований: ЭКГ — глубокие отр. з. Т, нарушения ритма, удлинение QТ интервала; ЭХОКС+ОФЭКТ: акинез, гипокинез передней стенки, верхушки. при нормокинезе базальных отделов, «куполообразное» изменение конфигурации сердца; КАГ: отсутствие стенозов коронарных артерий; динамики тропонина (небольшой подъем при выраженном поражении) выставлен основной диагноз: Такоцубо-кардиомиопатия. Заключение: Синдром такоцубо обнаруживается у 1,7- 2,2% пациентов с ОКС. Знание диагностических критериев этого синдрома позволяет своевременно поставить правильный диагноз и выбрать необходимую тактику ведения пациента. [стр. 825 ⇒]
Российский национальный конгресс кардиологов 2017 ОСОБЕННОСТИ ВЛИЯНИЯ ЛЕВОКАРНИТИНА НА СИСТОЛИЧЕСКУЮ И ДИАСТОЛИЧЕСКУЮ ФУНКЦИЮ У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА Аляви А.Л., Туляганова Д.К., Сабиржанова З.Т., Тошев Б.Б., Ражабова Д.И. АО «Республиканский Специализированный Научно-Практический Медицинский Центр Терапии и Медицинской Реабилитации», Ташкент, Узбекистан Целью настоящего исследования было изучение влияния левокарнитина на систолическую и диастолическую функцию левого желудочка у больных ишемической болезнью сердца. Материалы и методы: Обследованы 134 больных ИБС. Стенокардией напряжения ФК 2-3 в возрасте от 21 до 72 лет (средний возраст 51,2±5,7 лет). Все больные в анамнезе имели ранее перенесенный инфаркт миокарда. Всем больным было проведено базисное лечение, включавшее в себя назначение антиагрегантов, b-адреноблокаторов, ингибиторов АПФ, статинов. І группа (основная) — 66 больных, которым дополнительно к базисной терапии внутривенно капельно в течение 30–45 мин вводили препарат «Алмиба» (Левокарнитин, Гранд Медикал, США) на физиологическом растворе 0,9%-200 мл., внутривенн капельно в течение 5 дней, ІІ (контрольная) группа —68 больных. Все больным при поступлении была проведена ТЛБАП с последующим стентированием КА. Методом ЭхоКГ были изучены параметры систолической функции ЛЖ. Исследование проводилась на эхокардиографе Samsung medison «Accuvix.V20» (Корея). Стресс-эхокардиографию с добутамином проводили исходно для обнаружения жизнеспособного миокарда и оценки эффективности лечения после стентирования. Оценка региональной систолической функции ЛЖ проводилась по 16 сегментарному делению ЛЖ, рекомендованному Американским обществом эхокардиографистов по 4-балльной шкале: гиперкинез – 0 баллов, нормокинез –1 балл, гипокинез -2 балла, акинез –3 балла и дискинез–4 балла. Далее рассчитывался индекс нарушения регионарной сократимости (ИНРС) как соотношение суммы баллов анализируемых сегментов к общему их количеству. Критериями жизнеспособности (обратимой дисфункции) миокарда при стресс-ЭхоКГ является появление двухфазной реакции сократимости миокарда в зоне асинергии в виде повышения его сократимости на один балл и более. В группе левокарнитина выявлены 841 сегментов с асинергией, из них 796 (75,4% из общего числа сегментов) сегментов с гипокинезией и 45 (4,2%) сегментов с акинезией. В этой группе добутаминовая проба в малых дозах показала жизнеспособность миокарда в 723 (86%) сегментах из всех асинергичных сегментов, некрозу миокарда соответствовал 118 (14%) сегментов ЛЖ. В контрольной группе выявлены 882 сегмента с асинергией (зона акинезии в 34 сегментах и гипокинезии 848 сегментах). При малых дозах добутамина отмечается достоверное уменьшение количества асинергичных сегментов на 60,5% (534 сегмента), что означает наличие жизнеспособного миокарда. У остальных 39,5% (348 сегмента) систолическое утолщение стенок ЛЖ не наблюдалось, то есть в этих сегментах имел место некроз миокарда. Зоны обратимой дисфункции достоверно больше обнаружены в группе левокарнитина, по сравнению с группой контроля (86% против 60,5%). В I и II группах индекс нарушения регионарной сократимости (ИНРС) при малых дозах достоверно снижался по сравнению с исходными показателями на 36,3% и 33,3% (p>0,05) соответственно. Более значительное уменьшение ИНРС отмечено в группе левокарнитина (с 1,87±0,1 на 1,18±0,02) (p>0,05) по сравнению с контрольной группой (с 1,98±0,04 на 1,32±0,01) (p>0,05). На повторной ЭхоКГ через месяц в I группе — 694 (96%) и в группе II 491 (92%) асинергичные сегменты стали нормокинетичными. Однако, в группе II через месяц из всех выявленных жизнеспособных сегментов в 8% сократительная функция не восстановилась. Показатели глобальной систолической функции были выше в группе больных, получавших левокарнитин, по сравнению с контрольной группой. [стр. 1022 ⇒]
ИНТЕРПРЕТАЦИЯ В настоящее время для оценки очаговых нарушений сократимости используют 16-сегментарную модель деления ЛЖ с 4–5-балльной качественной шкалой оценки: 1 — нормокинез, 2 — гипокинез, 3 — акинез, 4 — дискинез, 5 — аневризма (рис. 5-101). Ухудшение показателя сократительной функции миокарда на 1 балл и более в двух соседних сегментах считают признаком вызванной ишемии. [стр. 217 ⇒]
Систолическое утолщение миокарда выражается в процентах и называется фракцией систолического утолщения (ФСУ): Ф С У = (TS — T D ) / T D х 100%, где TS толщина миокарда в конце систолы, TD — толщина миокарда в конце диастолы. В норме Ф С У составляет >30%. С учетом данных показателей выделяют различные виды сократимости: 1) нормокинез — нормальная амплитуда движения и утолщение миокарда; 2) гипокинез — снижение амплитуды движения и утолщения миокарда; 3) гиперкинез — увеличение амплитуды движения и утолщения миокарда; 4) акинез — отсутствие дв1гжения и утолщения миокарда; 5) дискинез — движение сегмента миокарда в направлении, противоположном нормальному при отсутствии систолического утолщения. Для количественной оценки нарушений локальной сократимости применяется индекс сократимости, который равен отношению суммы сократимости исследуемых сегментов к irx обшему числу. Сократимость каждого сегмента оценивается по 5-балльной системе: 1 — нормокинез; 2 — незначительный и умеренный гипокинез; 3 — значительный гипокинез; 4 — акинез; 5 — дискинез [3]. П р и этом учитываются только те сегменты, сократимость которых можно достоверно оценить. В норме данный показатель равняется 1, его увеличение свидетельствует о нарушении сократимости. Оценка ПЖ вследствие особенностей его расположения (в основном за грудиной) и анатомического строения (форма трехгранной пирамиды с основанием, обращенным к П П ) при эхокардиографическом исследова. [стр. 125 ⇒]
4.9). B- и М-режим позволяют выявить зоны нарушения локальной сократимости. Выделяют следующие варианты сократимости: 1. Нормокинез – все участки эндокарда в систолу одинаково утолщаются. 2. Гипокинез – уменьшение утолщения эндокарда в одной из зон в систолу, по сравнению с остальными участками. Локальный гипокинез, как правило, связан с мелкоочаговым или интрамуральным поражением миокарда. 3. Акинез – отсутствие утолщения эндокарда в систолу в одном из участков. Акинез, как правило, свидетельствует о наличии крупноочагового поражения. 4. Дискинез – парадоксальное движение участка сердечной мышцы в систолу (выбухание). Дискинез характерен для аневризмы. Оценка состояния миокарда и прогноз течения заболевания производится с помощью индекса сократимости – суммы индексов, поделенных на число сегментов. Для этого оценивается сократимость каждого сегмента по 5-балльной системе: 1 – нормокинез, 2 – умеренный гипокинез, 3 – выраженный гипокинез, 4 – акинез, 5 – дискинез. В том случае, когда индекс сократимости больше 2, показатель фракции выброса составляет менее 30 %. Аналогичные схемы оценки сегментарной сократительной функции используются при исследовании сердца другими методами лучевой диагностики: КТ, МРТ, ОФЭКТ. [стр. 176 ⇒]
ЭхоКГ для подтверждения синдрома коронарной недостаточности включает следующие методы: — двухмерную ЭхоКГ в В-режиме; — одномерную ЭхоКГ в М-режиме; — допплеровскую ЭхоКГ; — цветное доплеровское картирование при ЭхоКГ; — стресс-ЭхоКГ; — допплер-стресс-ЭхоКГ; — чреспищеводную ЭхоКГ. При проведении ЭхоКГ должны быть оценены следующие функции левого желудочка: — глобальные (конечный систолический объем (КСО), конечный диастолический объем (КДО), ударный объем (УО), фракция выброса (ФВ), индекс нарушений сердечных сокращений); — сегментарные — сократимость 18 сегментов левого желудочка (нормокинез, гипокинез, акинез, дискинез). Стресс-ЭхоКГ может включать: ЭхоКГ с динамической физической нагрузкой, ЭхоКГ с чреспищеводной электростимуляцией, ЭхоКГ с фармакологическими пробами, ЭхоКГ со специальными пробами (гипервентиляция, кистевой динамоманометр). Преимуществами ЭхоКГ перед ЭКГ являются возможность выявления ишемии миокарда до появления ангинозных болей и прекращение физической нагрузки до депрессии сегмента ST. Для диагностики синдрома коронарной недостаточности необходимо проведение сцинтиграфии миокарда, которая позволяет оценить локализацию и объем дефектов перфузии миокарда, уровень нарушений микроциркуляции, общую и локальную сократительную способность миокарда в покое и при физической нагрузке. В клинической практике затруднения при установлении диагноза касаются больных, в анамнезе которых присутствуют не все классические признаки коронарной недостаточности. Загрудинная боль может быть расценена врачом как нетипичная для развития этого синдрома за счет субъективизма больного в описании своего состояния. Некоторые больные используют слово «острая» в качестве синонима «тяжелая», другие могут описывать боль как ощущение болезненности или как диспепсию. Может быть нетипичной локализация боли: в области шеи, верхних конечностей, плече, нижней челюсти и зубах. Нетипичное описание активности, провоцирующей боль, может также ввести врача в заблуждение: некоторые пациенты не могут выполнить даже небольшое. [стр. 108 ⇒]
В отдаленном периоде – проанализировано 5050 сегмента. Выявлено, что зон нормокинеза стало – 4367 (86,45%) это на 242 сегментов больше, чем до операции (р>0,05), зон гипокинеза стало недостоверно меньше – 297 (6%), (р>0,05). Акинетичных и дискинетичных сегментов стало также недостоверно меньше – 297 (6%) и 77 (1,5%) (р >0,05) соответственно. Гиперкинетичных сегментов стало 12 (0,2%), (p>0,05) недостоверно больше, по сравнению с исходным периодом. Исходно нормальное значение индекса локальной сократимости составило 1,7±0,52. В группе превалировали пациенты с легкой степенью нарушения локальной сократимости – 62%. Среднею степень тяжести имели 20% пациентов и 18% – тяжелую степень нарушения индекса локальной сократимости. И только у 2 пациентов (1%) был нормальным ИНЛС. В отдаленном периоде ИНЛС достоверно уменьшился до 1,39±0,41 (р=0,000001), но при данном показателе отмечено увеличение на 4% количество пациентов с легкой степенью, на 7% и 3% уменьшилось количество пациентов со средней и тяжелой степенью (р=н/д), в то время как количество пациентов без нарушения индекса локальной сократимости достигло достоверных величин – 7%(р=0,0002). Общий вывод Таким обоазом, реваскуляризация миокарда больных хронической ишемической болезнью сердца методом транслюминальной баллонной ангиопластики и/или интракоронарного стентирования по данным эхокардиографии, приводило к недостоверному увеличению количества нормокинетичных сегментов и недостоверному уменьшению количества диссинергичных сегментов. Но, несмотря на это, достоверно увеличивалось количество пациентов с нормальным значением индекса локальной сократимости (р=0,0002). [стр. 62 ⇒]
Нормокинез сердца что это такое

Если у вас возникло мерцание перед глазами всего лишь несколько раз, .

На нашем форуме всё больше и больше посетителей, которые обращаются .

В совокупности сосуды, входящие в состав яремных вен, осуществляют .

Холестерин — крайне противоречивое химическое соединение. По своей .

Крипторхизм – отсутствие в мошонке у мужчин одного или двух яичек .

Инсульт — болезнь с «женским лицом». Именно такая .

Волосатая лейкоплакия — одна из форм лейкоплакии, имеющая важное .

Трофическими язвами называют нарушения целостности кожного покрова .

Трофическая язва на ноге, см. фото – это патологические образования .
Как можно снять тахикардию в домашних условиях?
Как можно укрепить сердечную мышцу?
Показания и противопоказания к прижиганию сердца
Возможные последствия аритмии сердца
© Copyright 2014–2020 1poserdcu.ru
Копирование материалов сайта возможно без предварительного согласования в случае установки активной индексируемой ссылки на наш сайт.
Внимание! Информация, опубликованная на сайте, носит исключительно ознакомительный характер и не является рекомендацией к применению. Обязательно проконсультируйтесь с вашим лечащим врачом!
Источник: cc37.ru
