Синдром удлиненного интервала QT (LQT) – врожденная или приобретенная кардиальная патология, для которой характерно удлинение соответствующего интервала на электрокардиограмме, наличие повторных синкопальных состояний и высокого риска внезапной смерти вследствие развития злокачественных аритмий. Врожденный вариант синдрома встречается во всех этнических группах с частотой от 1:2000 до 1:2500. Несколько чаще страдают от него лица женского пола. Распространенность приобретенного синдрома колеблется от 2,5 до 4 случаев на 1 млн человек. В нашей статье рассмотрим, почему возникает LQT, какие симптомы вызывает, чем он опасен, и как его лечить.
Заболевание известно с конца 19 века, когда впервые было описано в медицинской литературе наблюдение за девочкой с врожденной глухотой и частыми обморочными состояниями, возникающими при сильном волнении (1856 г., Meissner). Позже была выявлена его элетрокардиографическая картина (1953 г., Moller). В настоящее время изучение этого синдрома и поиск эффективных методов его лечения продолжается.
Причины врожденного синдрома
В основе наследственного варианта синдрома лежат мутации генов, кодирующих функции белковых молекул ионных каналов в сердечной мышце. В настоящее время известно более 180 таких мутаций в 7 генах, которые расположены в 3, 7, 11 и 21-й хромосомах. В большинстве случаев они нарушают работу калиевых и натриевых каналов, реже – кальциевых каналов и специфических строительных белков. Это приводит к возрастанию длительности потенциала действия в кардиомиоцитах, инициирующему появление желудочковой тахикардии типа «пируэт», которая может переходить в фибрилляцию желудочков.
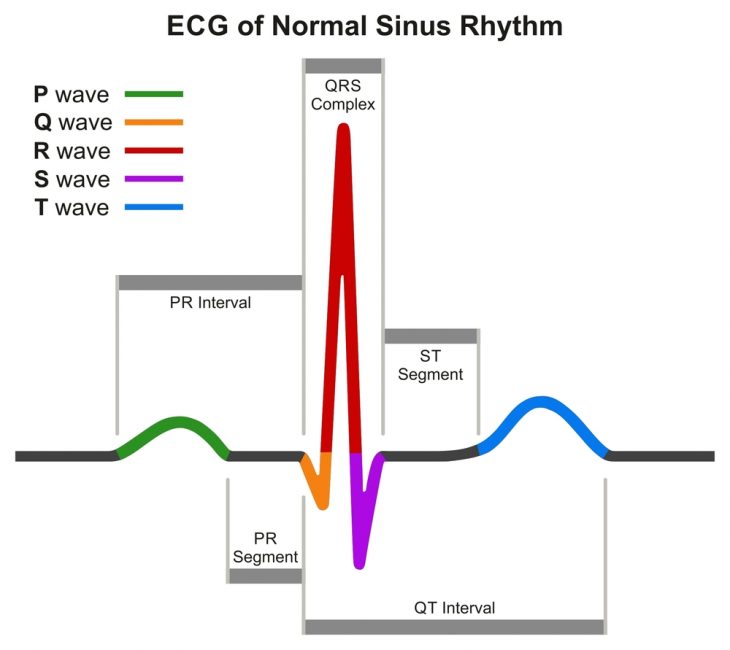
Процессы деполяризации и реполяризации, возникающие вследствие движения электролитов в клетку из внеклеточного пространства и обратно, на ЭКГ отражает интервал QT, который удлиняется при данной патологии.
В клинической практике выделяют 3 основных варианта наследственного синдрома:
- Романо-Уорда (характеризуется изолированным удлинением QT, передается от родителей с доминантными генами);
- Джервелла-Ланге-Нильсена (наследуется по аутосомно-рецессивному типу и сочетается с врожденной глухотой);
- аутосомно-доминантный вариант с экстракардиальными проявлениями.
Последний из них может проявить себя в виде:
- синдрома Андерсена-Тавила (удлинение QT сочетается с выраженной U-волной, желудочковой тахикардией, аномалиями развития костной системы, гипер- или гипокалиемическим периодическим параличом);
- синдрома Тимоти (синдактилия, врожденные сердечные аномалии, разные нарушения проводимости, крайне высокий риск внезапного летального исхода).
Приобретенная форма
Ранее считалось, что возникновение приобретенного синдрома LQT связано с нарушением работы ионных каналов, которое вызывает не мутация, а воздействие каких-либо внешних или внутренних факторов. Это утверждение справедливо, но доказано, что способствует развитию патологического процесса генетический дефект. При этом приобретенный синдром сложно разграничить с врожденной патологией, так как они имеют много общего. Обычно данная патология длительное время остается незамеченной и проявляет себя в неблагоприятных условиях, например под действием стресса или физических нагрузок. К факторам, способствующим удлинению интервала QT, относят:
- прием лекарственных средств (ниже рассмотрим, каких именно);
- электролитные нарушения (недостаток калия, натрия, магния);
- нарушения сердечного ритма;
- ишемическая болезнь сердца;
- миокардиты;
- гипертрофическая кардиомиопатия;
- заболевания нервной системы (травмы, инфекции, опухоли);
- изменение гормонального статуса (сахарный диабет, патология щитовидной железы или надпочечников);
- алкоголизм;
- голодание и др.
Особую опасность представляет воздействие на восприимчивый организм нескольких факторов риска.
Группы препаратов, способных влиять на длину интервала QT
В связи с тем, что синдром LQT может быть вызван прямым воздействием лекарственных препаратов, а их отмена часто приводит к нормализации всех показателей, рассмотрим подробнее, какие лекарственные средства могут изменять длину интервала QT:
- антиаритмики (амиодарон, новокаинамид, соталол, пропафенон, дизопирамид);
- антибиотики (эритромицин, спирамицин, кларитромицин, изониазид);
- антигистаминные препараты (эбастин, астемизол);
- анестетики;
- антимикотики (флуконазол, кетоконазол);
- противоопухолевые препараты;
- психотропные средства (дроперидол, амитриптилин);
- диуретики (индапамид) и др.
Их нельзя назначать лицам, уже имеющим удлинение этого интервала. А при позднем дебюте болезни обязательно исключается их роль как провоцирующего фактора.
Клинические проявления

Клиническая картина синдрома отличается полиморфизмом симптомов. Их выраженность может варьировать от легкого головокружения до потери сознания и внезапной смерти. Иногда последняя может выступать в роли первого признака болезни. Наиболее типичными проявлениями данной патологии считаются:
- приступы потери сознания;
- врожденная глухота;
- случаи внезапной смерти в семье;
- изменения на электрокардиограмме (QT более 450 мс, альтернация зубца Т, желудочковая тахикардия по типу «пируэт», замедление частоты сердечных сокращений).
При врожденных вариантах синдрома могут выявляться другие, характерные только для него симптомы.
Следует обратить внимание, что синкопальные состояния при данной патологии имеют свои особенности:
- возникают на фоне стресса, под действием сильных звуковых раздражителей (будильник, телефонный звонок), физической активности, занятий спортом (плавание, ныряние), во время резкого пробуждения от ночного сна, у женщин – после родов;
- наличие симптомов, предшествующих потере сознания (головокружение, резкая слабость, звон в ушах, потемнение в глазах, ощущение сердцебиения, тяжести за грудиной);
- быстрое восстановление сознания при благоприятном исходе;
- отсутствие амнезии и изменений личности (как при эпилепсии).
Иногда потеря сознания может сопровождаться судорогами и непроизвольным мочеиспусканием. В таких случаях проводится дифференциальная диагностика с эпилептическими припадками.
Течение патологического процесса у каждого больного может иметь определенные различия. Оно зависит как от генотипа, так и от условий жизни. Наиболее распространенными считаются следующие его варианты:
- синкопе, возникающие на фоне удлинения интервала QT;
- изолированное удлинение этого интервала;
- синкопе в отсутствие изменений на ЭКГ;
- полное отсутствие симптомов (высокий риск внезапной смерти без фенотипических проявлений заболевания).
Наиболее неблагоприятный вариант течения осложняется развитием фибрилляции желудочков и остановкой сердца.
При врожденных вариантах болезни обмороки появляются в детском возрасте (5-15 лет). Причем их возникновение у детей дошкольного возраста – прогностически неблагоприятный признак. А пароксизм желудочковой тахикардии, потребовавший оказания неотложной помощи, увеличивает вероятность повторной остановки сердца в ближайшее время в 10 раз.
Пациенты с синдромом удлиненного интервала QT, имеющим бессимптомное течение, могут не знать о своем диагнозе и иметь нормальную продолжительность жизни, но передавать мутацию по наследству своим детям. Такое течение наблюдается очень часто.
Принципы диагностики
Диагностика синдрома базируется на клинических данных и результатах электрокардиографии. Дополнительную информацию врачу предоставляет холтеровское мониторирование.
С учетом того, что поставить диагноз не всегда легко, разработаны большие и малые диагностические критерии. К последним относят:
- отсутствие слуха с рождения;
- изменчивость зубца Т в разных отведениях (на электрокардиограмме);
- нарушение процессов реполяризации миокарда желудочков;
- низкая частота сердечных сокращений.
Среди больших критериев выделяют:
- удлинение корригированного интервала QT более 450 мс в покое;
- эпизоды потери сознания;
- случаи болезни в семье.
Диагноз считается достоверным при наличии двух больших или одного большого и двух малых критериев.
Лечение

Основным направлением лечения таких больных является предупреждение злокачественных аритмий и остановки сердца.
Все лица, имеющие удлиненный интервал QT, должны избегать:
- стрессовых ситуаций;
- занятий спортом;
- тяжелых физических нагрузок;
- приема препаратов, увеличивающих длину этого интервала.
Из медикаментов при этом синдроме обычно назначаются:
- β-адреноблокаторы;
- препараты магния и калия;
- мексилетин или флекаинид (в низких дозах).
При неэффективности консервативной терапии прибегают к симпатической денервации или имплантации кардиовертера-дефибриллятора. Последнее особенно важно у больных с высоким риском внезапной сердечной смерти и перенесшим реанимационные мероприятия.
Лицам с отсутствием симптомов, но с изменениями на ЭКГ при наличии неблагоприятных факторов должно проводиться профилактическое лечение β-адреноблокаторами. Также оправдано назначение этих лекарств в послеродовом периоде у женщин, не имеющих ЭКГ-признаков данной патологии, при наличии случаев болезни среди близких родственников.
Заключение
При отсутствии лечения синдром удлиненного интервала QT нередко имеет неблагоприятный исход. Уровень летальности среди больных составляет около 20 % в течение первого года после постановки диагноза и около 50 % в последующие 10 лет. При этом сохранить жизнь человеку позволяет ранняя диагностика и правильное лечение. Современная тактика ведения таких пациентов снижает риск внезапной смерти почти в 10 раз.
Нужно учитывать, что истинный синдром удлиненного QT – редкое заболевание, требующее генетического исследования и другой диагностики. Только по наличию изменений на ЭКГ или суточного мониторирования диагноз поставить нельзя.
О синдроме удлиненного интервала QT в программе «Жить здорово!» с Еленой Малышевой (см. с 31:55 мин.):
Источник: myfamilydoctor.ru
Синдром удлиненного интервала QT (CУИ QT) представляет собой генетически детерминированное заболевание с высоким риском внезапной сердечной смерти (ВСС), характеризующееся постоянным или преходящим удлинением интервала QT на электрокардиограмме (ЭКГ), эпизодами потери сознания на фоне желудочковой тахикардии (ЖТ) и/или фибрилляции желудочков (ФЖ) [1].
СУИ QT, как известно, может быть врождённым или приобретенным [1]. Первый из них обычно проявляется в молодом возрасте (средний возраст 14 лет). Ежегодная частота ВСС при отсутствии лечения составляет от 0,9% до 5% (при наличии обмороков) [2], а при некоторых генетических формах достигает 40-70% в течение первого года после клинической манифестации [3, 4]. ВСС может стать первым проявлением заболевания [5, 6]. В патогенезе СУИ QT рассматриваются две основные гипотезы: ранняя — вегетативного дисбаланса в сторону повышения симпатических влияний, более современная — нарушения функции трансмембранных ионселективных каналов вследствие разных мутаций в генах, кодирующих структурные или регуляторные белки [3].
рушения функционирования калиевых, натриевых или кальциевых потенциалзависимых ионных каналов приводят к увеличению продолжительности потенциала действия в кардиомиоците, что при сопутствующих условиях может облегчить появление ранних или поздних постдеполяризаций и развитие ЖТ/ФЖ. К настоящему времени известно более 700 мутаций в 13 генах [1, 2], а по некоторым источникам — в 16 [7, 8].
В 1985 году P.J.Schwartz предложил диагностические критерии врождённого СУИ QT, которые в последующем изменялись. В настоящее время для постановки диагноза врождённого СУИ QT рекомендуются диагностические критерии, представленные в табл. 1 и 2 [2, 9].


Поскольку удлинение интервала QT может носить преходящий характер, а эпизоды синкопальных состояний вследствие ЖТ/ФЖ развиваются редко, в диагностике заболевания имеют значение продолжительная регистрация ЭКГ (суточное мониторирование ЭКГ или имплантируемые устройства) и провокационные пробы (например, проба с физической нагрузкой или с введением альфа- и бета-адреностимуляторов) [3, 7, 10].
рмальные значения длительности QTc, валидные для суточной записи ЭКГ, находятся в стадии разработки. Максимальные значения среднесуточного QTс у здоровых лиц при автоматическом расчете в разных системах холтеровского мониторирования обычно не превышают 450 мс [11]. Методы молекулярно-генетического анализа имеют большое значение в диагностике СУИ QT и определении прогноза больных [2]. По данным Международного регистра, примерно в 85% случаев заболевание является наследственным, в то время как около 15% случаев представляют собой следствие новых спонтанных мутаций. Примерно у 10% пациентов с СУИ QT при генотипировании было выявлено как минимум две мутации, связанные с генезом данного состояния, что определяет вариабельность его клинических проявлений и характера наследования [4]. Результаты молекулярно-генетического анализа позволили создать классификацию СУИ QT в зависимости от мутантного гена. Большинство пациентов с установленным диагнозом СУИ QT относится к первым трём вариантам синдрома: СУИQT 1 типа (35-50% случаев), СУИQT 2 типа (25-40% случаев) и СУИQT 3 типа (5-10% случаев) — см. табл. 3.

Остальные генотипы СУИ QT встречаются менее чем в 1,5% случаев [2, 12]. Различные типы наследственного СУИ QT характеризуются изменением реполяризации на ЭКГ: широкая гладкая волна T при СУИ QT 1 типа; двухфазная T-волна при СУИ QT 2 типа; низкоамплитудная и укороченная T-волна с удлиненным, горизонтальным ST-сегментом при СУИ QT 3 типа [13]. Однако в настоящее время не утратила актуальности фенотипическая классификация СУИ QT. Самый распространённый фенотипический вариант — это синдром Романо-Уорда с аутосомно-доминантным типом наследования (распространенность 1 случай на 2500 человек), который включает генотипы СУИ QT с 1 типа по 6 тип и СУИ QT с 9 типа по 13 тип и характеризуется изолированным удлинением интервала QT. Второй по распространённости фенотип с аутосомнорецессивным типом наследования — синдром Джервелла-Ланге-Нильсена (СУИ QT-JLN1 и СУИ QT-JLN2 с мутациями в генах KCNQ1 и KCNE1 соответственно), для которого характерно очень выраженное удлинение интервала QT и врожденная глухота [2]. Крайне редко встречается третий фенотип, характеризующийся экстракардиальными проявлениями (например, аномалией развития костной системы) и аутосомно-доминантным типом наследования. Он подразделяется на следующие подтипы: синдром Андерсена-Тавила (генотип СУИ QT 7 с мутацией в гене KCNJ) и синдром Тимоти (генотип СУИ QT 8 с мутацией в гене CACNA1c). При синдроме Тимоти отмечают наиболее выраженное удлинение интервалов QT и QTc (до 700 мс), сопровождающееся крайне высоким риском ВСС (средняя продолжительность жизни составляет 2,5 года) [7]. Около 50% случаев синдрома Андерсена-Тавила и синдрома Тимоти обусловлены мутацией de novo [7]. При проведении комплексных генетических анализов мутации удаётся обнаружить приблизительно у 75% больных СУИ QT, поэтому отрицательный результат генетического анализа не позволяет полностью исключить диагноз СУИ QT [13]. Приобретенный СУИ QT обусловлен нарушением электрической гомогенности миокарда или его иннервации вследствие острых состояний, хронических заболеваний, либо под влиянием лекарственных средств (противоаритмические, психотропные, антигистаминные, антибиотики, прокинетики, цитостатики и др.) [1].
Факторами, провоцирующими развитие жизнеугрожающих аритмий, могут быть физическая нагрузка, эмоциональные состояния, плавание, громкие резкие звуковые сигналы (например, звонок будильника), послеродовый период. Реже аритмии возникают во время сна или в покое [2]. Примерно у 20% больных, имеющих вторичное удлинение QT, выявляются специфические для СУИ QT мутации. Существует мнение, что пациенты с приобретенной формой СУИ QT являются латентными носителями таких генотипов, клинически проявляющихся под воздействием внешних провоцирующих факторов [4, 12]. Стратификация индивидуального риска осуществляется с учетом клинических, электрокардиографических и генетических параметров. На сегодняшний день нет данных, свидетельствующих о прогностической значимости инвазивного электрофизиологического исследования с программированной стимуляцией желудочков у пациентов с СУИ QT [2]. Молекулярно-генетическая диагностика помогает разрабатывать генспецифическую терапию СУИ QT. В частности, установлено, что β-адреноблокаторы наиболее эффективны при СУИ QT1, менее эффективны при СУИ QT2 и неэффективны при СУИ QT3. В то же время известно, что при СУИ QT2 более действенны препараты калия, а блокаторы натриевых каналов (например, мексилетин) — при СУИ QT3. Такие рекомендации по образу жизни, как исключение активного плавания, особенно при СУИ QT1, избегание воздействия громких звуков при СУИ QT2, могут способствовать предотвращению опасных для жизни аритмий [1, 2, 10]. Сохранение обмороков или эпизодов ВСС на фоне терапии β-адреноблокаторами является абсолютным показанием к имплантации кардиовертера-дефибриллятора. Учитывая роль повышенной симпатической активности в патогенезе СУИ QT, в качестве одного из дополнительных ресурсов лечения у больных с тяжелым течением заболевания рассматривают левостороннюю симпатическую денервацию [2, 10].
Пациентка С. 22 лет поступила в плановом порядке в кардиологическое отделение клиники СЗГМУ им. И.И.Мечникова для эндоваскулярного лечения стеноза правой почечной артерии. При поступлении предъявляла жалобы на эпизоды повышения артериального давления (АД), в последнее время до 170/100 мм рт.ст., сопровождавшиеся головными болями в затылочной области и висках. Привычными значениями АД считает 110-130/70-80 мм рт.ст. При опросе по системам органов выяснилось, что с детства у больной наблюдаются внезапные потери сознания с частотой 1-2 раза в год, по поводу чего неоднократно обследовалась, причина синкопальных состояний установлена не была. Кроме того, у пациентки длительно имеется почти постоянная заложенность носа в течение дня, усиливающаяся в горизонтальном положении, по поводу чего ежедневно использует интраназальные капли «нафтизин». В течение последних 3 лет наблюдается увеличение числа психоэмоциональных стрессов (обучение в вузе) и нарушение режима сон-бодрствование: ограничение ночного сна, смещение фазы сна (отход ко сну со второй половины ночи с последующим поздним пробуждением).
Анамнез заболевания. Впервые эпизоды повышения АД стала отмечать около 2 лет назад с максимальным значением 190/110 мм рт.ст. Обследована амбулаторно. По данным эхокардиографии не выявлено отклонений от нормы. По данным суточного мониторирования АД: динамика характерна для стабильной систолодиастолической артериальной гипертензии, преимущественно в ночные часы. Значимого повышения уровня гормонов щитовидной железы и надпочечников не выявлено. По данным дуплексного исследования правая почечная артерия на протяжении диффузно изменена с гемодинамически значимым стенозом — линейная скорость кровотока до 600 см/с, левая почечная артерия диффузно изменена с неравномерным утолщением стенок и ускорением кровотока, но без гемодинамически значимого стенозирования. По данным мультиспиральной компьютерной томографии брюшной полости с контрастированием выявлены признаки стеноза правой почечной артерии до 83% (правая почечная артерия диаметром 0,6 см, на расстоянии 0,6 см от устья сужена); признаки стеноза нижней брыжеечной артерии до 50%; КТ-картина аномалии развития — самостоятельное отхождение от аорты печеночной артерии. Пациентке было назначено лечение в виде амлодипина 2,5 мг в сутки, на фоне которого отмечалось уменьшение частоты эпизодов повышения АД (до 1-2 раз в неделю) и снижение уровня АД (150-170/90-100 мм рт.ст). При подъеме АД принимает таблетку каптоприла под язык с положительным эффектом. Учитывая наличие стеноза правой почечной артерии и сохраняющуюся артериальную гипертензию, больная была направлена в клинику на оперативное лечение: ангиопластику с возможным стентированием правой почечной артерии.
В анамнезе обращали на себя внимание следующие факты. С 15 лет пациентка стала отмечать синкопальные состояния с частотой 1-2 раз в год. Наблюдались два варианта обмороков. Первый развивался абсолютно внезапно, на фоне полного благополучия, без предвестников, продолжался от 2 до 5 минут, с последующим быстрым восстановлением сознания; при этом больная падала, судорог, мочеиспускания и прикуса языка не наблюдалось. Второй возникал на фоне головокружения и общей слабости, с постепенным восстановлением сознания: сначала слуха, а потом зрения. По поводу потерь сознания наблюдалась и обследовалась у невролога. Однако в ходе обследования, которое включало в себя магнитнорезонансную томографию головного мозга, электроэнцефалографию, ультразвуковую диагностику брахиоцефальных артерий, выяснить причину синкопальных состояний не удалось. В детстве часто болела воспалительными заболеваниями верхних дыхательных путей (ринит, синуситы, отиты). В возрасте 12 лет заметила снижение слуха. Осмотрена сурдологом, диагностирована левосторонняя хроническая сенсоневральная тугоухость 3 степени, дисфункция слуховых труб, хронический вазомоторный ринит. В течение многих лет пользуется интраназальными каплями, чаще всего, «нафтизином» (1 флакон использует в течение 1-2 дней). За последние 7 лет пациентке неоднократно проводилось суточное мониторирование ЭКГ (СМ-ЭКГ). При анализе ежегодных заключений СМ-ЭКГ в течение последних 3 лет обращала на себя внимание длительная регистрация удлинённого корригированного QT-интервала свыше 450 мс: от 64% до 87% времени мониторирования. На одном из мониторов ЭКГ регистрировались эпизоды миграции водителя ритма по предсердиям, замещающего предсердного ритма. В частности, по результатам последнего СМ-ЭКГ, выполненного на амбулаторном этапе, регистрировался синусовый ритм со средней ЧСС 83 в 1 минуту, эпизоды предсердного ритма, желудочковая экстрасистолия 3 градации по M.Ryan. За сутки наблюдалось удлинение корригированного QT-интервала свыше 450 мс (до 556 мс) в течение 14 часов 49 минут — 87% времени (рис. 1).

Интервал QTс за всё время наблюдения принимал значения от 355 мс до 556 мс (ср 474 мс), во время бодрствования от 355 мс до 556 мс (ср 468 мс), во время физических нагрузок от 431 мс до 470 мс (ср 446 мс), во время сна от 372 мс до 550 мс (ср 480 мс). Кроме того, зарегистрировано изменение реполяризации в виде отрицательных или двухфазных Т в грудных отведениях с V1 по V5 в состоянии покоя и положительных Т в тех же отведениях при выполнении физической нагрузки (рис. 2).

Эпидемиологический и аллергологический анамнез без особенностей. Наследственный анамнез со стороны матери не отягощён, однако обращал на себя внимание ее акушерско-гинекологический анамнез: первая беременность завершилась мертворождением, а вторая — рождением девочки с синдромом Дауна, причина смерти которой в грудном возрасте остаётся неизвестной. Наша пациентка появилась на свет в результате родоразрешения третьей беременности. Наследственный анамнез со стороны отца не отягощен (со слов матери больной). Пациентка никогда не курила, алкогольные и наркотические средства не употребляла. Объективный статус: состояние удовлетворительное, сознание ясное, положение активное. Телосложение нормостеническое. Рост 164 см, вес 60 кг, индекс массы тела 22,3. Кожные покровы физиологического цвета. Обращали на себя внимание дистопия передних зубов и дисплазия эмали. Периферических отеков нет. Пульс ритмичный, удовлетворительного наполнения и напряжения, с частотой 110 в 1 минуту. Границы относительной сердечной тупости не расширены. Тоны сердца ясные, ритмичные, шумов нет. АД 135/80 мм рт.ст. с обеих сторон. Частота дыхательных движений 16 в 1 минуту. При перкуссии легких определяется ясный легочный звук. Дыхание везикулярное, хрипов нет. Язык влажный, чистый. Живот мягкий, безболезненный. Печень и селезенка не увеличены. Почки не пальпируются. Поколачивание по пояснице безболезненное. В клиническом и биохимическом анализах крови и общем анализе мочи, выполненных в стационаре, па- тологических изменений не было. На ЭКГ при поступлении в нашу клинику: синусовый ритм с частотой сердечных сокращений 64 в 1 минуту, P = 100 мс, PQ = 130 мс, QRS = 90 мс, QT = 420 мс, RR = 940 мс, QTc = 433 мс, частичная блокада правой ножки пучка Гиса (рис. 3).

Обращало на себя внимание изменение процессов реполяризации в отведениях V2-V4 в виде «-» или «+/-» зубцов Т. Через неделю в стационаре на ЭКГ покоя был зарегистрирован предсердный ритм с частотой сердечных сокращений 53 в 1 минуту (QTс = 450 мс). При сравнении с ЭКГ при поступлении — реполяризация без изменений. Эпизоды предсердного ритма регистрировались у пациентки раньше, до стационара, как на обычной ЭКГ, так и при СМ-ЭКГ. По данным СМ-ЭКГ (без терапии), выполненного в стационаре: синусовый ритм в течение времени наблюдения, с частотой сердечных сокращений от 48 до 156 (средняя 74) в 1 минуту. Зарегистрированы следующие аритмии: одиночные наджелудочковые экстрасистолы с предэктопическим интервалом 541 мс, днем — 1, ночью — нет. Паузы за счет синусовой аритмии продолжительностью от 778 до 1588 (в среднем 1070) мс, всего — 12 (1 в час), днем- 9, (1 в час) ночью — 3. Ишемические изменения ЭКГ не обнаружены. В течение суток наблюдалось удлинение QTc свыше 450 мс в течение 13 часов 57 минут (64% времени). Интервал QTс за всё время наблюдения принимал значения от 424 мс до 541 мс (средний 498 мс), во время бодрствования от 424 мс до 533 мс (средний 486 мс), во время ФН от 455мс до 518 мс (средний 486 мс), во время сна от 475 мс до 541 мс (средний 506 мс). Вариабельность ритма сердца: соотношение высокочастотного и низкочастотного компонентов сбалансировано, ночной прирост высокочастотной составляющей вариабельности отсутствует. По данным эхокардиографии, выполненной в стационаре, патологических изменений не выявлено. По данным дуплексного сканирования сосудов почек, выполненного в стационаре: диаметр аорты на уровне почечных артерий 16 мм; в инфраренальном отделе 15 мм, стенки ровные, не утолщены, просвет не сужен; слева диаметр почечной артерии в области устья 4,2 мм, кровоток не ускорен (V=105 см/м); справа в дистальной части почечной артерии просвет неравномерно сужен, ускорение кровотока с Vmax≈540см/с.
Заключение: стеноз правой почечной артерии в дистальной части 80%. По данным УЗИ почек, выполненного в стационаре: признаки простой мелкой кисты левой почки, диффузных изменений правой почки. Размеры обеих почек нормальные. Таким образом, у больной имелась артериальная гипертензия, в генезе которой не исключался вазоренальный механизм, обусловленный, вероятнее всего, фибромышечной дисплазией. Больной был назначен метопролола тартрат 12,5 мг 2 раза в сутки, рекомендованы соблюдение физиологического режима сон-бодрствование и постепенное уменьшение вплоть до отмены интраназальных адреномиметиков. За время госпитализации существенного изменения режима дозирования интраназальных сосудосуживающих препаратов не удалось достигнуть, но с большим успехом получилось соблюдать физиологический режим сон- бодрствование. Повышение АД до 140-150/80-90 мм рт. ст. наблюдалось только в начале госпитализации. На подобранной дозе β-блокатора были достигнуты цифры АД 110-120/70-80 мм рт. ст. и частота сердечных сокращений 55-75 в 1 минуту. Пациентка была консультирована нефрологом: учитывая возраст, отсутствие факторов риска атеросклероза, выявленные аномалии строения других сосудов, стеноз правой почечной артерии был расценен как фибромышечная дисплазия почечной артерии. Ввиду стабильного АД на фоне монотерапии, нормальных размеров правой почки и нормальной функции почек (креатинин =79 мкмоль/л, скорость клубочковой фильтрации = 92 мл/мин/1,73 м2), было принято решение воздержаться в настоящее время от эндоваскулярного лечения стеноза почечной артерии. Учитывая наличие синкопальных состояний в анамнезе, удлинение корригированного QT-интервала по данным СМ-ЭКГ и нарушение процессов реполяризации по данным ЭКГ был поставлен диагноз СУИ QT. Состояние больной в стационаре оставалось стабильным, эпизодов потери сознания не наблюдалось, желудочковых нарушений ритма не зарегистрировано. После выписки из стационара для дальнейшего дообследования и лечения пациентка была направлена на консультацию к врачу-аритмологу в Северо-Западный центр диагностики и лечения аритмий Научно-клинического и образовательного центра «Кардиология» СПбГУ. Для подтверждения наследственного СУИ QT в международной генетической лаборатории «Health in Code» (Ла-Корунья, Испания), специализирующейся на молекулярно-генетической диагностике наследственных заболеваний сердца, пациентке было выполнено тестирование, включавшее в себя поиск мутаций в 13 известных генах, связанных с синдромом удлинённого QT (СACNA1C, KCNE1, KCNE2, KCNH2, KCNJ2, KCNQ1, RYR2, SCN5A и др.). Однако генетический вариант наследственного СУИ QT идентифицировать не удалось. Методом геномного секвенирования нового поколения (NGS) у пациентки выявлена мутация в гене MYBPC3, ассоциированная с развитием гипертрофической кардиомиопатии. Пациентке было предложено имплантировать подкожный «регистратор событий» для длительного наблюдения, от чего она отказалась. Больной были даны рекомендации после выписки из стационара продолжить приём β-блокаторов в максимально переносимых дозах в сочетании с препаратами магния, контроль АД, исключить прием интраназальных капель с симпатомиметическим эффектом. На фоне перечисленных лечебно-профилактических мероприятий в течение 1 года синкопальные состояния не рецидивировали, больную не беспокоило повышение АД, интервал QTc уменьшился, но не нормализовался. Наблюдение за пациенткой продолжается.
Обсуждение
Диагноз СУИ QT у молодой пациентки 22 лет был установлен во время плановой госпитализации по поводу артериальной гипертензии. Стеноз правой почечной артерии был подтверждён и, вероятнее всего, обусловлен врождённой аномалией — фибромышечной дисплазией. Однако взаимосвязи между повышением АД и стенозом почечной артерии выявлено не было. При наблюдении за больной отмечалась эмоциональная лабильность, была замечена четкая взаимосвязь повышения АД с психоэмоциональным напряжением. Также нельзя было исключить влияние на АД безконтрольного ежедневного длительного интраназального применения симпатомиметиков («нафтизина») в больших дозах. Кроме того, ингибитор ангиотензинпревращающего фермента каптоприл хорошо снижал АД и положительный эффект был получен на минимальной гипотензивной терапии β-блокаторами. Поэтому больной не проводилась хирургическая коррекция стеноза почечной артерии, а было рекомендовано мониторирование функции почек и уровня АД, соблюдение физиологического режима сон-бодрствование, отмена интраназальных капель, обладающих симпатомиметическим эффектом, и подбор гипотензивной терапии. Прогностически более серьезным диагнозом представлялся выявленный СУИ QT: по модифицированной шкале P.J.Schwartz суммарно, как минимум, 4 балла (QTc более 480 мс — 3 балла, синкопе вне нагрузки — 1 балл) [1, 2, 10]. Кроме того, не представляется возможным однозначно трактовать наличие тугоухости (не исключена взаимосвязь с перенесёнными отитами), неизвестна причина смерти сестры пациентки в младенческом возрасте. В связи с имеющимися синкопальными состояниями, возникшими в детстве, пациентка наблюдалась и обследовалась у врачей, в том числе у неврологов. Была проведена комплексная диагностика, позволившая исключить неврологические причины обмороков. Больной неоднократно регистрировалась ЭКГ и проводилось СМ-ЭКГ в течение 7 лет, при анализе которых оставался недооценённым факт удлинённого интервала QT и изменений процессов реполяризации в стандартных и, особенно, в грудных отведениях V1-V4. Примечательным фактом истории болезни пациентки является длительное применение α-адреномиметиков в больших дозах. В литературе есть единичные сведения об их возможном влиянии на реполяризацию миокарда и на развитие аритмий [14]. Не представляется возможным полностью исключить участие α-адреномиметиков в манифестации СУИ QT. С клинико-электрокардиографической точки зрения характер изменения зубца Т в грудных отведениях соответствовал второму типу СУИ QT, но условия возникновения синкопальных состояний более соответствовали третьему. Несмотря на то, что у пациентки не был выявлен ни один из известных генетических вариантов СУИ QT, это не отрицает возможное наличие других, пока еще неизвестных генных мутаций. Весьма интересно выявленное сочетание с мутацией в гене MYBPC3, связанной с развитием гипертрофической кардиомиопатии. В литературе имеются единичные описания таких ассоциаций [15, 16].
Литература
1. Бокерия, О.Л., Санакоев М.К. Синдром удлинённого QT-интервала. Неинвазивная аритмология. — 2015. — Т12. — N2. — С. 114-127.
2. Priori S.G., Blomstrцm-Lundqvist C., Mazzanti A. et al. ESC 2015 guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. European Heart Journal. — 2015. — Vol. 36, N 41. — P. 2793-2867. doi: 10.1093/eurheartj/ehv316.
3. Ильдарова Р.А., Школьникова М.А. Современная тактика ведения пациентов молодого возраста с синдромом удлиненного интервала QT: от ранней диагностики к имплантации кардиовертера дефибриллятора и мониторингу маркеров риска внезапной смерти. Сибирский медицинский журнал. — 2015. — Т30. — N1. — С. 28-35.
4. Liu J.F., Jons C., Moss A.J. et al. International Long QT Syndrome Registry. Risk factors for recurrent syncope and subsequent fatal or near-fatal events in children and adolescents with long QT syndrome. JACC. — 2011. — № 57. — Р. 941-950. doi: 10.1016/j.jacc.2010.10.025.
5. Гордеева М.В., Велеславова О.Е., Батурова М.А. и др. Внезапная ненасильственная смерть молодых людей (ретроспективный анализ). Вестник аритмологии. — 2011. — Т65. — С.25-32.
6. Гордеева М.В., Митрофанова Л.Б., Пахомов А.В. и др. Внезапная сердечная смерть молодых людей. Вестник аритмологии. — 2012. — Т68. — С.34-44.
7. Баранов А.А., Школьникова М.А., Ильдарова Р.А. и др. Синдром удлинённого QT. Клинические рекомендации. — М., 2016. — 25 с.
8. Bezzina C.R., Lahrouchi N., Priori S.G. Genetics of Sudden Cardiac Death // Circ. Res. — 2015. — Vol. 12, № 116. — P. 1919-1936. doi: 10.1161/CIRCRESAHA.116.304030.
9. Priori S.G., Wilde A.A., Horie M. et al. HRS/EHRA/ APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes //Heart Rhythm. — 2013. — Vol. 10, № 12. — Р. 1932-1963. doi: 10.1016/j.hrthm.2013.05.014.
10. Бокерия Л.А., Бокерия О.Л., Голухова Е.З. и др. Желудочковые аритмии. Клинические рекомендации. — М.: «ФГБУ ННПЦССХ им. А.Н.Бакулева» МЗ РФ, 2017. — 50 с.
11. Макаров Л.М., Рябыкина Г.В., Тихоненко В.М. и др. Национальные российские рекомендации по применению методики холтеровского мониторирования в клинической практике. Российский кардиологический журнал — 2014 — N2 (106) — С. 6-71.
12. Ревишвили А.Ш., Неминущий Н.М., Баталов Р.Е. и др. Всероссийские клинические рекомендации по контролю над риском внезапной остановки сердца и внезапной сердечной смерти, профилактике и оказанию первой помощи. Вестник аритмологии — 2017 — Т89 — С. 2-104.
13. Голицын С.П., Кропачёва Е.С., Майков Е.Б. и др. Наследственный (врожденный) синдром удлиненного интервала QT. Диагностика и лечение нарушений ритма сердца и проводимости. Клинические рекомендации. Общество специалистов по неотложной кардиологии. — М., 2013. — С. 154-170.
14. Urrutia, J., Alday A., Gallego M. et al. Mechanisms of IhERG/IKr Modulation by α1-Adrenoceptors in HEK293 Cells and Cardiac Myocytes. Cell. Physiol. Biochem. — 2016. — Vol. 40, № 6. — P. 1261-1273. doi: 10.1159/000453180.
15. Vilsendorf D.M., Strunk-Mueller C., Gietzen F.H., Kuhn H. Simultaneous hypertrophic obstructive cardiomyopathy and long QT syndrome: a potentially malignant association. Z Kardiol. 2002 Jul;91(7):575-80.
16. Boczek N.J., Ye D., Jin F. et al. Identification and Functional Characterization of a Novel CACNA1C-Mediated Cardiac Disorder Characterized by Prolonged QT Intervals With Hypertrophic Cardiomyopathy, Congenital Heart Defects, and Sudden Cardiac Death. Circ Arrhythm Electrophysiol. 2015 Oct;8(5):1122-32. doi: 10.1161/CIRCEP. 115.002745.
«Вестник аритмологии», № 94, 2018
Источник: spbpmc.ru
Наследственный (врождённый) синдром удлиненного интервала QT
Введение
Наследственный синдром удлинённого интервала QT (СУИQT, в англоязычной литературе — Long QT syndrome — LQTS или LQT) является наиболее частым и наиболее изученным из данных заболеваний, проявляющимся удлинением интервала QT на ЭКГ [при отсутствии других вызывающих это изменение причин], рецидивирующими синкопальными и пресинкопальными состояниями вследствие пароксизмов TdP, а также случаями внезапной сердечно-сосудистой смерти.
Эпидемиология
Распространенность заболевания в популяции составляет около 1:2000 новорождённых. Следует отметить, что эти данные учитывают только случаи «явного» увеличения продолжительности интервала QT, выявленного при регистрации ЭКГ. У некоторых больных симптомы заболевания могут полностью отсутствовать в течение всей жизни и проявляться лишь при возникновении дополнительных факторов, способствующих удлинению интервала QT, например гипокалемии, или при назначении лекарственных препаратов, способных увеличивать длительность интервала QT. Кроме того, удлинение интервала QT может носить преходящий характер, следовательно, истинная распространённость данного заболевания в популяции, по-видимому, ещё больше.
Этиология
Основной причиной СУИQT является дисфункция ионных каналов и насосов, приводящая к увеличению продолжительности фаз реполяризации кардиомиоцитов. Нарушение функции ионных каналов может быть обусловлено мутацией в генах основных порообразующих α-субъединиц, добавочных субъединиц, осуществляющих регуляцию их функции, белков-переносчиков, необходимых для транспортировки молекул, а также вспомогательных белков, опосредующих «встраивание» молекул в биологические мембраны и взаимодействие с клеточными структурами.
Классификация и клинические проявления
В табл. 1 представлена генетическая классификация синдрома удлиненного интервала QT: указаны гены, мутации в которых обнаруживают при соответствующих типах заболевания, кодируемые данными генами белки и изменения ионных токов, приводящие к удлинению фаз реполяризации. Следует отметить, что при проведении молекулярно-генетического скрининга больных СУИQT примерно в 25% случаев генетические нарушения не обнаруживают, что позволяет ожидать в дальнейшем выявление новых генетических мутаций, приводящих к возникновению заболевания.
Таблица 1. Молекулярно-генетические типы наследственного синдрома удлинённого интервала QT
Описаны следующие фенотипические формы синдрома удлиненного интервала QT: синдром Романо–Уорда (Romano–Ward), синдром Джервелла и Ланге–Нильсена (Jervell and Lange-Nielsen), синдром Андерсена–Тавила (Andresen–Tawil) и синдром Тимоти (Timothy).
Наиболее распространённая форма заболевания с аутосомно-доминантным типом наследования — синдром Романо–Уорда (Romano–Ward), характерными клиническими проявлениями которого являются увеличение продолжительности интервала QT, рецидивирующие синкопальные состояния, чаще всего обусловленные полиморфной желудочковой тахикардией (ЖТ) типа пируэт, и наследственный характер заболевания. Более 90% случаев синдрома Романо–Уорда представлены СУИQT 1-го (СУИQT1), 2-го (СУИQT2) и 3-го (СУИQT3) типов, имеющих особенности клинических и электрокардиографических проявлений (табл. 2, рис. 1).
Таблица 2. Клиническая характеристика основных типов наследственного синдрома удлинённого интервала QT.
 Рис. 1. Изменения ЭКГ при различных типах наследственного синдрома удлиненного интервала QT: (А) — широкая гладкая волна T при СУИQT1; (Б) — двухфазная T-волна при СУИQT2; (В) — низкоамплитудная и укороченная T-волна с удлиненным, горизонтальным ST-сегментом при СУИQT3.
Рис. 1. Изменения ЭКГ при различных типах наследственного синдрома удлиненного интервала QT: (А) — широкая гладкая волна T при СУИQT1; (Б) — двухфазная T-волна при СУИQT2; (В) — низкоамплитудная и укороченная T-волна с удлиненным, горизонтальным ST-сегментом при СУИQT3.
СУИQT1 — наиболее распространенный тип синдрома, обусловленный мутацией в гене KCNQ1, кодирующем α-субъединицу калиевого канала, генерирующего ток IKs, который является основным током реполяризации при высокой частоте сердечного ритма. Снижение силы IKs приводит к недостаточному укорочению интервала QT при нарастании частоты сердечных сокращений. По этим причинам больным СУИQT1 характерно возникновение TdP на фоне физической нагрузки (рис. 2) и эмоционального стресса. Особенностью ЭКГ при СУИQT1 является удлиненная и гладкая волна Т (см. рис. 1А). 
Рис. 2. Развитие пароксизма полиморфной желудочковой тахикардии типа Torsade de Pointes на фоне физической нагрузки у больной синдромом Романо–Уорда (фрагмент непрерывной записи суточного мониторирования ЭКГ по Холтеру).
Причиной СУИQT2 является мутация в гене KCNH2, кодирующем α-субъединицу калиевого канала Kv11.1, генерирующего ток IKr. При СУИQT2 пароксизмы TdP могут возникать как во время нагрузки, так и в покое. Характерным провоцирующим фактором является резкий громкий звук. На ЭКГ больных СУИQT2 регистрируют непротяженную, двухфазную волну Т (см. рис. 1Б).
СУИQT3 является менее распространённой формой заболевания, обусловленной мутацией в гене SCN5A, кодирующем α-субъединицу натриевого канала, что приводит к нарушению инактивации натриевых каналов, продолжающемуся вхождению ионов Na+ в клетку и увеличению продолжительности реполяризации кардиомиоцитов. TdP у больных СУИQT3 возникают на фоне брадикардии, преимущественно во время сна. Физические нагрузки, напротив, переносятся хорошо и сопровождаются укорочением интервала QT. Характерной особенностью ЭКГ у данных больных является удлиненный сегмент ST с отсроченным началом непродолжительной низкоамплитудной волны Т (см. рис. 1В).
Существенно реже встречается аутосомно-рецессивная форма заболевания (синдром Джервелла и Ланге–Нильсена), для которой характерны врождённая нейросенсорная тугоухость, более выраженное увеличение длительности интервала QT и большая частота опасных для жизни желудочковых аритмий. Заболевание обусловлено мутациями в генах KCNQ1 или KCNE2, кодирующих основную и добавочную субъединицы потенциал-зависимых калиевых каналов Kv7.1, приводящими к снижению силы тока IKs.
Синдром Андерсена–Тавила — редкая форма заболевания, при которой удлинение интервала QT сопровождается появлением волны U, пароксизмами как полиморфной желудочковой тахикардии типа TdP, так и двунаправленной желудочковой тахикардии. В 60% случаев заболевание обусловлено мутацией в гене KCNJ2, кодирующем α-субъединицу калиевых каналов аномального входящего выпрямления Kir2.1, генерирующих ток IK1, сила которого снижается. В 40% случаев генетический дефект в настоящее время обнаружить не удаётся. Характерные экстракардиальные проявления заболевания, такие как, аномалии развития костной системы (низкорослость, микрогнатия, большое расстояние между глазницами, низкое расположение ушных раковин, сколиоз, клинодактилиия), гипокалемия и периодический калий-зависимый паралич, присутствуют не у всех больных. Синдром Андерсена–Тавила — заболевание с аутосомно-доминантным типом наследования, однако семейный характер заболевания прослеживается далеко не всегда, в связи с трудностями диагностики, неспецифическими клиническими проявлениями заболевания и неполной пенетрантностью мутантных генов. До 50% случаев заболевания обусловлены мутацией de novo
Синдром Тимоти — крайне редкая форма СУИQT, обусловленная мутацией в гене CACNA1c, кодирующем α-субъединицу кальциевых каналов CaV1.2. При данном синдроме отмечают наиболее выраженное удлинение интервалов QT и QTc (до 700 мс), сопровождающееся крайне высоким риском внезапной сердечно-сосудистой смерти (средняя продолжительность жизни составляет 2,5 года). До 60% больных имеет различные врождённые пороки сердца [открытый артериальный проток, тетраду Фалло, открытое овальное окно и дефекты межжелудочковой перегородки] и различные нарушения проводимости (характерны преходящая и постоянная формы АВ блокады II степени с проведением на желудочки 2:1). Среди экстракардиальных проявлений заболевания описаны когнитивные нарушения (задержка психомоторного развития, аутизм), гипогликемия, иммунодефициты, аномалии строения лица (сглаженность носогубной складки, низкое расположение ушных раковин), а также частичное или полное сращение пальцев кистей и стоп (синдактилия). Синдром Тимоти наследуется по аутосомно-доминантному типу, однако подавляющее большинство случаев заболевания обусловлено мутацией de novo.
Диагностика
Критерии, применяемые для постановки диагноза наследственного СУИQT, предложенные J.P. Schwarz, представлены в табл. 3.Таблица 3. Диагностические критерии наследственного синдрома удлинённого интервала QT (в соответствии с изменениями 2006г.).
Наследственный СУИQT диагностируют в случае, если сумма баллов составляет ≥3,5, при наличии подтверждённой молекулярно-генетическими методами мутации, приводящей к увеличению продолжительности интервала QT, при повторной регистрации на ЭКГ удлинения интервала QTc ≥600 мс в случае отсутствия других причин удлинения интервала QT.
Диагноз наследственного СУИQT может быть также поставлен при повторной регистрации на ЭКГ удлинения интервала QTc до 480–499 мс у пациентов с синкопальными состояниями неясного генеза, при отсутствии генетической мутации и других причин удлинения интервала QT.
Методы молекулярно-генетической диагностики имеют большое значение в диагностике СУИQT и определении прогноза больных. При проведении комплексных генетических анализов мутации удаётся обнаружить приблизительно у 75% больных, поэтому отрицательный результат генетического анализа не позволяет полностью исключить диагноз СУИQT.
Проведение комплексного генетического анализа на выявление возможных мутаций в генах KCNQ1 KCNH2 и SCN5A (СУИQT 1, 2 и 3-го типов — наиболее распространённые формы заболевания) рекомендовано всем больным, имеющим клинические проявления СУИQT, отягощённый семейный анамнез и удлинение интервала QTc, зарегистрированное на ЭКГ в покое или при проведении провокационных диагностических проб, а также всем пациентам, не имеющим характерных СУИQT симптомов, при регистрации на ЭКГ удлинения интервала QTc >500 мс при отсутствии других возможных причин удлинения интервала QT.
Проведение комплексного генетического анализа на выявление возможных мутаций в генах KCNQ1 KCNH2 и SCN5A может иметь смысл у пациентов, не имеющих характерных СУИQT симптомов, при регистрации на ЭКГ удлинения интервала QTc >480 мс при отсутствии других возможных причин удлинения интервала QT.
В случае обнаружения у больного СУИQT генетической мутации проведение скрининга, направленного на выявление этой мутации, рекомендовано всем близким родственникам, даже при отсутствии у них характерных этому заболеванию клинических проявлений и изменений ЭКГ.
Поскольку удлинение интервала QT может носить преходящий характер, в диагностике заболевания имеют значение продолжительная регистрация ЭКГ (например, суточное мониторирование ЭКГ по Холтеру; данный метод особенно информативен у больных СУИQT 2-го и 3-го типов, поскольку у больных этими формами заболевания наибольшее увеличение длительности интервала QT отмечают обычно в ночное время) и провокационные пробы.
В целях обеспечения безопасности пациента и повышения диагностической значимости, существует ряд требований, которые должны быть учтены при проведении данных диагностических исследований. Поскольку в ходе исследований возможна индукция опасных для жизни нарушений ритма сердца, все провокационные пробы должны проводиться опытным медицинским персоналом при непрерывной регистрации ЭКГ (следует производить мониторирование ЭКГ до полной нормализации индуцированных в ходе исследования изменений ЭКГ, при проведении фармакологических провокационных проб — не менее 30 мин после окончания введения препарата) и систематическом измерении АД больного, в условиях непосредственной доступности необходимого для сердечно-легочной реанимации оборудования [включая дефибриллятор] и возможности незамедлительного вызова врача-реаниматолога. Проведение нагрузочных проб должны осуществлять физически тренированные сотрудники, способные уберечь пациента от падения в случае возникновения гемодинамического коллапса при индукции желудочковых аритмий.
Провокационные пробы далеко не всегда вызывают типичные для конкретного заболевания изменения ЭКГ. Пограничные изменения не должны расцениваться как диагностически значимые. В случае пограничных изменений ЭКГ или отрицательного результата исследования при большой вероятности заболевания (характерная клиническая картина, результаты генетических исследований) целесообразно проведение другой провокационной пробы.
Для выявления СУИQT используют следующие провокационные пробы.
- Активная ортостатическая проба. Оценка динамики интервала QT при регистрации ЭКГ в ходе ортостатической пробы обладает диагностической значимостью, позволяя в ряде случаев выявить больных СУИQT. После перехода в вертикальное положение отмечается умеренное увеличение частоты синусового ритма, при этом у здоровых пациентов длительность интервала QT уменьшается, а у больных СУИQT (особенно 2-го типа) продолжительность интервала QT уменьшается менее существенно, не изменяется или увеличивается.
- Проба с дозированной физической нагрузкой на велоэргометре или тредмиле. Наиболее информативна оценка длительности интервала QT в период восстановления. Длительность интервала QTc >445 мс в конце периода восстановления (спустя 4 минуты после окончания нагрузки) характерна для больных СУИQT 1-го и 2-го типов. При этом длительность интервала QTc <460 мс в начале периода восстановления позволяет отличить больных СУИQT 2-го типа от больных СУИQT 1-го типа.
Фармакологические провокационные пробы.
- Проба с адреналином (эпинефрином). Позволяет выявить больных СУИQT1, поскольку при этой форме заболевания при проведении инфузии адреналина отмечается парадоксальное увеличение длительности интервала QT. Предложены 2 протокола проведения данной пробы: протокол Шимицу (Schimizu), в ходе которого вслед за болюсным введением осуществляется кратковременная инфузия адреналина, и протокол Мейо (Mayo), в соответствии с которым осуществляется внутривенная инфузия постепенно увеличиваемой дозы адреналина. Оба этих протокола обладают сопоставимыми чувствительностью и специфичностью, хорошо переносятся и редко сопровождаются нежелательными реакциями. Проба расценивается как положительная при увеличении длительности интервала QT >30 мс на фоне инфузии адреналина в дозе до 0,1 мкг/кг в мин. Следует отметить, что правильное измерение длительности QT на фоне инфузии адреналина часто затруднено изменениями морфологии зубцов T, особенно если при этом регистрируются высокоамплитудные волны U. Сопутствующий прием β-адреноблокаторов снижает диагностическую значимость пробы. Среди нежелательных реакций, возникающих на фоне инфузии адреналина, необходимо упомянуть артериальную гипертензию и индукцию опасных для жизни нарушений ритма. Диагностическое исследование должно быть прекращено при повышении систолического АД >200 мм рт.ст. (или при меньших значениях в случаях, если артериальная гипертензия сопровождается выраженными клиническими проявлениями), возникновении рецидивирующих неустойчивых пробежек или индукции устойчивого пароксизма ЖТ. В случае возникновения клинически значимых нежелательных эффектов целесообразно применение короткодействующих β-адреноблокааторов, вводимых внутривенно.
- Проба с аденозином. Больным СУИQT характерно увеличение продолжительности интервалов QT >410 мс и QTc >490 мс, регистрируемые во время минимальной частоты сердечных сокращений при индуцированной аденозином брадикардии. В настоящее время диагностическая значимость данной пробы изучена на ограниченном количестве больных генетически подтвержденным СУИQT, поэтому интерпретация полученных в ходе исследования результатов требует осторожности.
Источник: MedSpecial.ru
Признаки и симптомы
Синдром удлиненного интервала QT как правило диагностируется после того, как у человека случается приступ обморока или сердечный приступ. В некоторых ситуациях это состояние диагностируется после внезапной смерти члена семьи. У некоторых людей диагноз ставится, когда ЭКГ показывает удлинение интервала QT.
Диагностика
Результаты физического обследования как правило не указывают на диагноз синдрома удлиненного интервала QT, но у некоторых людей могут обнаруживаться чрезмерная брадикардия для своего возраста, а у некоторых пациентов может наблюдаться потеря слуха (врожденная глухота), что указывает на возможность синдрома Джервелла и Ланге-Нильсена. Скелетные аномалии, такие как низкорослость и сколиоз наблюдаются при синдроме Андерсена. Врожденные пороки сердца, когнитивные и поведенческие проблемы, заболеваний опорно-двигательного и иммунной дисфункции могут наблюдаться при синдроме Тимоти.
Исследования
Диагностические исследования у людей с подозрением на синдром включают в себя следующие:
- Измерение уровня калия и магния в сыворотке;
- Исследование функции щитовидной железы;
- Фармакологические провокационные пробы эпинефрином или изопротеренолом;
- Электрокардиография больного и членов семьи;
- Генетическое тестирование больного и членов семьи.
Удлинённый скорректированный интервал QT в ответ на тест, когда пациент стоит, который связан с повышенным симпатическим тоном, может дать больше диагностической информации у больных, имеющих синдром. Это увеличение QT в результате положения стоя может сохраняться даже после того, как частота сердечных сокращений вернется в норму.
Лечение
Никакое лечение не может устранить причину синдрома удлиненного интервала QT. Антиадренергические терапевтические меры (например, использование бета-адреноблокаторов, левосторонняя церукотракальная стеллектомия) и аппаратная терапия (например, использование кардиостимуляторов, имплантируемых кардиовертер-дефибрилляторов) направлены на снижение риска и летальности сердечных приступов.
Медикаментозное
Бета-адренергические блокирующие агенты являются лекарственными препаратами, которые могут назначаться для лечения синдрома и включают в себя следующие препараты:
- Надолол
- Пропранолол
- Метопролол
- Атенолол
При этом Надолол является предпочтительным бета-блокатором, который должен использоваться в дозе 1-1,5 мг / кг / день (один раз в день для больных старше 12 лет, два раза в день для более молодых людей).
Хирургическое лечение
Хирургическое вмешательство у людей, страдающим синдромом удлиненного интервала QT может включать следующие процедуры:
Имплантация кардиовертер-дефибрилляторов
Размещение кардиостимулятора
Левая цервико торакальная стеллэктомия
Люди, у которых наблюдается синдром, должны избегать участия в спортивных соревнованиях, выполнять тяжелые физические упражнения и стараться не избегать эмоциональных стрессов.
Кроме того, также следует избегать следующих препаратов:
Анестетики или лекарства от астмы (например, адреналин)
Антигистамины (например, дифенгидрамин, терфенадин и астемизол)
Антибиотики (например, эритромицин, триметоприм и сульфаметоксазол, пентамидин)
Сердечные препараты (например, хинидин, прокаинамид, дисопирамид, соталол, пробукол, бепридил, дофетилид, ибутилид)
Желудочно-кишечные препараты (например, цизаприд)
Противогрибковые препараты (например, кетоконазол, флуконазол, итраконазол)
Психотропные препараты (например, трициклические антидепрессанты, производные фенотиазина, бутирофеноны, бензизоксазол, дифенилбутилпиперидин)
Калий-теряет лекарства (например, индапамид, другие диуретики, лекарства от рвоты / диареи)
Причины
Интервал QT представляет собой продолжительность активации и восстановления желудочкового миокарда. Продолжительное восстановление от электрического возбуждения увеличивает вероятность дисперионной рефрактерности, когда некоторые части миокарда могут быть невосприимчивыми к последующей деполяризации.
С физиологической точки зрения дисперсия происходит при реполяризации между тремя слоями сердца, а фаза реполяризации имеет тенденцию к увеличению в среднем миокарде. Вот почему T-волна обычно широкая, а интервал Tpeak-Tend (Tp-e) представляет собой трансмуральную дисперсию реполяризации. При длительном синдроме QT она увеличивается и создает функциональную возможность для трансмуральной повторной инициации.
Гипокалиемия, гипокальциемия и использование петлевых диуретиков являются факторами риска удлинения интервала QT.
Синдром делится на два клиинческих варианта – синдром Романо-Уорда (семейным происхождением с аутосомно-доминантным наследованием, продолжением QT и желудочковыми тахикардиями) или синдромом Джервелла и Ланга-Нильсена (с семейным происхождением с аутосомно-рецессивным наследованием, врожденной глухотой , удлинением QT и желудочковыми аритмиями). Описаны два других синдрома: синдром Андерсена и синдром Тимоти, хотя среди ученых ведутся некоторые споры о том, следует ли их включать в синдром удлиненного интервала QT.
Тахиаритмия Torsade de pointes
Удлинение QT может привести к полиморфной желудочковой тахикардии, что само по себе может привести к фибрилляции желудочков и внезапной сердечной смерти. Широко распространено мнение о том, что Torsade de pointes активируется реактивацией кальциевых каналов, реактивацией запаздывающего тока натрия или уменьшением тока в камере, который приводит к ранней последеполяризации, в состоянии с повышенной трансмуральной дисперсией реполяризации, обычно связанной с удлиненным интервалом QT, служит в качестве функционального вспомогательного субстрата для поддержания тахикардии.
Трансмуральная дисперсия реполяризации не только обеспечивает субстрат для механизма повторного входа, но также увеличивает вероятность ранней постдеполяризации, инициирующего события для тахиаритмии, за счет продления временного окна для каналов кальция, чтобы оно оставалось открытым. Любое дополнительное условие, которое ускоряет реактивацию кальциевых каналов (например, повышенный симпатический тон), увеличивает риск ранней постдеполяризации.
Генетика
Известно, что синдром удлиненного интервала QT вызван мутациями генов сердечных каналов калия, натрия или кальция; было идентифицировано по меньшей мере 10 генов. Основываясь на этом генетическом фоне, характеризуются 6 типов синдрома Романо-Уорда, 1 тип синдрома Андерсена и 1 тип синдрома Тимоти и 2 типа синдрома Джервелла-Ланге-Нильсена.
Синдром является результатом мутаций генов, кодирующих белки сердечного ионного канала, которые вызывают аномальную кинетику ионных каналов. Укороченное отверстие калиевого канала при 1 типе, 2 типе, 5 типе, 6 типе, 1 и 1 типе синдрома Джервелла-Ланге-Нильсена и замедленное закрытие натриевого канала в при 3 типе синдрома перезаряжает миокардиальную клетку положительными ионами.
У людей, имеющих синдром различные адренергические стимулы, включая физические упражнения, эмоции, громкий шум и плавание, могут ускорить аритмическую ответную реакцию. Однако аритмии могут возникать и без таких предшествующих состояний.
Удлинение интервала QT, вызванное лекарственными препаратами
Вторичное (индуцированное лекарством) удлинение интервала QT также может увеличить риск наступления желудочковых тахиаритмий и внезапной сердечной смерти. Ионный механизм аналогичен ионному механизму, наблюдаемому при врожденном синдроме (т. е. внутренней блокаде выброса калия).
В дополнение к лекарственным средствам, которые потенциально могут удлинить интервал QT, в этом расстройстве играют роль несколько других факторов. Важными факторами риска для удлинения QT, вызванного лекарственными средствами, являются следующие:
Электролитные нарушения (гипокалиемия и гипомагниемия)
Гипотермия
Аномальная функция щитовидной железы
Структурная болезнь сердца
Брадикардия
Лекарственное удлинение QT может также иметь генетический фон, состоящий из предрасположенности ионного канала к аномальной кинетике, вызванной мутацией или полиморфизмом гена. Однако данных недостаточно, чтобы утверждать, что у всех больных с удлинением QT, вызванным лекарственным средством, существует генетическая обусловленность синдрома.
Прогноз
Прогноз для людей, страдающих синдромом хороший, который лечится приемом бета-блокаторов (и при необходимости использованием других терапевтических мер). К счастью, эпизоды torsade de pointes обычно самоограничиваются у пациентов с синдромом QT; только около 4-5% сердечных приступов имеют смертельный исход.
Люди с высоким риском (т. е. те, у кого случалась остановка сердца или происходили повторные сердечные приступы, несмотря на бета-блокаторную терапию) значительно повышают риск внезапной сердечной смерти. Для лечения таких больных используется имплантируемый кардиовертер-дефибриллятор; прогноз после имплантации МКБ хороший.
Смертность, заболеваемость и ответные реакции на фармакологическое лечение различаются по различным типам синдрома.
Синдром удлиненного интервала QT может приводить к обморокам, внезапной сердечной смерти, что как правило происходит у здоровых молодых людей.
Несмотря на то, что внезапная сердечная смерть обычно возникает у больных с симптомами, она также может возникать при первом эпизоде обморока примерно у 30% больных . Это подчеркивает важность диагностики синдрома в предсимптомный период. В зависимости от типа присутствующей мутации внезапная сердечная смерть может иметь место во время физических нагрузок, эмоционального стресса, покоя или сна. 4 тип синдрома связан с пароксизмальной фибрилляцией предсердий.
Научные исследования показали улучшенную ответную реакцию на фармакологическое лечение с пониженной частотой внезапной сердечной смерти при 1 и 2 типах синдрома QT по сравнению с 3 типом.
Неврологический дефицит после прерванной остановки сердца может осложнить клинический курс пациентов после успешной реанимации.
Видео: Синдром удлиненного интервала QT
Источник: cardio-bolezni.ru
Показатели кардиограммы удлиненный интервал QT В последнее время стало беспокоить сердце, периодически как-то странно дергается (как буд-то очень быстро бьется), часто учащенный пульс, сделал кардиограмму в поликлинике, терапевт сказал, что очень хорошая кардиограмма, из показателей посмотрел только пульс и общий вид кардиограммы. Я сама заинтересовалась показателями и что они значат, нашла таблицу с нормами, и увидела, что у меня удлинен интервал QT, но терапевт на это не обратила внимания, нашла информацию, что удлинение этого интервала увеличивает риск желудочковой тахикардии и тахикардии типа "Пируэт", а они могут привести к фибрилляции желудочков и остановке сердца, но при этом это все успешно лечится… И вот у меня возник вопрос, то ли я слишком много всего начиталась, то ли терапевт это не считает серьезной проблемой… Другой терапевт послушав меня и не видя кардиограммы назначил Метополол и Мельдоний… И сейчас не знаю что делать, пить или не пить, беспокоится по этому поводу или нет, может сделать дополнительные исследования… Подскажите пожалуйста…Показатели кардиограммы удлиненный интервал QT В последнее время стало беспокоить сердце, периодически как-то странно дергается (как буд-то очень быстро бьется), часто учащенный пульс, сделал кардиограмму в поликлинике, терапевт сказал, что очень хорошая кардиограмма, из показателей посмотрел только пульс и общий вид кардиограммы. Я сама заинтересовалась показателями и что они значат, нашла таблицу с нормами, и увидела, что у меня удлинен интервал QT, но терапевт на это не обратила внимания, нашла информацию, что удлинение этого интервала увеличивает риск желудочковой тахикардии и тахикардии типа "Пируэт", а они могут привести к фибрилляции желудочков и остановке сердца, но при этом это все успешно лечится… И вот у меня возник вопрос, то ли я слишком много всего начиталась, то ли терапевт это не считает серьезной проблемой… Другой терапевт послушав меня и не видя кардиограммы назначил Метополол и Мельдоний… И сейчас не знаю что делать, пить или не пить, беспокоится по этому поводу или нет, может сделать дополнительные исследования… Подскажите пожалуйста…
Источник: health.mail.ru
