Все важные процессы в организме человека происходят на клеточном уровне. Ткани, как совокупность клеток, выполняют защитную, опорную, регулирующую и другие значимые функции. При нарушении клеточного обмена, вызванном разными причинами, происходят разрушительные реакции, которые могут привести к изменениям функционирования организма и даже отмиранию клеток. Некроз кожи является следствием патологических изменений и может стать причиной необратимых смертельно опасных явлений.
Что такое некроз тканей
В организме человека ткань, представленная совокупностью структурно-функциональных элементарных клеток и внеклеточных тканевых структур, участвует во многих жизненно важных процессах. Все виды (эпителиальная, соединительная, нервная и мышечная) взаимодействуют между собой, обеспечивая нормальную жизнедеятельность организма. Естественное отмирание клеток является неотъемлемой частью физиологического механизма регенерации, но патологические процессы, возникающие в клетках и межклеточном матриксе, влекут за собой опасные для жизни изменения.
Самыми тяжелыми последствиями для живых организмов характеризуется некроз тканей – отмирание клеток под влиянием экзогенных или эндогенных факторов. При этом патологическом процессе происходит набухание и изменение нативной конформации молекул цитоплазматических белков, что приводит к утрате их биологической функции. Результатом омертвения является слипание белковых частиц (флокуляция) и окончательное разрушение жизненно необходимых постоянных компонентов клетки.
Причины
Прекращение жизненной активности клеток происходит под воздействием изменившихся внешних условий существования организма или в результате патологических процессов, происходящих внутри него. Причинообразующие факторы возникновения некроза классифицируются в разрезе их экзогенного и эндогенного характера. К эндогенным причинам, по которым ткани могут омертветь, относятся:
- сосудистые – нарушения в работе сердечно-сосудистой системы, которые привели к нарушению кровоснабжения тканей, ухудшению кровообращения;
- трофические – изменение механизма клеточного питания, нарушение процесса обеспечения сохранности структуры и функциональности клеток (например, некроз кожи после операции, долго незаживающие язвы);
- метаболические – нарушение метаболических процессов вследствие отсутствия или недостаточной выработки определенных ферментов, изменение общего обмена веществ;
- аллергические – высокоинтенсивная реакция организма на условно безопасные вещества, результатом которой являются необратимые внутриклеточные процессы.

Экзогенные патогенные факторы обусловлены воздействием на организм внешних причин, таких как:
- механические – повреждение целостности тканей (ранение, травма);
- физические – нарушение функциональности, вследствие воздействия физических явлений (электрический ток, радиация, ионизирующее излучение, очень высокая или низкая температура – обморожение, ожог);
- химические – раздражение химическими соединениями;
- токсические – поражение кислотами, щелочами, солями тяжелых металлов, лекарственными средствами;
- биологические – разрушение клеток под воздействием патогенных микроорганизмов (бактерий, вирусов, грибков) и выделяемых ими токсинов.
Признаки
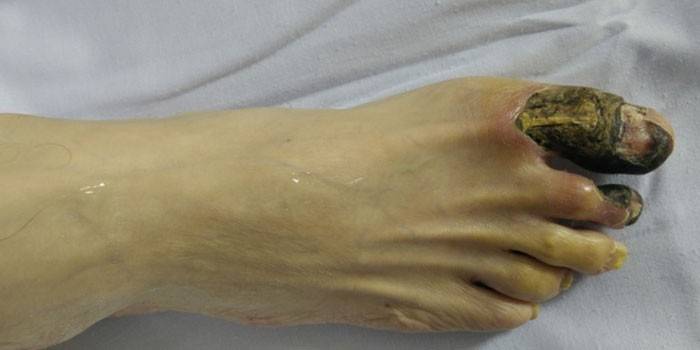
Начало некротических процессов характеризуется потерей чувствительности в пораженной области, онемением конечностей, чувством покалывания. Об ухудшении трофики крови свидетельствует бледность кожных покровов. Прекращение кровоснабжения поврежденного органа приводит к тому, что цвет кожи становится синюшный, а затем приобретает темно-зеленый или черный оттенок. Общая интоксикация организма проявляется в ухудшении самочувствия, быстрой утомляемости, истощении нервной системы. Основными симптомами некроза являются:
- утрата чувствительности;
- онемение;
- судороги;
- отечность;
- гиперемия кожных покровов;
- ощущение холода в конечностях;
- нарушение функционирования дыхательной системы (одышка, изменение ритмики дыхания);
- повышение частоты сердечных сокращений;
- перманентное повышение температуры тела.
Микроскопические признаки некроза
Раздел гистологии, посвященный микроскопическому изучению пораженных тканей, называется патогистология. Специалисты этой области исследуют срезы органов на предмет выявления признаков некротического повреждения. Омертвение характеризуется следующими изменениями, происходящими в клетках и межклеточной жидкости:
- утрата способности клеток к избирательному окрашиванию;
- преобразование ядра;
- дискомплексация клеток в результате изменения свойств цитоплазмы;
- растворение, распад межуточного вещества.
Потеря способности клеток избирательно красится, под микроскопом выглядит, как бледная бесструктурная масса, без четко выраженного ядра. Преобразование ядер клеток, подвергшейся некротическим изменениям, развивается в следующих направлениях:
- кариопикноз – сморщивание клеточного ядра, происходящее в результате активизирования кислых гидролаз и повышения концентрации хроматина (основного вещества клеточного ядра);
- гиперхроматоз – происходит перераспределение хроматиновых глыбок и их выстраивание по внутренней оболочке ядра;
- кариорексис – полный разрыв ядра, темно-синие глыбки хроматина расположены в произвольном порядке;
- кариолизис – нарушение хроматиновой структуры ядра, его растворение;
- вакуолизация – в клеточном ядре формируются пузырьки, содержащие прозрачную жидкость.

Высокое прогностическое значение при некрозе кожи инфекционного происхождения имеет морфология лейкоцитов, для изучения которой проводятся микроскопические исследования цитоплазмы пораженных клеток. Признаками, характеризующими некротические процессы, могут быть следующие изменения цитоплазмы:
- плазмолизис – расплавление цитоплазмы;
- плазморексис – распад содержимого клетки на белковые глыбки, при заливке ксантеновым, красителем изучаемый фрагмент окрашивается в розовый цвет;
- плазмопикноз – сморщивание внутренней клеточной среды;
- гиалинизация – уплотнение цитоплазмы, приобретение ею однородности, стекловидности;
- плазмокоагуляция – в результате денатурации и коагуляции, происходит распад жесткой структуры молекул белка и утрата их естественных свойств.
Соединительная ткань (межуточное вещество) в результате некротических процессов подвергается постепенному растворению, разжижению и распаду. Изменения, наблюдаемые при гистологических исследованиях, происходят в следующем порядке:
- мукоидное набухание коллагеновых волокон – стирается фибриллярная структура вследствие накопления кислых мукополисахаридов, что приводит к нарушению проницаемости сосудисто-тканевых структур;
- фибриноидное набухание – полная утрата фибриллярной исчерченности, атрофирование клеток межуточного вещества;
- фибриноидный некроз – расщепление ретикулярных и эластических волокон матрикса, развитие бесструктурности соединительной ткани.
Виды некроза
Для определения характера патологических изменений и назначения соответствующего лечения возникает необходимость классифицировать некроз по нескольким признакам. Основу классификации составляют клинические, морфологические и этиологические признаки. В гистологии выделяется несколько клинико-морфологических разновидностей некроза, принадлежность которых к той или иной группе определяется исходя из причин и условий развития патологии и структурных особенностей ткани, в которой она развивается:
- коагуляционный (сухой) – развивается в насыщенных белками структурах (печень, почки, селезенка), характеризуется процессами уплотнения, обезвоживания, к этому виду относится ценкеровский (восковидный), некроз жировой ткани, фибриноидный и казеозный (творогообразный);
- колликвационный (влажный) – развитие происходит в тканях, богатых влагой (мозг), которые подвергаются разжижению вследствие аутолитического распада;
- гангрена – развивается в тканях, которые соприкасаются с внешней средой, выделяют 3 подвида – сухой, влажный, газовый (зависит от места локализации);
- секвестр – представляет собой участок омертвевшей структуры (чаще костной), не подвергшейся саморастворению (автолизу);
- инфаркт – развивается вследствие непредвиденного полного или частичного нарушения кровоснабжения органа;
- пролежни – формируется при местном нарушении кровообращения вследствие постоянной компрессии.
В зависимости от происхождения некротических изменений ткани, причин и условий их развития, некроз классифицируют на:
- травматический (первичный и вторичный) – развивается под непосредственным воздействием патогенного агента, по механизму возникновения относится к прямым некрозам;
- токсигенный – возникает, как следствие влияния токсинов различного происхождения;
- трофоневротический – причиной развития служат нарушения работы центральной или периферической нервной системы, вызывающие нарушения иннервации кожных покровов или органов;
- ишемический – возникает при недостаточности периферического кровообращения, причиной может служить тромбоз, закупорка сосудов, низкое содержание кислорода;
- аллергический – появляется вследствие специфической реакции организма на внешние раздражители, по механизму возникновения относится к непрямым некрозам.
Исход
Значение последствий омертвения тканей для организма определяется исходя из функциональных особенностей отмирающих частей.
самым тяжелым осложнениям может привести некроз сердечной мышцы. Независимо от вида повреждения некротический очаг является источником интоксикации, на который органы реагируют развитием воспалительного процесса (секвестрация) для того, чтобы оградить здоровые участки от вредного воздействия токсинов. Отсутствие защитной реакции свидетельствует об угнетенной реактивности иммунитета или высокой вирулентности возбудителя некроза.
Неблагоприятный исход характеризуется гнойным расплавлением поврежденных клеток, осложнением которого является сепсис и кровотечения. Некротические изменения в жизненно важных органах (корковом слое почек, поджелудочной железе, селезенке, головном мозге) может привести к летальному исходу. При благоприятном исходе происходит расплавление отмерших клеток под воздействием ферментов и замещение омертвевших участков межуточным веществом, которое может происходить в следующих направлениях:
- организация – место некрозированной ткани замещается соединительной с образованием рубцов;
- оссификация – мертвый участок замещается костной тканью;
- инкапсуляция – вокруг некротического очага формируется соединительная капсула;
- мутиляция – наружные части тела отторгаются, происходит самоампутация омертвевших участков;
- петрификация – обызвествление подвергшихся некрозу участков (замещение солями кальция).
Диагностика
Выявить некротические изменения поверхностного характера не составляет труда для специалиста-гистолога. Для подтверждения диагноза, установленного на основании устного опроса пациента и визуального осмотра, понадобится тестирование крови и образца жидкости из поврежденной поверхности. При наличии подозрений на образование газов при диагностированной гангрене будет назначен рентген. Омертвение тканей внутренних органов требует более тщательной и обширной диагностики, которая включает такие методы, как:
- рентгенографическое исследование – применяется, как метод дифференцированной диагностики для исключения возможности других заболеваний со схожими признаками, способ эффективен на ранних стадиях болезни;
- радиоизотопное сканирование – показано при отсутствии убедительных результатов рентгена, суть процедуры заключается во введении специального раствора, содержащего радиоактивные вещества, которые во время сканирования отчетливо видны на снимке, при этом пораженные ткани, ввиду нарушенного кровообращения, будут явно выделяться;
- компьютерная томография – проводится при подозрении на отмирание костной ткани, во время диагностики выявляются кистозные полости, наличие жидкости в которых свидетельствует о патологии;
- магнитно-резонансная томография – высокоэффективный и безопасный метод диагностики всех стадий и форм некроза, с помощью которого обнаруживаются даже несущественные изменения клеток.
Лечение
При назначении терапевтических мер при диагностированном отмирании тканей учитывается ряд важных моментов, таких, как форма и вид заболевания, стадии некроза и наличие сопутствующих болезней. Общее лечение некроза кожи мягких тканей предполагает прием фармакологических препаратов для поддержания истощенного болезнью организма и укрепление иммунитета. С этой целью назначаются следующие виды препаратов:
- антибактериальные средства;
- сорбенты;
- ферментные препараты;
- диуретики;
- витаминные комплексы;
- сосудоукрепляющие средства.
Специфическое лечение поверхностных некротических повреждений зависит от формы патологии:
|
Цель терапии | Способы лечения | ||||
|
|
|
||||
| Мокрый |
|
|
При локализации некротических поражений во внутренних органах лечение заключается в применении широкого спектра мер по минимизации болевых симптомов и сохранению целостности жизненно важных органов. Комплекс лечебных мероприятий включает:
- медикаментозную терапию – прием нестероидных противовоспалительных средств, сосудорасширяющих препаратов, хондропротекторов, лекарств, способствующих восстановлению костной ткани (витамин Д, кальцитониты);
- гирудотерапию (лечение медицинскими пиявками);
- мануальную терапию (по показаниям);
- лечебные физические упражнения;
- физиотерапевтические процедуры (лазеротерапия, грязелечение, озокеритолечение);
- оперативные способы лечения.

Хирургическое вмешательство
Оперативное воздействие на пораженные поверхности применяется только при безрезультативности осуществляемого консервативного лечения. Решение о необходимости проведения операции должно быть принято незамедлительно при отсутствии на протяжении более 2 дней положительных результатов предпринятых мер. Промедление без веских причин может привести к опасным для жизни осложнениям. В зависимости от стадии и разновидности заболевания назначается проведение одной из следующих процедур:
|
Вид хирургического вмешательства |
Показания к проведению операции |
Суть процедуры |
Возможные осложнения |
|
Некротомия |
Ранние этапы развития заболевания, влажная гангрена с локализацией в области грудной клетки или конечностей |
Наносятся лампасные или клеточные разрезы омертвевших покровов и прилегающих тканей до начала кровоточивости. Целью манипуляций является снижение интоксикации организма путем выведения скопившейся жидкости |
Редко инфицирование в области разрезов |
|
Некрэтомия |
Влажный некроз, появление видимой разграничительной зоны, отделяющей жизнеспособную ткань от мертвой |
Удаление некрозированных участков в пределах пораженной зоны |
Инфицирование, расхождение наложенных швов |
|
Ампутация |
Прогрессирующий влажный некроз (гангрена), отсутствие положительных изменений после проведения консервативной терапии |
Усечение конечности, органа или мягких покровов путем резекции существенно выше визуально определяемой пораженной области |
Отмирание тканей на оставшейся после резекции части конечности, ангиотрофоневроз, фантомные боли |
|
Эндопротезирование |
Поражения костной ткани |
Комплекс сложных хирургических манипуляций по замещению пораженных суставов протезами, изготовленных из высокопрочных материалов |
Инфицирование, смещение установленного протеза |
|
Артродес |
Отмирание костных тканей |
Резекция костей с последующим их сочленением и сращиванием |
Снижение трудоспособности пациента, ограниченность подвижности |
Профилактические меры
Зная основополагающие факторы риска возникновения некротических процессов, следует предпринимать профилактические меры по предупреждению развития патологии. Наряду с рекомендуемыми мероприятиями необходимо регулярно диагностировать состояние органов и систем, и при обнаружении подозрительных признаков обратиться за консультацией к специалисту. Профилактикой патологических клеточных изменений является:
- снижение риска травматизма;
- укрепление сосудистой системы;
- повышение защитных сил организма;
- своевременное лечение инфекционных заболеваний, острой респираторной вирусной инфекции (ОРВИ), хронических болезней.
Источник: sovets.net
Что вы не знали об ишемическом инсульте
Статистика МОЗ доказывает, что с каждым годом увеличивается количество больных, у которых патологически изменены сосуды в организме. Одним из самых опасных последствий такого явления считается ишемический инсульт головного мозга. К сожалению, это заболевание в первые сутки может спровоцировать летальный исход, если вовремя не отреагировать на симптоматику, не обратиться за профессиональной медицинской помощью.
Что такое ишемический инсульт (ОНМК)? Какой разновидностью характеризуется данное заболевание? Причины и клиническая картина, первая помощь больному до приезда скорой помощи? Какой вариант лечения и восстановления предлагает современная медицина? Каждый из этих вопросов детально изучается многими специалистами, невропатологи постоянно исследуют причины ишемического инсульта, разрабатывают различные программы профилактического воздействия, ведь появление этого заболевания может быть в любом возрасте начиная с рождения.
Виды ишемического инсульта, их характеристики
 » alt=»Инсульт» width=»500″ height=»344″>
» alt=»Инсульт» width=»500″ height=»344″>
На сегодняшний день врачи выделяют такие виды ишемического инсульта:
По скорости нарастания:
- транзисторная ишемическая атака. При этом виде происходит острое нарушение мозгового кровообращения по ишемическому типу в продолжение суток, при этом клиническая картина будет зависеть от области, которая была поражена;
- «малая атака». Ишемические атаки проявляются у больного в течение 2-22 дней, но при правильном неврологическом лечении симптоматика смазывается и может вообще исчезать;
- прогрессирующий. При этом виде последствия инфаркта головного мозга всегда самые серьёзные, не каждый пациент полностью восстанавливается;
- тотальный. Ишемический инфаркт головного мозга в таком случае развивается обширно, клинические проявления яркие, прогноз для дальнейшей жизни при этом виде непредсказуемый.
По степени тяжести:
 » alt=»Степень» width=»200″ height=»131″>
» alt=»Степень» width=»200″ height=»131″>
- Лёгкий. Люди после такого типа восстанавливаются быстро и за короткий промежуток времени.
- Средний. Инфаркт мозга носит очаговый характер, при этом сознание не страдает, может быть только неврологическая симптоматика;
- Тяжёлый. Такой вид возникает внезапно, имеет сложную клиническую картину, поражается сознание. Ранний восстановительный период у таких больных сложный, требует правильного и длительного лечения, в дальнейшем понадобится реабилитация с восстановлением функций поражённых участков мозга.
Также существует классификация ишемического инсульта по причине, которая его вызвала:
- кардиэмболический. Ишемический инсульт тогда проявляется из-за суженного просвета в сосудах головного мозга (эмболии). Причины ишемического инсульта – хронические формы патологий сердечно-сосудистой системы (инфаркта и пороков сердца, аритмии). Возникает кардиэмболический тип внезапно, при этом клиническая картина неврологических проявлений очень яркая;
- атеротромботический. Причины возникновения – атеросклероз центральных сосудов головного мозга. Клинические проявления появляются постепенно, пиковое проявление отмечается во время сна. Мозговой процесс нарушается из-за оторвавшегося тромба, который перекрыл один из сосудов;
- гемодинамический. Инсульты подобного типа возникают из-за атеросклероза, стеноза либо патологических изменений сосудов головного мозга. Возникнуть проблема может в любой момент, независимо от физической активности или состояния покоя;
- реологический. Ишемию в таком случае провоцируют внешние факторы, не связанные с патологиями сосудистой системы;
- лакунарный. Признаки ишемического инсульта, его причины появления у больных связаны с сахарным диабетом или гипертонией.
Инсульт по ишемическому типу также разделяется в зависимости от места локализации:
 » alt=»Артерии» width=»200″ height=»125″>
» alt=»Артерии» width=»200″ height=»125″>
- В сонной артерии.
- В позвоночной артерии либо её ветви.
- В мозговой.
Прогноз для дальнейшей работы мозга после инсульта у каждого человека индивидуален, поскольку патология проявляется большим разнообразием типов, клинических проявлений и последствий.
Главное, что должен знать каждый пациент: только своевременная диагностика и правильное, систематическое лечение патологий сосудистой системы поможет избежать ишемического инсульта.
Клиническая картина ишемического инсульта
Если у больного развивается ишемический инсульт, симптомы появляются внезапно за пару минут, а то и секунд, лишь у 20 % может клиническая картина проявляться постепенно, от нескольких часов и до нескольких суток.
Симптомы ишемического инсульта тесно связаны с участком головного мозга, который был поражён. Практически во всех случаях наблюдается нарушение функций головного мозга, теряется двигательная активность большого участка тела. В тяжёлых случаях с ишемическим инсультом приходит полное угнетение сознания и кома.
Инфаркт мозга практически во всех случаях имеет следующие проявления:
 » alt=»Слабость» width=»200″ height=»141″>
» alt=»Слабость» width=»200″ height=»141″>
- полная потеря сознания, в редких случаях – сильное возбуждение;
- тошнота, может открыться рвота;
- жар, который будет сопровождаться обильным выделением пота;
- сильная головная боль. Она является сигналом того, что начинается инфаркт головного мозга. Симптомы и проявления боли будут зависеть от места локализации патологии сосуда;
- нарушение ориентации.
Все эти проявления носят общий характер, но существуют симптомы, которые дают возможность человеку и врачу конкретно указать на инфаркт мозга.
К ним относят:
- Двигательные нарушения. Из-за отёчности мозга может полностью исчезать чувствительность во всём теле или правой, левой его части.
- Речевая афазия. Больные могут перестать говорить или произносить фразы, которые непонятны окружающим.
- Нарушения зрения. Может полностью пропасть зрение в одном глазу или появиться двоение.
- Амнезия. Встречается нечасто, но человеку придётся долго лечиться, проходить реабилитацию, чтобы восстановиться. В единичных случаях больные живут без прошлых знаний и воспоминаний до конца своих дней.
Для этой болезни также характерны специфические симптомы, помогающие врачу на первых этапах определить область поражения.
Например:
- отёк мозга при инсульте в левой части – происходит парализация или снижение чувствительности в правой части;
- отёк головного мозга при инсульте в височной части – нарушение логического мышления, нежелание говорить, сильное депрессивное состояние.
Причины, приводящие к ишемическому инсульту
 » alt=»Врач» width=»200″ height=»133″>
» alt=»Врач» width=»200″ height=»133″>
Учитывая, что всё чаще ставится людям диагноз – «ишемический инсульт», причины детально изучаются врачами. Именно детальное знание всех факторов, приводящих к заболеванию, поможет не только выбирать правильные тактики лечения, но и помогать проводить профилактические мероприятия.
Среди самых распространённых причин врачи называют следующие:
- Гипертоническая болезнь. Хроническая форма этого заболевания вызывает набухание сосудов, их стенки ослабевают, теряют тонус.
- Атеросклеротические бляшки. Высокий уровень холестерина – это всегда сужение просвета в сосудах и риск образования тромба.
- Гипертоническая болезнь и атеросклероз – это максимальная угроза для развития ишемического инсульта. Лечение будет продолжительным и сложным.
- Сахарный диабет тяжёлой степени.
- Мигрень. При игнорировании частых и сильных головных болей развивается церебральный ангиоспазм.
- Перенесённый инфаркт миокарда.
- Воспалительные процессы в эндокарде.
- Аритмия.
- Пороки сердца.
Нужно всегда помнить, что не только заболевания, но и образ жизни может вызвать инфаркт головного мозга. Последствия тогда будут непредсказуемыми.
В основном причиной становится:
 » alt=»Алкоголь» width=»200″ height=»112″>
» alt=»Алкоголь» width=»200″ height=»112″>
- алкоголь с курением;
- систематическая интоксикация лекарственными препаратами;
- наследственный фактор;
- возрастные изменения;
- длительный приём гормональных препаратов;
- врождённые патологии кровеносных сосудов.
Последствия ишемического инсульта головного мозга напрямую связаны с причиной, которая его вызвала.
Диагностические мероприятия
Лечение ишемического инсульта любого вида проводится только в условиях стационара. При поступлении в стационар врач обязательно проводит ряд инструментальных исследований. Чем раньше больной будет обследован и назначено лечение, тем менее фатальными будут последствия.
При поступлении проводят следующую диагностику:
 » alt=»Диагностика» width=»200″ height=»89″>
» alt=»Диагностика» width=»200″ height=»89″>
- Изучение и сбор анамнеза. Врач уточняет, сколько длились симптомы, когда и как ухудшилось состояние, есть ли хронические недуги у больного.
- Исследование неврологических нарушений. Человек, перенёсший ишемический инсульт, последствия может иметь в нарушениях мочевой, дыхательной или сосудистой систем. Отёк после кровоизлияния может блокировать определённую часть мозга, вызывая отсутствие функционирования некоторых органов или частей тела.
- Обязательно проводится лабораторное исследование анализов крови и мочи.
- Человека, перенёсшего ишемический инсульт головного мозга, последствия которого не являются тяжёлыми, могут направить на МРТ или КТ. Эта аппаратура позволяет установить место разрыва сосуда, выявить тип заболевания. Также данная диагностика проводится при последующем лечении, чтобы видеть эффективность выбранной схемы терапии.
Варианты лечения
Диагностировав ишемический инсульт головного мозга, прогноз для жизни больного не даст ни один врач. Только после проведённой терапии можно будет сказать, какое восстановление потребуется и в какой мере вернутся двигательные, речевые функции.
Первым заданием медикаментозной терапии будет предупреждение осложнений, восстановление функций поражённого участка мозга.
Понимая, что такое инфаркт и инсульт, врач проводит все мероприятия по предупреждению:
 » alt=»Назначение» width=»200″ height=»150″>
» alt=»Назначение» width=»200″ height=»150″>
- отёков мозга;
- воспалительных процессов в мочеполовой системе;
- пролежней;
- застойных пневмоний;
- тромбоэмболии.
Первые шесть дней больные проводят в реанимационных палатах, где проводятся все мероприятия по ликвидации острых нарушений дыхательной и сердечно-сосудистой систем. В случае комы больным проводят интубирование и подсоединяют аппарат искусственной вентиляции лёгких.
В эти дни проводится круглосуточный мониторинг:
- артериального давления. Его показатели не должны опускаться ниже, чем на 10 % от нормы;
- работы сердечной мышцы;
- частоты пульса;
- частоты дыхания;
- уровня гемоглобина в крови;
- уровня сахара;
- температуры тела.
Обязательно вводятся такие группы препаратов:
- антикоагулянты;
- лекарства, которые разжижают кровь;
- антиагреганты;
- вазоактивные препараты;
- нейротрофики;
- ангиопротекторы;
- антиоксиданты.
Последствия ишемического инсульта
Лечение и реабилитация после ишемического инсульта займёт не менее 1-2 лет. Но, как показывает медицинская практика, у многих остаются последствия.
Среди самых распространённых выделяют следующие:
 » alt=»Последствия» width=»200″ height=»113″>
» alt=»Последствия» width=»200″ height=»113″>
- Постинсультная депрессия. У многих появляются ощущения разбитости, они боятся стать обузой для близких. Больные становятся агрессивными, пугливыми, у них может меняться настроение по несколько раз на день без видимых на то причин.
- Полная либо частичная потеря чувствительности в конечности или на лице. Восстановление после ишемического инсульта дома обязательно предполагает курсы массажей, ЛФК, которые помогут вернуть утраченную чувствительность.
- Утрата двигательной активности. Жизнь после ишемического инсульта для многих становится невозможна без инвалидного кресла, ходунков или палки. Многим становится трудно выполнять обычную бытовую работу.
- Когнитивные нарушения. Больные забывают своё имя, адрес, родных.
- Нарушений речевой функции. У человека, перенёсшего ишемический инсульт, реабилитация обязательно предполагает восстановление речевой функции. Больным приходится учить слова, связывать их в предложения.
- Нарушение координации. Некоторым, чтобы прожить самостоятельно, приходится ограничить двигательную активность. При резких движениях у них появляется головокружение, пошатывание, случаются падения.
- Эпилептические приступы. Такой вариант возможен, но проявляется только у 10 % всех больных.
Чем дольше будут сохраняться последствия перенесённого ишемического инсульта, тем тяжелее будет избавиться от них навсегда.
Прогноз для жизни
Для человека, перенёсшего ишемический инсульт, прогноз для жизни будет зависеть от степени поражения головного мозга и от терапевтических мероприятий, которые были проведены в первые 23 дня.
Дать точный прогноз в первые дни не сможет ни один врач. Тяжесть последствий перенесённого инсульта чаще всего оценивают по шкале инсульта Национального института Здоровья.
- В первые 30 дней умирает примерно 15-20 % больных. Такой высокий процент объясняется появлением осложнений в виде отёка головного мозга, пневмоний, эмболии лёгочной артерии, почечной недостаточности.
- Самая большая цифра летальных исходов фиксируется в первые 72 часа после инсульта. Это связано с большими объёмами поражения мозга или сочетания инсульта с инфарктом миокарда.
- Среди оставшихся в живых 60-70 % впоследствии получают инвалидность. Из них к концу первого года умирает ещё 40 % от повторного инсульта, к концу пятого года летальный исход фиксируется у 40 %, к десятому году – 25 %.
- Что касается восстановления двигательной активности, то максимальных успехов удаётся достичь в первые 3 месяца. Если за этот период восстановление не удалось, то в дальнейшем это маловероятно.
Какое давление при инсульте?
Инсульт – это опасная патология, которая характеризуется нарушением кровообращения в головном мозге и структурными изменениями, возникающими в результате этого патологического процесса. Артериальное давление при инсульте – важная составляющая диагноза, именно из-за этого показателя и нарушается обычный процесс функционирования мозга, что приводит к инвалидизации пациента.
Механизм появления и развития инсульта
Перед тем как ответить на вопрос, какое давление при инсульте, нужно отличить две формы болезни. Инсульт бывает двух видов:
- геморрагический (кровоизлияние в мозг);
- ишемический (инфаркт мозга).
В обоих случаях артериальное давление при инсульте сыграло не последнюю роль. Геморрагический вид развивается в том случае, когда артериальное давление у человека пониженное и резко повысилось по каким-то причинам до критических отметок. При этом необязательно иметь в анамнезе гипертоническую болезнь.
Геморрагический инсульт может возникнуть, если типичное давление человека находилось на отметках в 150/100 мм рт. ст., но резко поднялось до показателей 220/150 мм рт. ст. В таком случае мелкие кровеносные сосуды не выдерживают перенапряжения и лопаются с последующим кровоизлиянием и формированием гематомы.
Если инсульт ишемический, то вероятно, что у пациента есть в анамнезе гипертоническая болезнь, а также склонность к тромбозу или атеросклерозу. В случае резкого повышения показателей артериального давления, тромб отрывается от стенки крупного сосуда и поступает с током крови в мозг, где и закупоривает небольшой сосуд. Показатели давления при ишемическом инсульте — от 200/100 мм рт. ст. до 250/180 мм рт. ст. и выше.
В результате участок мозга недополучает кровь, что вызывает локальный отек, формирование некротического участка и повышение давления. Геморрагический инсульт развивается быстрее, чем ишемический и зона некроза в таком случае увеличивается. Тяжесть состояния человека зависит от количества умерших нервных клеток в процессе.
Первая реакция организма
Повышение показателей артериального давления после инсульта – это нормально. Нельзя сбивать повышенное давление самостоятельно. Артериальная гипертензия возникает как защитный механизм организма, она уменьшает и локализует патологический процесс в мозге, и продолжает кровоснабжать целостные участки.
Причины такого явления:
- Нарушение регуляции мозгового кровоснабжения.
- Повышение давления внутри черепа.
- Увеличение содержания норадреналина в крови.
Именно показатели повышенного артериального давления поддерживают мозговую перфузию. Нормальное значение систолического АД находится на уровне 180 мм рт. ст. Есть отдельные мозговые зоны, которые еще подлежат восстановлению, они называются полутенью или пенумброй. Если артериальное давление падает, то такие «пограничные» клетки также становятся нежизнеспособными. Низкие показатели АТ в первые дни после инсульта способствуют увеличению патологического процесса и большего количества отрицательных последствий.
Лечение инсульта разное в зависимости от формы. В любом случае пациента как можно скорее нужно доставить в стационар. Если патология имеет ишемический характер, то в терапевтическое окно, в течение трех часов, можно применить реперфузионную терапию. Тромб, который закупорил сосуд, рассосется, и давление можно будет постепенно снижать.
Инсульт важно вовремя выявить и облегчить последствия. Симптоматика микроинсульта такая:
- Увеличение показателей систолического/верхнего артериального давления на 10–15 единиц в сравнении с нормальными цифрами.
- Головокружение и шум в ушах с носовыми кровотечениями.
- Нарушение координации движений, шаткая или шаркающая походка.
- Слабость, ухудшение зрения и почерка.
Микроинсульт требует обращения к врачу, поскольку после такого состояния в десятки раз повышается риск возникновения обширного инсульта. Нельзя списывать симптоматику на стрессовую ситуацию, особенно если до этого возник гипертонический криз.
Симптомы обширного инсульта похожи на проявления микроинсульта, но они более длительные и глубокие. Возможно присоединение потери сознания, подключение судорог или перезов частей тела. Наблюдается слабость в конечностях, а артериальное давление повышается при этом на 40–50 единиц.
Как резко повышенное, так и резко пониженное давление после инсульта приводят к смертельным исходам с одинаковой частотой.
Период восстановления
Период восстановления после инсульта – это время, когда нужно быть максимально осторожным. Если возникновение патологического состояния было спровоцировано высоким давлением, и разновидность инсульта была геморрагической, то у 60% пациентов на пятый–шестой день возникает рецидив, то есть повторный прорыв сосудов головного мозга.
Как только были купированы первые признаки болезни и остановлено кровотечение, стоит назначить максимально мягкие гипотензивные препараты. Оптимальный показатель для периода восстановления – 150 мм рт. ст. Этот показатель должен поддерживаться специалистами, если пациент старше 60 лет или устанавливается самостоятельно у некоторых больных. В это время пониженное давление после инсульта – неопасно для здоровья.
В период восстановления еще нельзя применять диуретики, которые могут спровоцировать рецидив болезни. Контролируется профиль АД, показатель измеряется каждые три часа. В качестве корректоров высокого артериального давления применяются:
- «Каптоприл»;
- «Эналаприл»;
- «Клонидин» или «Клофелин»;
- «Бензогексоний»;
- «Пентамин».
При низком давлении в острый или восстановительный период важно исключить сердечную патологию и инфаркт миокарда.
Реабилитационный период
В реабилитационном периоде в зависимости от количества потерянных нейронов при инсульте наблюдаются такие состояния, как:
- параличи, парезы конечностей или частей тела;
- утрудненная речь;
- потеря памяти;
- тревожность;
- страх смерти.
Мониторинг артериального давления необходимо проводить пожизненно в профилактических целях. У молодых пациентов показатели на тонометре приходят в норму спустя два–три месяца после инсульта. Пациентам любого возраста нужно проходить профилактические осмотры у терапевта раз в два месяца после перенесенного инсульта и получать препараты для восстановления организма.
Инвалидность после инсульта
Инсульт – опасное заболевание c острым нарушением кровообращения в головном мозге, которое развивается в результате закупорки сосудов или их повреждения. Чаще всего ему подвержены люди старшего возраста.
Если случился инсульт, необходима экстренная медицинская помощь, которая должна быть оказана в течение первых 3-8 часов. Даже если помощь была своевременной и пациент остался жив, последствия могут быть тяжелыми. Не исключена частичная или полная потеря двигательной функции, приводящая к нетрудоспособности. По статистике, около 80% больных получают инвалидность после инсульта, и четвертой части из них требуется постоянных уход в течение всей жизни. Лишь пятая часть всех перенесших инсульт может вернуться к относительно нормальной трудовой деятельности после реабилитационных мероприятий. В зависимости от тяжести состояния пациенту может быть назначена 1, 2 или 3 группа инвалидности.
Виды инсульта
Он бывает двух типов: геморрагический инсульт и ишемический.
Ишемический
Этот вид заболевания наиболее распространен – около 80% всех случаев. Чаще всего случается у людей пожилого возраста. Его еще называют инфарктом мозга. Ишемический инсульт возникает из-за нарушения кровообращения в головном мозге по причине сужения просвета сосудов или закупорки тромбами. В результате часть мозга перестает снабжаться кровью и происходит отмирание тканей (некроз) этой области.
Геморрагический
Возникает от разрыва сосуда мозга. Существует две разновидности геморрагического инсульта: кровоизлияние в мозг и кровоизлияние субарахноидальное.
Первый наиболее распространен и обычно развивается у людей возраста около 50 лет. Основная причина – гипертоническая болезнь, реже – атеросклероз.
Второй тип представляет собой кровоизлияние в пространство между оболочками спинного и головного мозга, в котором находится ликвор (спинномозговая жидкость). Такой инсульт может случиться и в возрасте 30 лет. Основные его причины – артериальная гипертензия, курение, алкоголизм, прием большой дозы спиртного за один раз.
Кому дают инвалидность
Не все перенесшие инсульт могут оформить инвалидность. Группу можно получить строго по медицинским показаниям. Ее назначают согласно Федеральному закону и его изменений на основании результатов всех необходимых обследований. Обычно ее дают тем больным, у которых часть мозга полностью не восстановилась, нарушены движения, речь, другие функции.
- Первая группа показана больным, которые утратили способность себя обслуживать и нуждаются в постоянной помощи и уходе, а также тем, кто может частично себя обслуживать, при этом им нужно обеспечить необходимые социально-бытовые функции.
- Вторую группу получают пациенты, у которых нарушения функций стойкие и выраженные, но они не утратили способность себя обслуживать.
- Третья группа присваивается людям с умеренными нарушениями и умеренными ограничениями функций, которые в дальнейшем могут исчезнуть. В этом случае трудоспособность может быть сохранена, но запрещены некоторые виды работ.
Как получить
Право на получение инвалидности есть у каждого пациента, перенесшего инсульт и имеющего для этого медицинские показания. Занимается присвоением группы медицинская экспертная комиссия. Во время специальной экспертизы оценивается состояние больного, его трудоспособность и назначаются ограничения по физнагрузке.
Оформление займет достаточно много времени. В первую очередь пациенту нужно получить у лечащего врача направление на медико-социальную экспертизу (МСЭ), затем сдать анализы и пройти все необходимые обследования.
Таким образом, нужно подготовить следующие документы:
- заявление;
- направление от врача на экспертизу с подписью главного врача и печатью медучреждения;
- результаты обследований и анализов, которых нет в истории болезни;
- амбулаторную карту из поликлиники, где он проходит лечение;
- удостоверение личности (паспорт);
- если человек трудоустроен – копию трудовой книжки, справку о зарплате;
- больничный лист (если он есть) и справку о профессиональных заболеваниях и травмах.
Все обследования можно пройти в стационаре или в поликлинике (если человек ходячий). Направление на экспертизу дают в поликлинике после того, как будет рассмотрена история болезни и результаты анализов.
После подачи заявления пациенту будет назначена дата прохождения комиссии, в состав которой обычно входит три специалиста. На основании всех предоставленных документов и будет вынесено решение о присвоении инвалидности или отказе. Во время экспертизы анализируют все условия, в которых находится больной: трудовые, бытовые, социальные.
Группу определяют по следующим категориям:
- зависимости больного от окружающих;
- ограниченности способностей к самообслуживанию;
- способности передвигаться;
- способности ориентироваться в пространстве;
- способности контролировать свое поведение и общаться с окружающими.
Во время экспертизы обязательно ведется протокол. И случае присвоения инвалидности, и в случае отказа оформляется акт, который является официальным документом.
После получения группы человеку нужно обратиться в пенсионный фонд, для того чтобы ему назначили пенсию, и в социальный фонд для получения льгот.
Если пациенту отказали и он не согласен с решением комиссии, у него есть право в течение трех суток подать письменное заявление в бюро МСЭ, где он прошел освидетельствование, для проведения повторной экспертизы. Если ответ его снова не устроил, можно обжаловать его на другом уровне – в Федеральном бюро МСЭ.
Если инвалидность не пожизненная, то необходимо проходить ежегодное освидетельствование при 2 и 3 группах и один раз в два года при 1 группе. Оно назначается для отслеживания положительной динамики и возможного пересмотра группы. Ежегодное освидетельствование может быть отменено по достижении женщиной 50-летнего возраста и мужчиной 60-летнего.
Если инвалидность назначена пожизненно, но человек не согласен с группой, он может подать заявление на переосвидетельствование.
С большей долей вероятности получат группу инвалидности пациенты из следующих категорий:
- перенесшие инсульт ранее и не долечившиеся;
- гипертоники;
- больные с нарушениями в работе сердца и сосудов;
- люди с почечной недостаточностью;
- пациенты с сахарным диабетом;
- люди с хроническими заболеваниями, ограничивающими нормальную жизнедеятельность;
- пациенты с вредными привычками.
Виды труда, запрещенные после инсульта
В случае сохранения трудоспособности, например, при инвалидности 3 группы, все равно остаются виды деятельности, которые запрещены:
- в стрессовых ситуациях и с физическим напряжением;
- на улице (перепады температур могут вызвать гипертонический криз);
- с токсическими веществами;
- работа, при которой нужно держать в напряжении шею.
Заключение
Каждый случай инсульта требует индивидуального рассмотрения. Невозможно заранее сказать, положена человеку группа инвалидности или нет. Для этого необходимо пройти МСЭК, после чего и будет вынесено решение.
Источник: davlenie.giperton-med.ru
Коронарогенные (ишемические) некрозы миокарда
Некроз миокарда, возникающий вследствие ухудшения коронарного кровотока (ишемии), называется инфарктом миокарда.
Некроз инфаркт миокарда
представляет собой одну из острых форм ИБС, при которой доставка к сердцу кислорода и питательных веществ не удовлетворяет потребности сердца в этих веществах.
Этиология
В этиологии инфаркта миокарда играют важную роль атеросклероз коронарных артерий, их тромбоз, спазм и (достаточно редко) эмболия коронарных артерий. К факторам риска инфаркта миокарда можно отнести все те, которые указаны как факторы риска ИБС (см. начало данного раздела). Сочетание двух или трех факторов риска увеличивает вероятность возникновения инфаркта миокарда.
Патогенез
Выделяют следующие последовательно развивающиеся стадии в патогенезе инфаркта миокарда.
1. Выключение дыхательной цепи митохондрий и активация гликолиза как следствие начавшейся ишемии. Накопление недоокисленных продуктов метаболизма (прежде всего молочной кислоты) обусловливает появление боли.
2. Ингибирование основных метаболических путей, подавление гликолиза (из-за слишком большого снижения pH в ткани миокарда) и цикла Кребса, вследствие чего развивается дефицит аденозинтрифосфата. Наблюдается накопление жирных кислот вследствие угнетения их р. окисления, а также нарушение ионного равновесия в кардиомиоцитах
3. Разрушение мембран кардиомиоцитов в результате включения в патогенез инфаркта так называемой липидной триады. В нее входят активация липаз и фосфолипаз, активация свободнорадикального перекисного окисления липидов и детергентное действие на миокард избытка жирных кислот. Все указанные изменения происходят в мембранах сарколеммы, лизосом, саркоплазматического ретикулума и митохондрий и приводят к их повреждению и повышению проницаемости. Следствием этого является выход аутолитических ферментов лизосом в клетки миокарда, а также накопление в них избытка свободного Са++. Избыток Са++ вызывает контрактуру миофибрилл и приводит к дальнейшей активации липаз и фосфолипаз.
4. Заключительная стадия необратимых повреждений кардиомио-цитов и некроз ишемического участка миокарда.
Клинические проявления
Основными клиническими симптомами инфаркта миокарда являются:
1. Локализующаяся за грудиной сильнейшая боль, иррадиирующая в левое плечо, левую руку и межлопаточную область. Эта боль может возникать в покое днем или в ночное время.
В отличие от приступа стенокардии болевой синдром при инфаркте миокарда длится дольше и не купируется повторным приемом нитроглицерина. Следует отметить, что в тех случаях, когда болевой приступ длится более 15 мин, а принимаемые меры неэффективны, необходимо немедленно вызвать бригаду скорой медицинской помощи.
Встречаются и атипичные формы инфаркта миокарда, при которых характерные симптомы, в частности болевой синдром, могут отсутствовать (безболевая форма инфаркта миокарда).
2. Ослабление сократительной способности миокарда вследствие выпадения из акта сокращения поврежденного участка миокарда ведет к уменьшению сердечного выброса. При этом в зоне некроза с помощью эхокардиографии могут выявляться различные нарушения движения стенки поврежденного желудочка: акинезия, гипокинезия, дискинезия (выбухание участка инфаркта в момент систолы). Последнее может свидетельствовать о формировании острой аневризмы сердца-
3. Аритмии. В связи с изменением в зоне инфаркта биоэлектрических свойств кардиомиоцитов возникают нарушения сердечного ритма (вплоть до развития фибрилляции сердца), что приводит к значительным расстройствам системной гемодинамики и усугубляет нарушение контрактильной функции сердца. Источником эктопической активности на ранних стадиях развития инфаркта служит, как правило, окржающая зону некроза так называемая паранекротическая зона.
4. Появление типичных изменений ЭКГ. К ним относятся смещение сегмента ST выше или ниже относительно изоэлектрической линии, появление патологического комплекса QS (свидетельствует о наличии в миокарде очага глубокой ишемии или некроза), а также появление гигантского зубца Т. Он может быть положительным или отрицательным. Если подобный зубец Т появляется в раннем периоде инфаркта миокарда, его трактуют (как и смещение сегмента ST) как проявление острой ишемии миокарда. Если же он появляется на поздних стадиях, его связывают с формированием в миокарде рубцовых изменений.
В зависимости от особенностей изменений ЭКГ различают следующие формы инфаркта миокарда:
• Q-образующий инфаркт, или Q-инфаркт (с формированием патологического глубокого зубца Q, что может свидетельствовать о крупноочаговом трансмуральном инфаркте);
• Q-необразующий инфаркт, или He-Q-инфаркт (сопровождается не появлением зубца Q, а появлением отрицательного зубца Т, что свидетельствует о мелкоочаговом инфаркте миокарда).
5. В крови повышается содержание так называемых маркеров инфаркта миокарда: миокардиальной фракции креатинфосфокиназы, миоглобина, а также тропонина-Т, который имеет на сегодняшний день наиболее важное значение в диагностике инфаркта миокарда.
6. Одно из важных проявлений инфаркта миокарда – ухудшение реологических свойств крови, что способствует тромбообразованию. При инфаркте миокарда венозный тромбоз диагностируется у 10-15 % больных.
7. Кроме описанных выше изменений могут наблюдаться расстройства мозгового кровообращения, нарушения функции желудочно-кишечного тракта. Через несколько часов от начала инфаркта миокарда развивается лейкоцитоз. Весьма характерно для инфаркта появление так называемого симптома перекреста между числом лейкоцитов в крови и СОЭ, когда в конце 1-й недели выраженность лейкоцитоза снижается, а СОЭ увеличивается.
Осложнения
К ранним осложнениям относят острую сердечную недостаточность, кардиогенный шок, отек легких, механические осложнения (разрыв папиллярных мышц, перегородки и стенок миокарда), тампонаду сердца, перикардит, тромбоэмболию легочной артерии, являющуюся одной из наиболее частых причин внезапной смерти.
К поздним осложнениям (возникают через 2-3 нед. и более от начала инфаркта) относят постинфарктный синдром Дресслера, хроническую недостаточность кровообращения, развитие аневризм сердца, тромбоэмболию легочной артерии и повторные инфаркты миокарда. Что касается синдрома Дресслера, то он возникает через 2-6 нед. от начала инфаркта и проявляется перикардитом, плевритом и пневмонией. В его патогенезе играет роль образование аутоантител к деструктивно измененным при инфаркте белкам миокарда — миокардиальным аутоантигенам.
Принципы патогенетической терапии
1. Ликвидация болевого приступа с помощью сильнодействующих анальгетиков и наркотических средств.
2. Использование антиагрегантов и тромболитических препаратов. В качестве доврачебной помощи рекомендуется использовать аспирин.
3. Уменьшение потребности сердца в кислороде, улучшение его доставки и снижение риска возникновения аритмий ф-адреноблокаторы).
Рекомендуется также использовать:
• ингибиторы ангиотензинпревращающего фермента;
• седативные и снотворные препараты;
• противоаритмические средства.
4. Важное значение имеют и хирургические методы лечения, в частности аортокоронарное шунтирование и баллонная ангиопластика со стентированием коронарных артерий.
Некоронарогенные (неишемические) некрозы миокарда
Поражения сердца этого типа возникают как результат нарушения метаболизма в сердечной мышце в связи с действием на сердце избытка электролитов, гормонов, токсических продуктов обмена, кардиальных аутоантител. Различают следующие виды некоронарогенных некрозов миокарда.
Электролитно-стероидные некрозы
Образование данного вида некрозов связано с патогенным действием на миокард избытка вводимых в организм гормонов коры надпочечников (прежде всего минералокортикоидов) в сочетании с солями натрия. Такое воздействие приводит к увеличению проницаемости мембран кардиомиоцитов для натрия и накоплению его в сердце. Развивающийся впоследствии отек и «осмотический взрыв» клеток миокарда сопровождается возникновением очагов некроза.
Катехоламиновые некрозы миокарда
Повреждающее действие избыточных концентраций катехоламинов на сердце объясняется следующими механизмами.
Во-первых, сами катехоламины, и прежде всего адреналин, обладают прямым повреждающим действием на миокард.
Во-вторых, несмотря на то что катехоламины расширяют коронарные сосуды, они в значительно большей степени увеличивают потребность сердца в кислороде, т. к. повышают частоту сердечных сокращений и артериальное давление. Поэтому при прохождении крови по венечным сосудам кислород утилизируется раньше, чем кровь достигнет прекапиллярного отдела микрососудистого русла. Это приводит к тому, что в миокарде появляются участки, получающие кровь, обедненную кислородом.
В-третьих, под влиянием избытка катехоламинов в миокарде происходит активация перекисного окисления липидов, продукты которого повреждают мембраны кардиомиоцитов.
Токсические и воспалительные некрозы миокарда
Данные виды некрозов возникают при интоксикации или поражении миокарда воспалительным процессом. Токсический миокардит может возникать вследствие воздействия некоторых химических соединений и фармакологических препаратов, например кокаина, лекарственных средств, применяемых при лечении злокачественных опухолей. Эти токсические вещества оказывают прямое повреждающее действие на миокард, приводя к развитию необратимой дистрофии и появлению мелкоочаговых некрозов.
Примером воспалительных некрозов миокарда служат различные миокардиты: ревматические и дифтерийные. При любом воспалительном процессе, как и в данном случае, наблюдается альтерация (повреждение) миофибрилл. Развивающийся воспалительный отек также способствует альтерации. Все это ведет к развитию микронекрозов миокарда.
Аутоиммунные некрозы
Одним из примеров аутоиммунных некрозов миокарда служит синдром Дресслера, о котором было сказано выше.
Поврежденные белки при инфаркте миокарда могут стать аутоантигенами, к которым в организме вырабатываются антитела. Повторное развитие некротического процесса обусловливает запуск реакции «антиген-антитело» во многих участках сердечной мышцы, что вызывает множественные микронекрозы.
Источник: cardio-bolezni.ru
