В Европейской клинике регулярно проводится постановка кава-фильтров пациентам с онкологическими заболеваниями для профилактики развития тромбоэмболии легочной артерии (ТЭЛА). Также мы устанавливаем кава-фильтры больным с высокими риском развития ТЭЛА, не страдающим раком, например, при тромбозе глубоких вен голени, при различных видах нарушения свертывания крови и ряде других заболеваний. Нижеприведенная информация будет полезной для всех пациентов, нуждающихся в постановке кава-фильтров.
Единой общепринятой концепции по поводу хирургической профилактики ТЭЛА в международной практике нет. В США принят радикальный подход с установкой кава-фильтров с учетом эмбологенности тромба. В странах Западной Европы рекомендуют имплантацию только при невозможности проведения антикоагулянтной терапии при ТЭЛА.

Своевременная постановка кава-фильтров у больных с онкологическими заболеваниями является частью комплексной терапии при поздних стадиях рака, и довольно широко используется в рутинной клинической практике в странах Западной Европы. В зависимости от формы рака и стадии онкозаболевания кава-фильтры устанавливаются примерно 1,5–6,5% всех больных.
К сожалению, в отечественной клинической практике из-за низкой материальной обеспеченности системы здравоохранения показания к постановке кава-фильтров существенно сужены, что вносит свой вклад в высокий уровень смертности и более высокую частоту внезапной смерти по сравнению с данными онкологического реестра США и национальных раковых реестров ведущих стран Западной Европы.
Установка кава-фильтра позволяет не только избежать ТЭЛА на фоне терапии рядом химиопрепаратов, но и провести тромболизис ранее возникших тромбов.
Врачами отделения интервенционной хирургии Европейской клиники накоплен большой опыт профилактики и лечения тромбозов вен, тромбоэмболии легочной артерии, тромбофлебита на фоне варикозной болезни вен при онкологических заболеваниях. В отделении интервенционной хирургии используются как временные, так и постоянные венозные фильтры.
Что такое кава-фильтр?
Кава-фильтр представляет собой высокотехнологичную сетку на сложно моделированном каркасе или иную сложную конструкцию. С помощью рентгеноваскулярного вмешательства кава-фильтр устанавливается в просвет нижней полой вены, чуть ниже впадения в нее почечных артерий (инфренеальная позиция).
Кава-фильтр, установленный в нижней половой вене, задерживает все частицы размером более 2–4 мм (в зависимости от конструкции). Это позволяет току венозной крови от нижних конечностей и всех внутренних органов свободно проходить сквозь фильтр, задерживая при этом крупные тромбы, которые потенциально могут привести к значимому тромбозу или ТЭЛА.
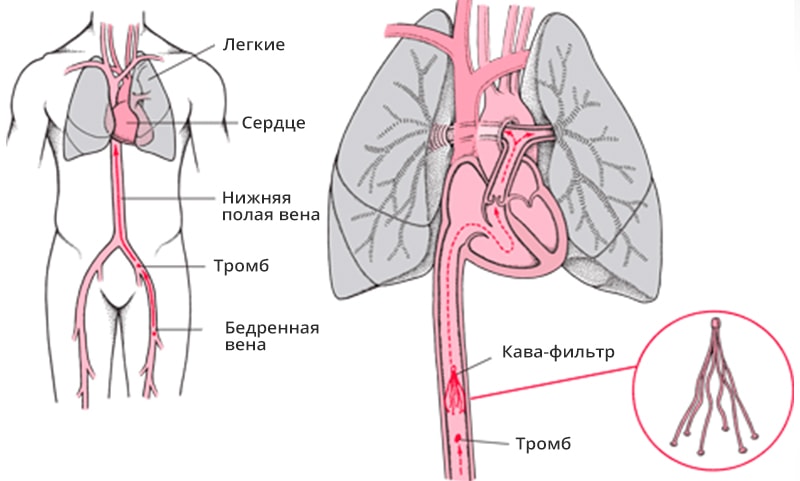
Под действием противосвертывающей системы крови и принимаемых противосвертывающих препаратов, например, варфарина, застрявшие тромбы растворяются прямо на кава-фильтре. При правильно установленном фильтре повторного вмешательства проводить не приходится. Современные конструкции кава-фильтров тромбируются крайне редко.
Какие кава-фильтры устанавливаются в Европейской клинике?
Мы используем самые современные модели фильтров, такие как:
- постоянный фильтр TrapEase (Cordis, США),
- съемные фильтры OptEase (Cordis, США),
- Guenther Tulip (Cook, США).
Одна из последних новинок в области профилактики ТЭЛА — кава-фильтр ALN (ALN, Франция). Это первый в мире кава-фильтр, который можно как оставить в вене пожизненно, так и удалить в сроки до 500 дней. Это самый большой период возможного удаления для съёмных кава-фильтров.
Кава-фильтр надежно фиксируется в стенке сосуда под воздействием температуры тела. Фильтр имеет рентгеноконтрастные метки из золотых колец, встроенных в интродьюсер катетера, которые позволяют с легкостью отслеживать движение кава-фильтра по извитым сосудам. Двухуровневая структура фильтра позволяет эффективно улавливать различные по размеру эмболы, не нарушая кровотока.
Наличие кава-фильтра в полой вене не влияет на работу магнитного резонансного томографа, поэтому пациент с фильтром может при необходимости проходить МРТ-исследование.
Как проводится установка кава-фильтра?
Процедура имплантации кава-фильтра в настоящее время является обычным эндоваскулярным вмешательством. Проводник, с помощью которого имплантируется кава-фильтр, вводится через бедренный доступ и большую подкожную вену, либо в яремную и подключичную вены под контролем рентгенотелевидения. Выбор доступа определяется предполагаемой локализацией тромба, поскольку проведение катетера через тромбированные вены чревато фрагментацией тромба с развитием ТЭЛА. Как правило, кава-фильтр устанавливается на уровне ниже устьев почечных вен.

Обычно операция выполняется в условиях рентген-операционной под кратковременным наркозом (поверхностной анестезией пропофолом). Во время выполнения процедуры имплантации пациент не чувствует никаких болезненных ощущений и дискомфорта.
После достижения катетером нужного уровня, кава-фильтр раскрывается, и проводник удаляется. Никаких швов на кожу не накладывается. Продолжительность процедуры постановки обычно составляет около 1 часа. После имплантации кава-фильтра проводится контрольная рентгенография для подтверждения правильности установки и контроля его месторасположения.
Мы рекомендуем ограничение физических нагрузок, желательно постельный режим в течение 1–2 дней после имплантации кава-фильтра. На 5–6 дней пациенту назначают антибиотики и антикоагулянты.
Какие существуют показания для установки кава-фильтров?
Общепринятыми показаниями к установке кава-фильтров являются:
- Тромбоз глубоких вен нижних конечностей с наличием неокклюзивных (флотирующих) тромбов — устанавливается постоянный кава-фильтр.
- Тромбоз глубоких вен ног при сопутствующей мерцательной аритмии, ишемической болезни сердца, сердечной недостаточности, а также у больных онкологическими заболеваниями, особенно на поздних стадиях.
- Эпизоды тромбоэмболии легочной артерии (ТЭЛА) в прошлом при наличии венозного тромбоза нижних конечностей в настоящее время — устанавливается постоянный кава-фильтр.
- Проведение операций на венах, лапароскопических вмешательств при тромбозе вен таза. На момент операции и ближайший послеоперационный период устанавливается временный кава-фильтр.

В Европейской клинике мы устанавливаем пациентам более 20-ти различных видов кава-фильтров как временных, так и постоянных от ведущих мировых производителей.
На какой срок устанавливается кава-фильтр?
Ряд кава-фильтров устанавливается пожизненно. Временные кава-фильтры обычно имплантируются на срок до 6 месяцев и удаляются после ликвидации проблем, ведущих к увеличению риска ТЭЛА.
Какие ограничения возникают у пациентов после установки кава-фильтра?
При установке универсальных съёмных кава-фильтров пациент находится под динамическим наблюдением врача-ангиохирурга или флеболога в течение 6 месяцев. При установленном кава-фильтре прием варфарина обязателен.
После снижения риска тромбоэмболии временный кава-фильтр удаляется, путём вмешательства, аналогичного постановке фильтра. Эта операция также проводится в условиях рентген-операционной врачом-ангиохирургом под рентгеновским контролем.
Принципиальное решение вопроса об удалении кава-фильтра принимается после выполнения повторного исследования гемодинамики в системе нижней полой вены (в т.ч. обеих конечностей), когда оценивается динамика разрешения тромбоза.
Установка несъёмных постоянных кава-фильтров, даже у пациентов с поздними стадиями рака, практикуется в настоящее время сравнительно мало, поскольку постоянный кава-фильтр наряду с положительной ролью — предотвращением тромбоэмболии — вызывает затруднение кровотока в бассейне нижней полой вены и формирование вторичной венозной недостаточности.

После установки кава-фильтра пациент живет обычной жизнью. Мы рекомендуем прием непрямых антикоагулянтов в поддерживающих дозировках. При наличии сопутствующей хронической венозной недостаточности желательно диспансерное наблюдение с посещением врача не реже 1 раза в месяц, употребление флеботоников и ношение компрессионного трикотажа. Кроме того, желательно прохождение контрольного дуплексного сканирования вен ног и нижней полой вены.
Есть ли у кава-фильтров какие-либо недостатки? Встречаются ли осложнения?
Учитывая большой практический опыт наших специалистов, являющихся корифеями эндоваскулярной хирургии в нашей стране, процент осложнений крайне низок и не превышает 1–3%. Среди них не представляющие угрозы жизни гематомы в точке доступа, незначительная миграция кава-фильтра и ряд других. Однако, польза от фильтра несоизмеримо больше, поскольку это снижает риск внезапной смерти от ТЭЛА в десятки раз.
Какова цена установки кава-фильтра в Москве?
Предлагаем вашему вниманию прайс, из которого вы можете узнать стоимость установки кава-фильтров в Европейской клинике:
- Имплантация постоянного кава-фильтра производства США — 108 000 р.
- Имплантация стент-фильтра в общую подвздошную вену — 108 000 р.
- Имплантация съемного кава-фильтра производства США или Франции — 137 000 р.
Источник: www.euroonco.ru
Актуальность проблемы
Тромбоэмболия легочной артерии (ТЭЛА) является грозным осложнением и третьей по частоте причиной внезапной смерти после инсультов и инфарктов. Это то, о чем в просторечье говорят: «оторвался тромб».
В основном тромбы возникают в глубоких венах ног на фоне длительной гиподинамии, заболеваний вен, нарушений свертывающей системы крови.
Оторвавшийся из периферической вены тромб перемещается по нижней полой вене вверх в правый желудочек сердца, откуда попадает в легочную артерию и может вызвать закупорку ее ветвей. При этом возникают грозные осложнения, часто приводящие к смерти в первые часы возникновения.
Лечение тромбоза вен нижних конечностей патогенетически довольно ясно: тромб надо убрать хирургическими методами или попробовать растворить медикаментами. Существует множество современных антитромботических препаратов, которые назначаются как для лечения, так и для профилактики тромбоза. Однако количество тромбозов глубоких вен нижних конечностей и связанных с ними осложнений с каждым годом не уменьшается, а только растет.

Если есть предрасположенность к тромбообразованию, сохраняются факторы риска, то патология эта будет возникать снова и снова, несмотря на лечение. Если уже произошла тромбоэмболия легочной артерии, и пациент остался жив, существует большая вероятность повторной ТЭЛА, так как заболевание это рецидивирующее.
Тогда встает вопрос не только лечения тромбоза, но и профилактики тромбоэмболии.
Задержать эмболы на пути к сердцу можно, создав для них механическое препятствие. Около 40 лет назад был предложен метод имплантации фильтра в просвет нижней полой вены. Первые фильтры имели много недостатков конструкции и часто сопровождались осложнениями.
Однако метод с годами получил широкое распространение. Из сложной сосудистой операции методика перешла в разряд малотравматичной чрезкожной манипуляции.
Что представляет собой кава-фильтр?
Современный кава-фильтр – это миниатюрная проволочная конструкция в виде зонтика, песочных часов, или гнезда. Основные требования к имплантам, внедряемым в полость сосуда:
- Устойчивость к коррозии.
- Надежная эффективность в улавливании тромбов.
- Обеспечение стабильной гемодинамики.
- Надежная фиксация.
- Простота установки.
- Желательно отсутствие ферромагнитных свойств.
- Простота извлечения в случаях временной установки.
Современные фильтры изготавливаются из:
- Высококачественной стали, покрытой специальной гепариннасыщенной мембраной.
- Титана.
- Нитинола (никелево-титановый сплав).
Кава-фильтры имеют различные размеры и подбираются индивидуально с учетом диаметра нижней полой вены у конкретного больного. Современные фильтры упакованы в специальные носители, которые с помощью проводника доставляются в нужное место установки. Там носитель снимается, фильтр расправляется и фиксируется на месте (или за счет специальных фиксирующих усиков, или за счет упругости конструкции).
Кава-фильтры могут быть:
- Постоянные – устанавливаются навсегда, удаление их невозможно. Такие фильтры плотно фиксируются к стенкам вены, так как имеют на своих опорах микроскопические шипы или усики.
- Съемные – устанавливаются на короткий период, в дальнейшем удаляются. Эти устройства не фиксируются специальными приспособлениями, эти фильтры связаны с проводником, конец которого фиксируется под кожей. С помощью этого проводника фильтр извлекается.
Показания для установки кава-фильтра
На настоящий момент антикоагулянтная терапия (лечение лекарствами, понижающими свертываемость крови) остается главным методом профилактики ТЭЛА при наличии рецидивирующего тромбоза. Имплантация кава-фильтра является несложной операцией, однако проводится только по очень строгим показаниям, и по большей части это связано с невозможностью применения антикоагулянтов.
Абсолютные показания для установки кава-фильтра:
- Противопоказания к терапии антикоагулянтами.
- Неэффективность лечения антикоагулянтами.
- Осложнения, возникшие в процессе лечения.
- Рецидивы тромбоэмболии, несмотря на терапию.
Относительные показания:
- Тромботическая болезнь в комбинации с сердечной недостаточностью.
- Тромболизис при тромбозе глубоких вен.
- Плохая переносимость антикоагулянтов.
- Тромбоз глубоких вен в комбинации с обширными травмами.
- Большие хирургические вмешательства у пациентов с высоким риском тромбоза.
- Протяженные флотирующие тромбы в глубоких венах.
Примечание: Флотирующий тромб – это тромб с небольшой площадью прикрепления к стенке сосуда, омываемый со всех сторон кровью и не перекрывающий полностью просвет вены. Такие тромбы наиболее опасны в плане отрыва и превращения в эмбол.
Противопоказания для установки кава-фильтров
Абсолютные:
- Критическое сужение просвета нижней полой вены.
- Невозможность доступа к нижней полой вене.
Относительные:
- Детский и подростковый возраст.
- Распространение тромбоза на надпочечный отдел нижней полой вены (выше отхождения от нее почечных вен).
- Септическое состояние пациента.
Как устанавливают кава-фильтр?
Перед операцией проводится стандартное обследование, а также ангиографическое исследование – проверяется проходимость и диаметр нижней полой вены, состояние почечных сосудов, выбирается идеальное место доступа.

Операция по установке кава-фильтра относится к высокотехнологичным эндоваскулярным операциям и проводится только в специализированных сосудистых центрах. Операционная должна быть оборудована рентгеноангиографической установкой.
Вмешательство проводится под местной анестезией. Присутствие анестезиолога обязательно. Производится катетеризация бедренной (в паховой области), подключичной, яремной (на шее), реже – локтевой вены. Затем через катетер с помощью гибкого проводника вводится сам фильтр, который упакован в специальный интродьюсер в сложенном состоянии. Под контролем высокочувствительного УЗ-датчика или рентгеновского аппарата проводник продвигается к месту прикрепления в нижней полой вене (обычно это чуть ниже места отхождения почечных вен). Здесь фильтр освобождают от носителя, он расправляется и устанавливается в правильное положение.
Очень важно, чтобы диаметр кава-фильтра соответствовал диаметру нижней полой вены. Так как при слишком маленьких размерах он может переместиться, а при больших – может произойти перфорация стенки вены.
Сама операция длится около 30 мин. Во время неё пациент не ощущает никакой боли.
После операции в течение нескольких дней рекомендуется постельный режим, назначаются антибиотики и гепарин.
Установка кава-фильтра никак не воздействует на причину заболевания. Поэтому пациентам, у которых отсутствуют противопоказания к терапии антикоагулянтами, она проводится и после операции по стандартным схемам.
Осложнения после установки кава-фильтра
Осложнения могут возникнуть уже во время самой операции. Крайне редко, но могут встречаться:
- Кровотечение.
- Пневмоторакс.
- Перфорация вены или артерии.
- Инфицирование.
- Неправильное положение во время установки.
Чем более продолжительное время фильтр находится в организме, тем большее количество осложнений может возникнуть:
- Тромбоэмболия фильтра с развитием окклюзии нижней полой вены.
- ТЭЛА при наличии фильтра.
- Тромбоз почечных вен.
- Тромбоз периферических вен.
- Перфорация стенок вены.
- Перемещение фильтра в правый желудочек сердца.
- Фрагментация фильтра.
- Образование гематомы в забрюшинном пространстве.
- Перфорация аорты, стенки кишки или почечной лоханки.
- Фильтр может быть причиной постоянных болей в поясничной области.
- Временные кава-фильтры с наличием якоря для извлечения, выведенного наружу, могут стать причиной инфицирования и сепсиса.
В некоторых случаях вероятность развития осложнений превышает пользу от установки кава-фильтра. В настоящее время все реже устанавливаются постоянные фильтры и все более внедряются в практику съемные кава-фильтры.
Съемный фильтр устанавливают на срок до нескольких недель на время интенсивного лечения тромбоза или обширных оперативных вмешательств. При возникновении риска осложнений съемные фильтры могут извлекаться из вены. Извлечение кава-фильтра аналогично операции его установки.
Если же осложнений от установленного фильтра нет, а риск тромбоэмболии сохраняется, он может оставаться в организме постоянно.
Снижение смертности и осложнений у пациентов с установленным кава-фильтром – доказанный факт, на этот счет проводились соответствующие исследования.
Стоимость различных моделей кава-фильтров вместе с установкой колеблется от 25 до 70 тыс. рублей.
Видео: имплантация временного кава-фильтра
Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
Источник: sosudinfo.ru
Введение
Тромбоз в системе нижней полой вены (НПВ) осложняет течение различных патологических процессов и входит в число наиболее распространенных сосудистых заболеваний. Наибольшую опасность представляет осложнение венозного тромбоза — тромбоэмболия легочных артерий (ТЭЛА). Только в США от данного осложнения ежегодно умирает не менее 240 тыс. человек [1].
Остановить процесс тромбообразования при венозном тромбозе может антикоагулянтная терапия. Однако у значительной доли больных она не способна обеспечить надежную защиту от эмболизации легочного артериального русла. Данная группа включает пациентов с флотирующими тромбами илеокавального сегмента, абсолютными либо относительными противопоказаниями к использованию антикоагулянтов, осложнениями антикоагулянтной терапии либо ее неэффективностью, с массивной ТЭЛА при наличии резидуального венозного тромба, больных с легочной гипертензией и низким кардиопульмональным резервом [2–5].
В таких случаях для предотвращения массивной ТЭЛА больным выполняют имплантацию противоэмболического кава-фильтра (КФ), впервые предложенного в 1967 г. американским кардиохирургом Kazi Mobin-Uddin [6]. Наряду с лечебной имплантацией КФ зарубежные клиницисты широко применяют профилактическую имплантацию КФ больным с предполагаемым длительным периодом иммобилизации и высоким риском венозных тромбоэмболических осложнений (ВТЭО), например, пациентам с черепно-мозговой травмой, повреждением позвоночника, множественными переломами конечностей и костей таза [4, 7, 8].
В зависимости от решаемой клинической задачи и конструктивных особенностей модели КФ подразделяют на 3 группы [9]:
постоянные;
съемные;
временные.
Постоянные КФ имплантируют на срок, соответствующий продолжительности жизни больного. Эндоваскулярное удаление такого КФ не предполагается. Конструкция съемных КФ позволяет выполнить эндоваскулярное удаление устройства. Оно технически возможно, но не обязательно. Временные КФ имеют в своей конструкции «якорное» устройство, конец которого выводится наружу или фиксируется под кожей. Удаление такого КФ обязательно. Данные модели не получили распространения, поскольку подобная конструкция способствовала миграции КФ и инфицированию устройства.
На основании поиска в базах данных (FDA Premarket Notification, MEDLINE, FDA MAUDE) c 1980 по 2014 г. идентифицированы 23 модели КФ — 14 съемных и 9 постоянных [10]. С учетом модификаций и КФ регионарных производителей, не включенных в обзор, общее количество моделей фильтрующих устройств составляет более сотни [11].
Несмотря на предпринимаемые в последнее десятилетие попытки ограничить рутинное использование КФ [2, 3], количество ежегодно имплантируемых в экономически развитых странах противоэмболических устройств исчисляется сотнями тысяч. За период с 1979 по 2007 г. в США ежегодное количество вмешательств увеличилось с 2 тыс. до 167 тыс. Согласно оценочным данным, в 2012 г. количество имплантированных КФ достигло 259 тыс. [12, 13]. В России в 2015 г. имплантировано 3111 КФ [14].
КФ эффективно решают первоочередную задачу по предотвращению легочной эмболии [8, 15]. Однако с накоплением опыта их применения стало очевидно, что длительное нахождение инородного тела в НПВ способно стать причиной различных, в т. ч. жизнеугрожающих, осложнений [16–19].
Создание съемных моделей КФ, которые предполагается удалять после устранения угрозы ТЭЛА, расширило возможности клиницистов. Однако в результате влияния целого комплекса медицинских, организационных и социальных проблем удаление таких КФ выполняют лишь в 9–49,1% наблюдений, а остальные имплантированные устройства переходят в категорию постоянных [15, 20–22]. С учетом того, что общее количество людей, живущих с КФ, исчисляется сотнями тысяч, их дальнейшая судьба представляет собой не только медицинскую, но и социальную проблему.
Осложнения имплантации кава-фильтров
Ранние осложнения
Все осложнения, связанные с применением как постоянных, так и съемных моделей КФ, принято подразделять на ранние (развившиеся в процессе установки или в течение суток после нее) и поздние.
Осложнения в процессе установки КФ связаны с техническими ошибками выполнения манипуляции либо с неправильным подбором диаметра фильтра. Пункцию сопутствующей артерии, кровотечение, гематому в зоне доступа, пневмоторакс, воздушную эмболию, некорректный уровень имплантации (супраренальный отдел НПВ, почечные, печеночные, подвздошные вены), наклон КФ, неполное его раскрытие, инфицирование, тромбоз вены доступа регистрируют в 3,5–15% случаев [8, 23–28].
Некоторые из осложнений носят казуистический характер. Так, описана имплантация КФ в позвоночный канал, к счастью, не вызвавшая неврологических расстройств у пациента [29]. Вероятно, это было обусловлено перфорацией проводником стенки НПВ и попаданием его и КФ в межпозвоночное отверстие. В литературе представлены 4 наблюдения ошибочной имплантации КФ в аорту [30–33], причем у 1 больного КФ обнаружили в аорте при компьютерной томографии случайно, через 16 лет после вмешательства. Травме НПВ в процессе установки КФ может сопутствовать повреждение ножками КФ поясничной артерии. Остановка продолжающегося кровотечения требует выполнения открытого хирургического вмешательства [34].
Выбор КФ неадекватного диаметра, нарушения техники имплантации ведут к дистальному или проксимальному смещению имплантируемого устройства вскоре после вмешательства. В последнем случае возможна миграция КФ в правое предсердие, правый желудочек и легочные артерии [16, 25, 35]. Описаны случаи повреждения трикуспидального клапана, перфорации правого желудочка и тампонады сердца [36, 37].
Технические ошибки имплантации, как правило, можно преодолеть по мере накопления опыта, что ведет к уменьшению числа ранних осложнений.
Поздние осложнения
Поздние осложнения имплантации включают: тромбоз КФ с возможным развитием ТЭЛА; синдром НПВ; повреждение стенок НПВ элементами фильтрующего устройства с проникновением их в двенадцатиперстную, тонкую или толстую кишку, поджелудочную железу, печень, надпочечник, почечную лоханку, аорту, позвоночник и другие забрюшинные структуры; фрагментацию КФ; дистальную или проксимальную миграцию фильтра либо его фрагментов в правые отделы сердца и легочные артерии, с возможным развитием перфорации миокарда и тампонады сердца; отклонение оси фильтра, неправильную позицию и фиксацию неоинтимой его обоймы, несущей крючок для удаления, к венозной стенке. Многие из поздних осложнений имплантации КФ представляют угрозу жизни пациента, и в отдаленном периоде недостатки КФ могут доминировать над их лечебной ролью. Доля больных с осложнениями увеличивается пропорционально времени нахождения КФ в просвете вены. Интересно, что при использовании съемных моделей осложнения наблюдают чаще [38, 39].
Для различных конструкций КФ характерны типичные осложнения. Конические фильтры имеют самый высокий риск повреждения сосудистой стенки (до 90–100%), фильтры с зонтичными или цилиндрическими элементами — тромбоза НПВ (30–50%), конический КФ Bard — фрагментации (40%) [10].
Для диагностики поздних осложнений применяют как весь комплекс современных средств визуализации, так и диагностическую лапаротомию. Иногда диагноз устанавливают только на аутопсии [17, 40–43].
Тромбоз КФ и НПВ
Тромбоз КФ и НПВ после имплантации современных моделей КФ диагностируют в 2,7–25% случаев [25, 39, 44].
Рутинное выполнение ангиосканирования значительно повышает частоту выявления тромбоза НПВ и КФ —
до 26,9% [45–48], а в течение первых 2 лет после имплантации — до 38,7% [49]. В качестве предрасполагающих к тромбозу факторов рассматривают низкую по отношению к почечным венам имплантацию КФ, отказ от антикоагулянтной терапии, гиперкоагуляцию, наличие злокачественного новообразования, особенности съемных биконических моделей КФ [22, 44, 50–52]. Следует учитывать, что у значительной доли пациентов с данным осложнением окклюзия КФ и НПВ служит показателем того, что фильтрующее устройство выполнило свое предназначение и предотвратило массивную эмболизацию легочного артериального русла [46, 50, 51]. По данным И.И. Затевахина с соавт., эмболию в КФ отмечают у 9,3% пациентов при сроке наблюдения до 10 лет [45]. Хроническая венозная недостаточность обеих нижних конечностей, развивающаяся в результате тромбоза НПВ и КФ, значительно ухудшает качество жизни человека, способна стать причиной инвалидизации, но жизни больного не угрожает, если тромбоз не распространяется проксимальнее КФ [50].
ТЭЛА после имплантации КФ
ТЭЛА после имплантации КФ диагностируют достаточно часто — в 1,1–7,7% наблюдений [8, 24, 44–46, 53]. Так, С.А. Athanasoulis et al. сообщили о развитии ТЭЛА у 97 из 1731 больного (5,6%), причем у 12 из них диагноз был поставлен лишь на аутопсии. Общее число летальных исходов от легочной эмболии в постимплантационном периоде (в среднем — через 135 сут) составило 65 (3,8%). Обращает на себя внимание тот факт, что клинический диагноз тромбоза НПВ после установки КФ был поставлен лишь 3,2% больных [25]. Установка КФ в супраренальную позицию увеличивает частоту постимплантационных легочных эмболий [54]. Использование инструментальных методов исследования повышает долю выявленных после имплантации КФ новых случаев ТЭЛА до 21% [49].
В качестве причины ТЭЛА, произошедшей несмотря на установку КФ, рассматривают формирование флотирующего тромба в «слепом кармане» между тромбированным КФ и почечными венами, неполное раскрытие, некорректную позицию КФ, миграцию его в правые отделы сердца [52, 55–57]. Возможно развитие легочной эмболии из участков венозного русла, не защищенных КФ (почечные, печеночные, гонадные вены, двойная НПВ, вены верхних конечностей, правые отделы сердца), «проскальзывание» тромбоэмболов через КФ, сформировавшиеся после тромбоза НПВ паракавальные венозные коллатерали [58]. По-видимому, такие клинические ситуации возможны, но значительно выше вероятность формирования эмболоопасного тромба на краниальной поверхности КФ. В литературе представлены единичные сообщения об открытом удалении эмболоопасных тромбов, сформировавшихся на краниальной поверхности фильтрующего устройства [52].
Пенетрация элементами КФ стенок НПВ и окружающих органов
Ограниченное проникновение элементов КФ в стенку НПВ является важным механизмом фиксации имплантируемого устройства. Однако постоянное давление металлической конструкции изнутри на стенку сосуда может вызывать проникновение ее острых частей за пределы НПВ и осложнения различной степени тяжести. Согласно совместному практическому руководству American College of Radiology и Society of Interventional Radiology, пенетрацией НПВ следует считать проникновение элемента устройства более чем на 3 мм от наружной поверхности сосуда [4].
Проанализировав базу данных MEDLINE за 1970–2014 гг., включающую 88 клинических исследований и 112 описаний клинических случаев, Z. Jia et al. сообщили, что из 9002 пациентов с 15 различными типами КФ пенетрация была обнаружена у 19% (1699 из 9002) больных и в 19% из этих наблюдений сопровождалась повреждением окружающих структур (322 из 1699). Только 8% пенетраций манифестировали яркой клинической симптоматикой (болевой синдром, геморрагические осложнения), 45% были бессимптомными, и в 47% случаев клинические проявления пенетрации описаны не были. Повреждение НПВ и окружающих структур потребовало открытого хирургического вмешательства, включая удаление КФ (n=63), эндоваскулярного стентирования или эмболизации (n=11), эндоваскулярного извлечения постоянной модели КФ (n=4), чрескожной нефростомии или стентирования мочеточника (n=3). Зарегистрированы 2 летальных исхода [17].
Впечатляет перечень органов и структур, в которые проникали элементы КФ. Чаще всего выявляли пенетрацию в двенадцатиперстную кишку, поясничный позвонок и аорту. Кроме того, описана пенетрация «ножек» КФ в тонкую и толстую кишку, диафрагму, поджелудочную железу, печень, почки и надпочечник, мочеточник и почечную лоханку, подвздошную, поясничную артерию, почечную артерию и вену, поясничные мышцы и лимфатические узлы. Пенетрацию выявляли значительно чаще после имплантации конических моделей КФ [17, 18, 59–61].
В ряде случаев элементы одного КФ пенетрировали в три и даже четыре органа одновременно [17]. О наблюдениях одновременного проникновения «ножек» фильтра в различные соседние органы сообщают многие исследователи [18, 41, 62, 63].
Клиницисты отмечают роль конической конструкции КФ в развитии пенетрации [21, 24, 61]. Так, Y. Saleh et al. описали пенетрацию всех 6 ножек фильтра Greenfield через 2 года после его имплантации [62]. Имплантируя животным КФ Gunther Tulip и Celect, А. Laborda et al. обнаружили, что уже через 1 мес. пенетрировали 59,3% «ножек» фильтров, при этом в ходе лапароскопии геморрагических осложнений не наблюдали [64]. Через 30 дней после имплантации КФ Cook Celect пенетрацию элементов устройства наблюдали у 39% пациентов, а через 90 дней — уже у 80% [18].
Высокий риск пенетрации неет и имплантация КФ модели Bird’s Nest. Обследуя больных в постимплантационном периоде, M.S. Starok et al. выявили сквозное повреждение стенок НПВ в 100% случаев [65].
Среди статистически значимых предпосылок к пенетрации НПВ элементами КФ отмечают длительное нахождение инородного тела в сосуде, женский пол и наличие злокачественного новообразования [18, 66].
Стандартное эндоваскулярное удаление КФ при повреждении «ножками» сосудистой стенки способствует регрессу болевого синдрома [38], однако может приводить к формированию псевдоаневризмы НПВ [67]. Пенетрация в окружающие органы и их разрушение во многих случаях выступают в качестве показаний к лапаротомии [41, 52, 68, 69]. Описано единственное наблюдение полностью лапароскопического удаления КФ Cook Celect, пенетрация элементов конструкции которого сопровождалась выраженным болевым синдромом, требующим назначения наркотических средств [70].
Пенетрация КФ в двенадцатиперстную кишку
Впервые пенетрация в двенадцатиперстную кишку стержней-распорок КФ Mobin-Uddin через 7 сут после его установки описана G.L. Irvin в 1972 г. [71]. В последующем число наблюдений прогрессивно возрастало, и в 2012 г. R.D. Maglor et al., проанализировав базы данных PubMed MEDLINE, Web of Sciences и LILACS (Literatura Latino-Americana e do Caribe em Ciências da Saúde), сообщили о 21 клиническом случае дуоденальной пенетрации. Наиболее часто данное осложнение развивалось при имплантации фильтров Greenfield, Bird’s Nest или Mobin-Uddin. У половины больных период после имплантации составлял 5 лет и более. Клинические проявления в виде болей в правых отделах живота и эпигастрии наблюдали у 11 больных, симптомы желудочно-кишечного кровотечения — у 5 пациентов (23%). Открытые оперативные вмешательства были выполнены 20 больным, причем только 10 пациентам проведены каватомия и удаление фильтра. В остальных случаях отсекали и удаляли пенетрирующую в кишку «ножку» КФ, а дефект кишки ушивали [61].
Разрушение элементами КФ стенки двенадцатиперстной кишки может сопровождаться формированием дуоденальных язв, профузным желудочно-кишечным кровотечением [72–74].
Наряду с работами, посвященными описанию оптимальной техники открытого извлечения фильтрующего устройства и его элементов [27, 52, 59, 68, 69, 74], в литературе представлены сообщения об успешном эндоваскулярном удалении КФ, пенетрирующих в двенадцатиперстную кишку [75, 76]. Кроме того, интерес представляет сообщение R. DuraiRaj et al. об эффективном консервативном лечении данного осложнения у пожилой больной с высокой степенью операционного риска [77].
Пенетрация КФ в тонкую или толстую кишку
J.D. Balshi et al. описали 2 случая перфорации тонкой кишки ножками фильтра Greenfield, потребовавшей выполнения лапаротомии, ушивания кишки и удаления фильтра [78]. Пенетрация ножки КФ в брыжейку тонкой кишки может стать причиной фиксации тонкой кишки к месту повреждения с формированием заворота и тонкокишечной непроходимости [59].
Мы нашли в литературе только одно описание пенетрации КФ (Cook Celect) в толстую кишку. Осложнение протекало бессимптомно, «ножка» КФ была обнаружена в ходе колоноскопии через 2 года после имплантации. Больной был успешно оперирован [79].
Пенетрация КФ в поджелудочную железу и печень
О пенетрации КФ Cook Celect в поджелудочную железу у 2 больных из обследованных 265 сообщают D. Zhou et al. [18]. Kalva SR et al., имплантируя КФ в супраренальную позицию, обнаружили пенетрацию фильтра в печень и поджелудочную железу у 2 больных из 70 [54]. Возможна сочетанная пенетрация КФ конической конструкции в двенадцатиперстную кишку и поджелудочную железу [42]. Последствием повреждения поджелудочной железы может стать формирование псевдокисты с развитием механической желтухи [80]. Описана пенетрация фрагментов конструкции КФ в паренхиму печени при неудачной попытке эндоваскулярного удаления устройства [81].
Пенетрация КФ в аорту
Тесная связь НПВ с брюшным отделом аорты создает реальные предпосылки для ее повреждения. В литературе представлены сообщения о пенетрации «ножек» КФ в аортальную стенку [19, 82], что может приводить к развитию забрюшинной гематомы, псевдоаневризмы аорты [60, 83], аортокавальной фистулы [63] и пристеночного тромбоза аорты [41]. Сходные последствия влечет за собой повреждение «ножкой» КФ поясничной артерии [84–86]. Данные осложнения наблюдают после имплантации КФ конической конструкции и КФ Bird’s Nest. Основным клиническим проявлением осложнения выступает болевой синдром [60, 63, 82]. Оптимальным методом лечения в такой ситуации является эндоваскулярное удаление КФ [82]. При формировании псевдоаневризмы успешно выполняют селективную эмболизацию поясничной артерии [82] или установку стент-графта [60]. Наряду с эндоваскулярными вмешательствами выполняют открытые операции [19, 41, 83].
Пенетрация в поясничные позвонки
Пенетрация КФ в поясничный позвонок (L2–L3) может вызывать сильные боли в спине, требующие назначения наркотических средств, и сопровождаться повреждением других органов [63, 87, 88]. Наряду с этим описано бессимптомное течение данного осложнения [89]. При изолированном повреждении поясничного позвонка выполняют эндоваскулярное удаление КФ [87] либо ограничиваются консервативным лечением [88, 89]. Комбинированное повреждение требует выполнения открытого оперативного вмешательства [63]. Для удаления КФ из просвета НПВ наряду с каватомией применяют извлечение предварительно сложенного КФ через прокол в стенке НПВ либо через поясничную вену [90].
Пенетрация КФ в органы мочевыделительной системы
Типичная имплантация КФ тотчас дистальнее почечных вен при развитии пенетрации его элементов может осложняться повреждением почечных вен, лоханки и мочеточника [91–93]. Клинические проявления представлены гематурией или признаками блока мочеточника [93, 94]. Компьютерная томография и уретероскопия позволяют уточнить диагноз. Наряду с эндоваскулярным и открытым удалением КФ либо его элементов выполняют нефростомию и стентирование мочеточника. При асимптомном течении возможно консервативное лечение [93, 94].
Дистальная и проксимальная миграция КФ
Миграцию КФ авторитетные международные руководства определяют как смещение устройства более чем на 2 см в краниальном либо каудальном направлении по отношению к первоначальной позиции [4]. Частота поздней дистальной миграции КФ достигает 3,2% случаев [48]. Дистальная миграция может сопровождаться пенетрацией в брыжейку тонкой кишки и выраженным болевым синдромом [95]. О спонтанном смещении КФ из инфраренальной в супраренальную позицию с развитием забрюшинной гематомы сообщают R. Satya et al. [96]. Проксимальную миграцию в правое предсердие с фатальным исходом может спровоцировать массивная тромбоэмболия в КФ [97].
Миграция КФ или его фрагментов в правые отделы сердца и ветви легочных артерий
C.A. Owens et al., проанализировав базы данных MEDLINE и OVID с 1967 по 2008 г., опубликовали сообщение о 98 наблюдениях миграции КФ в правое предсердие (n=22), правый желудочек (n=17), легочные артерии (n=11) либо фиксации фильтра в трикуспидальном клапане. Ведущими клиническими симптомами были аритмия (45,5%) и боли в грудной клетке (33,3%), отсутствовали клинические проявления у 22,7% больных. В общей сложности 34 больным (34,7%) для удаления КФ была выполнена торакотомия (умерло 2 больных), 31 — успешное эндоваскулярное вмешательство. Остальным больным по разным причинам оперативное вмешательство не выполняли либо попытка эндоваскулярного удаления была безуспешной (умерли 11 больных) [56]. В качестве причин поздней миграции КФ авторы предполагают неполное его раскрытие, большой диаметр НПВ, массивную тромбоэмболию в КФ, разрушение КФ, смещение его проводником при установке центрального катетера [56, 98, 99]. М. Porcellini et al. описали миграцию КФ TrapEase, дислоцированного в результате эмболизации тромбом, в правое предсердие у больного с открытым овальным окном, что дополнительно осложнилось ишемическим инсультом и тромбоэмболией плечевой артерии [100].
Фрагментация КФ, перфорация миокарда, тампонада сердца
Значительную опасность жизни больного представляют разрушение конструкции КФ и миграция (как правило, проксимальная) его фрагментов. Фильтрующие устройства выполняют из нержавеющей стали, титана и различных сплавов. Однако эта гибкая и изящная конструкция находится в условиях постоянного воздействия статических, динамических нагрузок, органических и неорганических веществ плазмы крови. В результате разрушение КФ наблюдают достаточно рано после его имплантации. Так, W.R. Chitwood et al. описали разрушение КФ Bird’Nest уже через 4 сут после его имплантации, причем фрагменты устройства мигрировали в правое предсердие и легочные артерии [101]. Обследуя больных с имплантированными в течение 5 лет КФ Bard Recovery, W. Nicholson et al. обнаружили разрушение конструкции фильтра и эмболизацию фрагментами, включая перфорацию миокарда и гемоперикард, у 25% больных [102]. Фрагменты КФ ALN через 10 лет после его имплантации наблюдали у больного одновременно в ветви легочной артерии, печеночной вене, эпикарде, стенке правого желудочка и межжелудочковой перегородке [103]. M.D. Tam et al. описали миграцию фрагментов КФ в легочные артерии, правый желудочек, почечные, подвздошные и бедренные вены [104]. Фиксация отломка КФ в трабекулярных мышцах может приводить под воздействием сердечных сокращений к перфорации стенки предсердия или желудочка, гемоперикарду и тампонаде сердца, что требует выполнения экстренного оперативного вмешательства [101, 102, 105].
В ряде случаев удается удалить мигрировавший в правый
желудочек КФ и его фрагменты эндоваскулярно [11, 106].
При неудаче внутрисосудистого вмешательства у стабильных больных с высоким операционным риском возможно консервативное лечение [107]. Фрагменты КФ из ветвей легочных артерий, как правило, удалить не удается [108].
Ангуляция КФ и фиксация его неоинтимой к стенке НПВ
Через несколько лет после установки КФ наблюдают изменение его оси со смещением обоймы устройства в почечную или поясничную вену [4, 52, 109]. Это явление рассматривают как следствие рубцового процесса, частичного разрушения конструкции, пролиферации неоинтимы. В результате обойма съемной модели КФ, несущая крючок для его удаления, оказывается закрытой эндотелием, рубцовой тканью или пристеночными тромботическими массами и недоступной для удаляющей КФ петли. Биконические фильтры (OptEase, TrapEase) и фильтры комбинированной конструкции контактируют с эндотелием своими боковыми гранями на значительной площади, в связи с чем фиксация их к стенке полой вены происходит быстрее. Превращение съемной модели КФ в постоянный фильтр представляет опасность в случае его некорректной позиции, особенно у молодых больных с ожидаемым длительным периодом жизни с инородным телом. При наличии показаний возможно прямое открытое удаление такого «съемного» фильтра [52, 110].
Смещение КФ интравенозными проводниками описано в ряде работ, поскольку человека с ранее имплантированным КФ в течение жизни могут неоднократно госпитализировать по различным причинам и в процессе лечения выполнять катетеризацию центральной вены. Обратная тракция проводника, запутавшегося в элементах конструкции КФ, способна не только сместить и разрушить эндоваскулярное устройство, но и травмировать стенку полой вены [111].
Заключение
Пути стратегического решения проблемы минимизации жизнеугрожающих осложнений имплантации КФ клиницисты видят в системной профилактике ВТЭО у госпитальных больных, в отказе от рутинного применения фильтрующих устройств, строгом определении показаний к их использованию, приоритете съемных моделей фильтров [2, 3, 51]. Перспективное направление — создание биоабсорбируемых моделей КФ. Экспериментальные данные [112] обнадеживают исследователей, однако опыт клинического применения в настоящее время отсутствует.
Между тем повседневная клиническая практика уже сейчас требует решения значительного числа тактических задач. В настоящее время количество людей, живущих с имплантированными КФ, вынужденных пожизненно сосуществовать с далеко не безопасным, как показал опыт, инородным телом в НПВ и составляющих, таким образом, группу потенциального риска развития осложнений, исчисляется сотнями тысяч. С увеличением длительности нахождения фильтрующего устройства в магистральном сосуде вероятность развития жизнеугрожающих осложнений увеличивается. В последние годы в США отмечают увеличение числа судебных исков, связанных с поздними осложнениями имплантации КФ [113]. На основании баз данных MEDLINE и FDA MAUDE для идентификации 23 типов КФ, применяемых в США, и связанных с ними осложнений разработано интерактивное мобильное приложение IVC Filter Compendium на платформах iOS (Apple) и Android (Google) [10].
При поступлении больного с неясной клинической картиной и проведении дифференциальной диагностики рекомендуют учитывать в качестве этиологического фактора патологического процесса наличие инородного тела в НПВ с возможной его пенетрацией в окружающие органы, фрагментацией, миграцией отломков и даже перфорацией миокарда [42, 56, 61].
В ходе выполнения лапаротомии врачам хирургических специальностей следует помнить о большой частоте бессимптомных пенетраций ножками КФ стенки НПВ во избежание повреждения органов брюшной полости при ее ревизии и собственных рук.
В настоящее время только формируется основанный на значимом числе собственных наблюдений и подтвержденный клинической практикой лечебно-диагностический алгоритм у больных с поздними осложнениями имплантации КФ, который уже сейчас является необходимым как сосудистым, так и общим хирургам, и его актуальность с каждым годом будет только возрастать.
Источник: www.rmj.ru
Международная классификация болезней 10-го пересмотра
Согласно международной классификации 10 пересмотра венотромбоз может формироваться на разных уровнях, поэтому тромбоз глубоких вен нижних конечностей (код по МКБ 10 – I80) выделен в отдельный подкласс «Болезни вен, лимфатических сосудов и лимфоузлов, не классифицированные в других рубриках. Флебит и тромбофлебит».
Что касается синдрома эмболии легочной артерии, то он классифицируется в МКБ 10 в рубрике «Легочное сердце и нарушения легочного кровообращения».
Тромбоэмболия легочной артерии (код по МКБ 10 –I26, легочная эмболия) характеризуется частичным/полным перекрытием просвета крупных либо мелких сосудов легочной артерии или ее ствола, в результате чего происходят гемодисциркуляторные нарушения, повышается артериальное давление в малом круге в сочетании с кардиореспираторными расстройствами или геморрагическим инфарктом легкого.
Несмотря на то, что МКБ с 1999 года была неоднократно пересмотрена и дополнена, код ТЕЛА по МКБ 10 пока не изменился. Следующий пересмотр международного классификатора (МКБ-11) предполагается в 2018 году.
Механизм формирования тромбоза вен и ТЭЛА
 Как правило, тромб образуется вследствие замедления тока крови по сосудам, увеличения ее вязкости, нарушений в свертывающей системе крови. Помимо этого тромбообразованию способствует повреждение внутренней поверхности венозных сосудов инфекционными или аллергическими агентами, что делает интиму шероховатой и создает благоприятные условия для формирования небольшого, но неизменно увеличивающегося в размерах сгустка.
Как правило, тромб образуется вследствие замедления тока крови по сосудам, увеличения ее вязкости, нарушений в свертывающей системе крови. Помимо этого тромбообразованию способствует повреждение внутренней поверхности венозных сосудов инфекционными или аллергическими агентами, что делает интиму шероховатой и создает благоприятные условия для формирования небольшого, но неизменно увеличивающегося в размерах сгустка.
Наиболее опасен в этом отношении флотирующий тромб, который бывает длиной до 15-20 см, при этом его конец, направленный в сторону бедра, не закреплен к стенке и свободно расположен внутри сосуда. После отрыва кусочек тромба с током крови двигается по нижней полой вене в сторону сердца.
Попав из правого желудочка сердца в легочную артерию, тромб провоцирует спазм капилляров, резкий выброс веществ, вызывающих массированное склеивание тромбоцитов и закупорку просвета сосуда, в результате чего возникает резкое увеличение давления в венах малого круга, что ведет к быстрому понижению системного артериального давления и нарушению кровообращения в миокарде. Позже присоединяется одышка с затрудненным вдохом, синюшность кожи и слизистых оболочек, появляются яркие клинические симптомы ТЭЛА.
Клиническая классификация и клиника ТЭЛА
Клиническая классификация тромбоэмболии сосудов легочной артерии включает в себя форму течения заболевания с указанием места закупорки сосуда и основные ТЭЛА симптомы:
| Форма |
Уровень окклюзии сосуда |
Клинические проявления |
|
Тяжелая |
Легочный ствол, главные ветви легочной артерии |
Сверхострое течение с кинжальными болями за грудиной, резкой инспираторной одышкой, усиливающей при дыхании и кашле, синюшность в сочетании с общей бледностью кожи, сильное снижение АД вплоть до коллапса, липкий пот, синдром острого легочного сердца, аритмия. В ряде случаев – бессознательное или шоковое состояние, судороги. |
|
Среднетяжелая |
Долевые сегментарные ветки |
Острое начало с быстро нарастающей дыхательной недостаточностью (средней интенсивности загрудинные боли, тяжесть в правом подреберье, инспираторная одышка, тахипноэ, акроцианоз, бледность кожи), признаки инфарктной пневмонии или инфаркта легкого (кашель с примесью крови, головокружение), правожелудочковая недостаточность. |
|
Легкая |
Мелкие ветви |
Течение рецидивирующее, могут быть слабовыраженные или мозаичные симптомы, на основании которых нельзя уверенно поставить диагноз ТЭЛА. В некоторых случаях больных беспокоит одышка с затрудненным вдохом, пароксизмальная одышка в сочетании с тахикардией, слабость, мушки перед глазами, склонность к гипотонии, обморокам, коллаптоидным состояниям, клинические и рентгенологические признаки пневмонии, беспричинный длительный субфебрилитет, боли в правом подреберье и животе вследствие переполнения печени кровью. |
ЭКГ признаки ТЭЛА в основном неспецифичны, но при остром и сверхостром течении наиболее характерен острый коронарный синдром — экстрасистолия, мерцательная аритмия предсердий, суправентрикулярная пароксизмальная тахикардия, ишемия миокарда.
Основные признаки тромбоза глубоких вен нижних конечностей
Учитывая, что ТЭЛА развивается чаще всего как осложнение ТГВ нижних конечностей, насторожить врача и самого пациента должны следующие признаки:
- Сильные боли, снижение чувствительности, покалывание, ощущение ползания мурашек в одной из нижних конечностей;
- Слабый пульс на ноге в области голеностопного сустава и на бедре;
- Локальное посинение конечностей на фоне мраморной кожи;
- Отеки, некрозы, гангрены с четкой демаркационной линией или язвенный распад на пораженной конечности;
- Стойкой беспричинное повышение температуры тела до субфебрильных цифр;
- Увеличение лейкоцитов и повышение СОЭ в клиническом анализе крови.
 Эти клинические симптомы указывают на то, что у пациента образовался тромбоз глубоких вен нижних конечностей и требуется безотлагательная медицинская помощь, а также профилактические мероприятия, препятствующие формированию ТЭЛА.
Эти клинические симптомы указывают на то, что у пациента образовался тромбоз глубоких вен нижних конечностей и требуется безотлагательная медицинская помощь, а также профилактические мероприятия, препятствующие формированию ТЭЛА.
Диагностика ТГВ нижних конечностей и ТЭЛА
Установить причину появления окклюзии сосудов, отходящих от легочной артерии, помогают тщательно собранный анамнез и инструментальные исследования. При подозрении на ТЭЛА или тромбоз глубоких вен, диагностика также должна состоять из лабораторных и инструментальных методов.
| Диагностика ТГВ нижних конечностей |
Диагностика ТЭЛА |
| Общий и биохимический анализ крови | Селективная ангиопульмография |
| Общий анализ мочи | Рентгенографическое исследование легких |
| Жгутовая и маршевая проба | Перфузионное сканирование легких с использованием альбумина или меченного 99Tc |
| Флебография | КТ грудной клетки с контрастированием |
| Доплеровское ультразвуковое сканирование | ЭКГ |
| Дуплексное ангиосканирование | |
| Реовазография |
Лечебная тактика при ТЭЛА
Частичное или полное перекрытие ствола или крупных сосудов легочной артерии необходимо купировать в течение первых же часов от момента появления. Неотложная помощь при ТЭЛА состоит из парентерального назначения фибринолитических (тромборастворяющих) препаратов для восстановления проходимости легочной артерии. Для профилактики рецидива назначают низкомолекулярный гепарин или антагонист витамина К, чаще всего варфарин.
 Кроме того, при ТЭЛА клинические рекомендации 2017 г. Европейского общества кардиологов учитывают вероятность возникновения кровотечений, поэтому медикаментозное лечение тромбоэмболии легочной артерии в первую очередь направляют на купирование ведущих симптомов, а антикоагулянты и фибринолитики применяют с большой осторожностью. В связи с этим неотложная терапия состоит из следующих мероприятий:
Кроме того, при ТЭЛА клинические рекомендации 2017 г. Европейского общества кардиологов учитывают вероятность возникновения кровотечений, поэтому медикаментозное лечение тромбоэмболии легочной артерии в первую очередь направляют на купирование ведущих симптомов, а антикоагулянты и фибринолитики применяют с большой осторожностью. В связи с этим неотложная терапия состоит из следующих мероприятий:
| Неотложна терапия при ТЭЛА |
Медикаментозные средства |
| снятие болевых ощущений в загрудинной области | наркотические и ненаркотические анальгетики |
| нормализация артериального давления и коронарного кровообращения | сосудосуживающие препараты, инфузионные растворы |
| приостановление тромбообразования и уменьшение нарастания тромба в размерах | низкомолекулярный гепарин, варфарин |
| устранение явлений кислородной недостаточности | подача увлажненного кислорода |
| устранение спазма бронхиального дерева | Эуфиллин парентерально, струйно |
Лечение ТГВ нижних конечностей
Первое, что советуют врачи больному, у которого поражены глубокие вены нижних конечностей – лечение тромбоза с помощью простых немедикаментозных методов:
- Смена двигательного режима в сторону увеличения физической активности — ходьба с палками, бег, езда на велосипеде, плавание, водная аэробика;
- Применение постурального дренажа – подъем ног выше уровня сердца на 20-30 минут несколько раз в день;
- Замена обычных колгот и чулок на компрессионные (4 класса компрессии);
- Нормализация массы тела;
- Изменение пищевых привычек.
Диета при тромбозе глубоких вен нижних конечностей назначается с целью увеличения в рационе сырых овощей и фруктов богатых клетчаткой и витаминами, снижения уровня углеводов за счет уменьшения потребления сладких и мучных блюд, отказа или значительного снижения количества соленой, острой, жирной и жареной пищи, которая усиливает жажду.
Помимо немедикаментозных мероприятий, все пациенты должны пройти курс лечения флеботропными лекарственными препаратами (Диосмин, Детролекс, Вазокет), а при необходимости и антитромбоцитарными или гемореологически активными препаратами (Актовегин).
Медикаментозное и эндохирургическое лечение
 Несмотря на то, что «золотым» стандартом лечения тромбоза глубокой вены является назначение антикоагулянтов и, в частности, антагонистов витамина К и низкомолекулярного гепарина, в некоторых случаях (высокая группа риска по развитию ТЭЛА или стандартные медикаментозные средства противопоказаны) целесообразно применение чрескожных эндоваскулярных методик, например, установка кава-фильтра (КФ), который помимо прочего служит профилактическим средством препятствующим развитию ТЕЛА.
Несмотря на то, что «золотым» стандартом лечения тромбоза глубокой вены является назначение антикоагулянтов и, в частности, антагонистов витамина К и низкомолекулярного гепарина, в некоторых случаях (высокая группа риска по развитию ТЭЛА или стандартные медикаментозные средства противопоказаны) целесообразно применение чрескожных эндоваскулярных методик, например, установка кава-фильтра (КФ), который помимо прочего служит профилактическим средством препятствующим развитию ТЕЛА.
Приспособление, внешне напоминающее зонт, тюльпан или сетку, является прекрасным средством защиты от развития окклюзии легочной артерии если:
- существуют противопоказания для назначения антикоагулянтов или тромболитиков;
- в недавнем прошлом пациент перенес геморрагический инсульт, обширную полостную операцию, множественную травму;
- в анамнезе у больного указано злокачественное новообразование, гемофилия.
Имплантация кава-фильтра при тромбозе — наиболее подходящее средство профилактики не только развития тромбоэмоболии легочной артерии, но и ее рецидива при условии безуспешности предшествующей антикоагулянтной терапии.
Имплантация КФ проводится под местной анестезией. Местом введения имплантата, как правило, является бедренная вена – в нее вводят полую иглу, через которую пропускают тонкий катетер. Под рентген-контролем катетер продвигают до нужного уровня и затем отсоединяют от него КФ, способный самостоятельно раскрываться и фиксироваться к внутренней стенке сосуда. После закрепления кава-фильтра катетер удаляют, а на место прокола накладывается давящая повязка.
Изредка в месте прокола образуется небольшая гематома, которая проходит без лечения. Через двое суток пациент возвращается к привычному для него образу жизни.
Источник: endovascular.moscow
