Когда и зачем ее проводят?
Когда в коронарных сосудах образуются тромбы или атеросклеротические бляшки, то просвет в них сужается, ограничивая доступ крови к миокарду.
Без необходимого снабжения, начинается ишемия — опасное сердечно-сосудистое заболевание, вследствие которого может произойти инфаркт и последующая остановка сердца.
Характерные симптомы ишемической болезни — боль в груди, одышка, слабость, ощущение нарушения сердечного ритма.
Для ее лечения, если медикаментозных средств оказывается недостаточно, и проводят данную операцию.
Показания и противопоказания
Реваскуляризация миокарда назначается при ишемической болезни, осложненной:
- Стенокардией, невосприимчивой к медикаментам.
- Инфарктом миокарда в острой форме.
- Сердечной недостаточностью.
- Аритмией желудочков.
- Ишемическим дефектом, почти полным сужением коронарных артерий.
Противопоказания к данному хирургическому вмешательству:
- Почечная недостаточность.
- Патология сердечных клапанов.
- Аневризма левого желудочка сердца.
- Неярко выраженная ишемия, при которой больной не получал медикаментозного лечения.
- Общее тяжелое состояние пациента, не позволяющее провести хирургическое лечение.
- Онкологические заболевания.
Проведение операции пожилым людям сопряжено с определенным риском, но сам по себе старческий возраст не является противопоказанием. Принимая решение, врачи руководствуются в первую очередь показаниями к хирургическому лечению.
Причина для реваскуляризации должна быть весомой, поскольку подобное вмешательство грозит высоким риском осложнений и возможного летального исхода после операции. Тип операции выбирает только врач.
Прямые методы
Хирургическая реваскуляризация проводится с помощью прямых и непрямых методов.
К прямым относятся:
- Аортокоронарное шунтирование.
- Коронарное стентирование.
- Баллонная ангиопластика.
Все эти способы подразумевают восстановление кровотока искусственным путем: благодаря использованию шунтов, стентов или баллонов. Главная цель подобного вмешательства — восстановление кровоснабжения сердечной мышцы.
Шунтирование
Коронарное шунтирование — это очень непростая и дорогая по стоимости операция.
Для ее успешного проведения необходима предварительная подготовка пациента и наличие команды специалистов: хирургов, кардиологов, реаниматологов, анестезиологов.
Перед ее проведением пациенту необходимо:
- Привести в норму артериальное давление.
- Нормализовать уровень сахара в крови.
- Стабилизировать количество сердечных сокращений.
А также, чтобы выявить противопоказания, пациента полностью обследуют.
Помимо общих запретов к проведению вмешательства этим методом, коронарное шунтирование не проводится при:
- Некоторых видах стенозов, когда просвет артерии почти полностью сужен.
- Недавно перенесенном инсульте.
Суть операции состоит в установке шунтов — искусственных проходов, соединяющих пораженную артерию с сердцем. Для восстановления кровообращения кровь пускают в обход пораженного участка.
В качестве материала для шунта используют подкожные вены пациента с плеч или бедер.
Ход операции:
- Врач-анестезиолог вводит пациента в общий наркоз.
- На грудине делают продольный разрез.
- С помощью данных ангиографии выбирают донорскую вену.
- Через небольшой прокол забирают сосуд для шунта.
- Чтобы у пациента не образовались тромбы, ему вводят гепарин.
- Подключают аппарат искусственного кровообращения.
- Накладывают шунт. За одну операцию их не ставят больше чем пять штук.
- Восстанавливают работу сердца и зашивают разрез.
Как правило, срок службы шунтов составляет примерно 5 лет. После операции высок риск осложнений, таких как инфицирование раны или неконтролируемое кровотечение. Цена подобной операции в клиниках довольна высока.
Стентирование
Метод коронарного стентирования заключается в установке специального стента в месте сужения артерии, питающей сердце. Он представляет собой металлический конус, изготовленный из мелкоячеистой сетки.
Используя катетер, сложенный стент вводят в артерию через прокол, наблюдая за операцией с помощью рентгенотелевидения.
Затем его устанавливают в месте сужения и расправляют. После этого он расширяет собой стенки артерии, восстанавливая кровоток.
В отличие от аортокоронарного шунтирования, стентирование — малоинвазивная процедура.
Ангиопластика
Баллонная ангиопластика по принципу действия схожа с коронарным стентированием: в суженную артерию с помощью катетера вводят баллончик и надувают, тем самым расширяя просвет сосуда.
Перед этим, с помощью ангиографии, специального рентгена с контрастом, выясняется точное расположение места сужения артерий.
Сама операция проводится следующим образом:
- Используя местную анестезию на бедре делают небольшой прокол в бедренную артерию.
- Через него в кровеносную систему вводят катетер с баллоном на конце.
- Под рентгеновским наблюдением баллон доставляют в суженное место и надувают его, расширяя просвет сосуда.
- После того, как сосуд достигнет необходимых размеров, баллон сдувают и катетер вместе с ним вынимают, а место прокола зашивают.
У этого вида лечения ишемии меньше всего противопоказаний, поскольку операция эндоваскулярная, миниинвазивная и низкотравматичная.
По сравнению с другими способами оперативного вмешательства у ангиопластики самый короткий период реабилитации.
Непрямые методы
Непрямая реваскуляризация проводятся с помощью лазерного и ударно-волнового метода.
К ним прибегают если оперативное вмешательство по каким-то причинам невозможно, а медикаментозной терапии недостаточно.
С использованием лазера
Трансмиокардиальная лазерная реваскуляризация миокарда является новым, экспериментальным методом лечения ишемии сердца, но несмотря на этот факт, ее начинают применять все чаще.
Суть ТМЛР заключается в воздействии лазера на миокард. Лазерным лучом в его толще делают отверстия и создают каналы, по которым идет кровоток. Через несколько месяцев они закрываются, но миокард остается реваскуляризирован.
К этому способу прибегают в основном если по каким-либо причинам шунтирование пациенту противопоказано.
Ударно-волновой метод
Также экспериментальный метод, который редко используется из-за отсутствия доказательств его эффективности.
При таком лечении на сердце направляют акустические волны, частота которых лежит в инфразвуковом диапазоне. Их воздействие стимулирует рост артерий и капилляров в пораженной зоне миокарда.
Процедура абсолютно безболезненна.
Возможные осложнения и реабилитация
Самый высокий риск осложнений и долгий период реабилитации наблюдается у коронарного шунтирования, поскольку это серьезное вмешательство, для проведения которого необходимо сделать большой разрез. Операция проводится на открытом, работающем сердце.
На риск возникновения осложнений влияет возраст пациента. Считается, что легче всего оперативное вмешательство переносится в возрасте от 30 до 55 лет. Осложнениями могут выступать — кровотечение, сердечная недостаточность и воспаление из-за инфицирования раны.
А вот после аортокоронарного стентирования период реабилитации составляет всего несколько дней. Осложнений, как правило, не возникает.
Период восстановления после проведения баллонной ангиопластики также небольшой. Осложнения могут возникнуть в течение шести месяцев: обратное сужение артерии, закупорка венечной артерии тромбом, в редких случаях – разрыв артерии. При сужении сосудов, после этой процедуры назначают блокирующие кальций лекарственные средства.
Лазерная реваскуляризация имеет короткий период реабилитации и редко приводит к негативным последствиям.
Ударно-волновая терапия, помимо недоказанности ее эффективности, имеет ряд осложнений, выражающихся в росте холестериновых бляшек, замещении отмершей ткани соединительной. Как итог – результат такого лечения непредсказуем.
Если не соблюдать правильный рацион, не вести здоровый образ жизни и не придерживаться рекомендаций лечащего врача, то только от одной операции проблемы с сердцем не исчезнут, они лишь временно не будут беспокоить.
Источник: infoserdce.com
Реваскуляризация миокарда
Общая информация
Реваскуляризация миокарда – широкое понятие, включающее как операцию КШ, так и различные виды ЧКВ на коронарных артериях. Наиболее известна и распространена баллонная ангиопластика, которую можно сочетать с другими воздействиями на атеросклеротически измененную коронарную артерию: установкой металлического каркаса – эндопротеза (стента), выжиганием бляшки лазером, разрушением бляшки быстро вращающимся буром и срезанием бляшки специальным атеротомическим катетером. Реваскуляризация, как и фармакотерапия, преследует 2 цели: улучшение прогноза (профилактика ИМ и ВС, уменьшение или полную ликвидацию симптомов. Основными факторами, которые определяют выбор метода лечения, являются индивидуальный сердечно-сосудистый риск и выраженность симптомов. Коронарное шунтирование Выделяют два показания к проведению КШ: улучшение прогноза (снижение смертности; снижение риска развития ИМ убедительно не доказана) и уменьшение симптомов. По влиянию на прогноз, операция КШ не выявила преимуществ перед фармакотерапией у пациентов группы низкого риска (ежегодная смертность – менее 1%). По данным мета-анализа, КШ улучшало прогноз только в группах среднего и высокого риска, однако в группе среднего риска 5-летняя смертность на фоне медикаментозной терапии составляла 13,9%, а ежегодная смертность – 2,8%, что по современным стандартам является высоким.
>При анализе исследований были установлены анатомические изменения коронарных артерий, при которых КШ способно улучшить прогноз: — значительный стеноз главного ствола левой коронарной артерии; — значительный проксимальный стеноз 3 основных коронарных артерий; — значительный стеноз 2 основных коронарных артерий, включая выраженный стеноз проксимальной части левой передней нисходящей коронарной артерии. Критерием значимого стеноза в этих исследованиях было сужение основных коронарных артерий ≥ 70% и главного ствола левой коронарной артерии ≥ 50%. При дисфункции левого желудочка хирургическое лечение имеет преимущества перед фармакотерапией (European Coronary Artery, North American CASS). Доказано, что хирургическое вмешательство уменьшает симптомы и ишемию миокарда и улучшает качество жизни больных СтСт. Эти эффекты наблюдаются чаще, чем улучшение прогноза. Следует тщательно взвешивать риск и пользу оперативного вмешательства у пациентов группы низкого риска, у которых его целью является только уменьшение симптомов. Периоперационная летальность при КШ составляет, в среднем, 1-4%. В последние 20 лет стандартом стало шунтирование левой передней нисходящей артерии с помощью левой внутренней грудной артерии и использование подкожной вены для шунтирования других артерий.
есте с тем, остается проблемой стенозирование венозных шунтов. В крупных исследованиях показано, что использование левой внутренней грудной артерии для КШ улучшает выживаемость и снижает частоту позднего ИМ, рецидивирующей стенокардии и необходимость в повторных вмешательствах на коронарных артериях. Накоплен опыт использования лучевой артерии. В этом случае, частота сохранения проходимости артерии превышает 90% в течение 3 лет. У больных, страдающих серьезными сопутствующими заболеваниями, целесообразно выполнять малоинвазивные вмешательства без искусственного кровообращения, которые могут привести к снижению периоперационной летальности и риска осложнений. Однако в настоящее время завершены рандомизированные исследования, которые показали отсутствие разницы исходов малоинвазивных вмешательств и стандартных операций в течение первых 3-х лет. В другом рандомизированном исследовании с ангиографическим контролем через 3-6 месяцев было выявлено снижение частоты сохранения проходимости шунта после малоинвазивных операций (90 против 98%). Чрескожные вмешательства на коронарных артериях Коронарная ангиопластика со стентированием у больных СтСт и подходящей анатомией коронарных артерий позволяет провести дилатацию одного или нескольких сосудов с высокой вероятностью восстановления их проходимости и приемлемым риском. Риск смерти после обычной ангиопластики составляет около 0,3-1%. Согласно данным исследования AVERT, у больных СтСт, относящихся к группе низкого риска, гиполипидемическая терапия не уступает ЧКВ на коронарных артериях в профилактике ишемических исходов.
нако ЧКВ дают более выраженный клинический антиангинальный эффект. Согласно результатам исследования COURAGE, вероятность смерти и нефатального инфаркта миокарда при наблюдении в течение 4,6 лет ничем не отличалась в группах больных, которым изначально выполнили коронарную ангиопластику со стентированием, и затем получавшим агрессивную медикаментозную терапию. Стентирование сосудов и использование стентов с лекарственным покрытием При мета-анализе 29 исследований у 9918 больных не было выявлено различий в смертности или частоте ИМ после стентирования коронарных артерий и стандартной баллонной ангиопластики. Однако стентирование приводит к снижению частоты рестеноза и необходимости в повторных вмешательствах на коронарных артериях. Согласно рандомизированным исследованиям (RAVEL), стенты с лекарственным покрытием (паклитаксель, сиролимус, эверолимус) значительно улучшают результаты лечения и снижают риск рестеноза и неблагоприятных исходов, включая необходимость в повторной реваскуляризации целевой артерии. Показания к реваскуляризации Кандидатами на реваскуляризацию миокарда являются больные, у которых имеются показания к коронарной ангиографии. Дополнительными показаниями являются следующие: — медикаментозная терапия не обеспечивает удовлетворительный контроль симптомов; — неинвазивные методы демонстрируют наличие распространенной зоны ишемии; — высокая вероятность успеха при допустимом риске послеоперационных осложнений; — больной предпочитает инвазивное лечение и имеет полную информацию о риске, связанном с вмешательством.
целесообразно рекомендовать инвазивное лечение больным, у которых риск периоперационной смерти превышает расчетную ежегодную смертность. Выбор метода реваскуляризации основывается на следующих факторах: — риск развития осложнений и смерти после вмешательства; — вероятность успеха, включая техническую возможность выполнения ангиопластики или КШ; — риск рестеноза или окклюзии шунта; — полнота реваскуляризации; — наличие сахарного диабета; — опыт лечебного учреждения; — желание больного. Противопоказания к реваскуляризации миокарда — Больные со стенозированием одной или 2 коронарных артерий без выраженного проксимального сужения передней нисходящей артерии, у которых имеются легкие симптомы стенокардии или отсутствуют симптомы и не проводилась адекватная медикаментозная терапия. В таких случаях инвазивное вмешательство нецелесообразно так же, как и при отсутствии признаков ишемии миокарда во время неинвазивных тестов или при наличии ограниченных участков ишемии жизнеспособного миокарда. — Пограничный стеноз (50-70%) коронарных артерий (помимо главного ствола ЛКА) и отсутствие признаков ишемии миокарда при неинвазивном исследовании. — Незначимый стеноз коронарных артерий (менее 50%). — Высокий риск осложнений или смерти (возможная летальность – более 10-15%), за исключением тех случаев, когда он нивелируется ожидаемым значительным улучшением выживаемости или качества жизни.
Рекомендации по реваскуляризации миокарда с целью улучшения прогноза у больных стабильной стенокардией (ЕОК, 2006)
Класс I: — КШ при выраженном стенозе главного ствола ЛКА или значительном сужении проксимального сегмента левой нисходящей и огибающей коронарных артерий (А); — КШ при выраженном проксимальном стенозе 3-х основных коронарных артерий, особенно у больных со сниженной функцией левого желудочка или быстровозникающей или распространенной обратимой ишемией миокарда при функциональных пробах (А); — КШ при стенозе одной или 2-х коронарных артерий, в сочетании с выраженным сужением проксимальной части левой передней нисходящей артерии и обратимой ишемии миокарда при неинвазивных исследованиях (А); — КШ при выраженном стенозе коронарных артерий, в сочетании с нарушением функции левого желудочка и наличием жизнеспособного миокарда по данным неинвазивных тестов (В). Класс II а: — КШ при стенозе одной или 2-х коронарных артерий без выраженного сужения левой передней нисходящей артерии у больных, перенесших внезапную смерть или стойкую желудочковую тахикардию (В); — КШ при выраженном стенозе 3-х коронарных артерий у больных сахарным диабетом, у которых определяются признаки обратимой ишемии миокарда при функциональных пробах (С); — чрескожное вмешательство или КШ у больных с признаками обратимой ишемии миокарда, выявленной с помощью функциональных проб или частыми эпизодами ишемии при повседневной активности (С).
Рекомендации по реваскуляризации миокарда с целью уменьшения симптомов у больных стабильной стенокардией (ЕОК, 2006)
Класс I: — КШ при многососудистом поражении (если технически возможно) у больных с умеренно выраженными или выраженными симптомами, которые не удается контролировать с помощью медикаментзной терапии, если риск операции не превышает его возможную пользу (А); — чрескожное вмешательство при стенозе одной коронарной артерии (если технически возможно) у больных с умеренно выраженными или выраженными симптомами, которые не удается контролировать с помощью медикаментзной терапии, если риск вмешательства не превышает его возможную пользу (А); — чрескожное вмешательство при многососудистом поражении (если оно технически возможно и отсутствуют анатомические факторы риска) у больных с умеренно выраженными или выраженными симптомами, которые не удается контролировать с помощью медикаментозной терапии, если риск вмешательства не превышает его возможную пользу (А). Класс II а: — чрескожное вмешательство при стенозе одной коронарной артерии (если оно технически возможно) у больных с легкими или умеренно выраженными симптомами, которые для них неприемлемы, если риск вмешательства не превышает его возможную пользу (А); — КШ при стенозе одной коронарной артерии (если технически возможно) у больных с умеренно выраженными или выраженными симптомами, которые не удается контролировать с помощью медикаментозной терапии, если риск операции не превышает его возможную пользу (А); — КШ при стенозе нескольких коронарных артерий (если технически возможно) у больных с легкими или умеренно выраженными симптомами, которые для них неприемлемы, если риск операции не превышает его возможную пользу (А); — чрескожное вмешательство при стенозе нескольких коронарных артерий (если технически возможно) у больных с легкими или умеренно выраженными симптомами, которые для них неприемлемы, если риск вмешательства не превышает его возможную пользу (А). Класс II b: — КШ при стенозе одной коронарной артерии (если технически возможно) у больных с легкими или умеренно выраженными симптомами, которые для них неприемлемы, если риск операции не превышает расчетную ежегодную смертность (В).
Сексуальная активность Половой акт может спровоцировать развитие стенокардии, поэтому перед ним можно принять нитроглицерин. Ингибиторы фосфодиэстеразы (силденафил, тадафил и варденафил), применяемые для лечения сексуальной дисфункции, не следует использовать в сочетании с пролонгированными нитратами.
Современные немедикаментозные методы лечения стабильной стенокардии
Усиленная наружная контрапульсация Усиленная наружная контрапульсация (УНКП) – вспомогательный метод лечения рефрактерной стенокардии, который заключается в последовательном нагнетании воздуха в манжеты, наложенные на нижние конечности. Весь процесс синхронизирован с ЭКГ. Во время диастолы манжеты последовательно и быстро раздуваются от голеней к бедрам и ягодицам. Это приводит к увеличению диастолического и коронарного перфузионного давления, усилению кровоснабжения миокарда. Мгновенное откачивание воздуха из манжет в начале сокращения желудочков (систолы) снижает сосудистое сопротивление и разгружает работу сердца (снижает постнагрузку). Отсроченными эффектами процедур является увеличение доставки кислорода и снижение потребности миокарда в кислороде, а конечным результатом – увеличение перфузионного коронарного давления и коллатерального кровотока, повышение выработки оксида азота, увеличение ангиогенеза и, в целом, – уменьшение стенокардии. К противопоказаниям метода относятся: декомпенсированная хроническая сердечная недостаточность, тяжелая патология клапанного аппарата сердца, тяжелая неконтролируемая артериальная гипертония (АД выше 180/110 мм рт.ст.), злокачественные аритмии, тяжелая патология периферических сосудов, тяжелая варикозная болезнь с наличием трофических язв, высокая легочная гипертония, аневризма и тромбозы различных отделов аорты. В рандомизированном плацебоконтролируемом мультицентровом исследовании внешняя (наружная) контрапульсация снижала частоту приступов стенокардии, увеличивала время нагрузки до появления стенокардии. В исследовании принимали участие 142 больных с рефрактерной стенокардией и положительным нагрузочным тестом. Курс лечения – 35 сеансов, каждый продолжительностью по 1 часу. Группа активного лечения – 75 человек, давление в манжете – 300 мм рт.ст., 4-7 сеансов в неделю. Группа плацебо – 67 человек, давление в манжете – 75 мм рт.ст. В международном исследовании у 978 больных с рефрактерной стенокардией III-IV ФК при использовании этой методики наблюдалось улучшение состояния на один ФК у 81% больных, качество жизни больных существенно улучшалось. Клинические эффекты курса процедур EECP включали: сокращение частоты приступов стенокардии, повышение толерантности к физической нагрузке, улучшение крово-снабжения ишемизированного участка миокарда по данным радионуклидной сцинтиграфии миокарда с таллием. В последнее время накапливаются данные о положительном влиянии УНКП на улучшение эндотелиальной функции сосудов и снижение агрессии атеросклероза. Ударно-волновая терапия сердца (УВТ) УВТ является новой технологией, позволяющей неинвазивным образом улучшать кровоснабжение миокарда в зоне ишемии за счет образования новых капилляров. Принцип УВТ основан на механическом воздействии на ишемизированный миокард энергией акустической волны. При этом в зоне воздействия высвобождается ряд вазоактивных субстанций, включая оксид азота и эндотелиальный фактор роста сосудов, способствующих вазодилатации и неоангиогенезу. Однако эффективность УВТ продемонстрирована лишь в пилотных исследованиях, поэтому выраженная положительная динамика клинических проявлений стенокардии и объективных показателей перфузии миокарда требует подтверждения в крупных рандомизированных исследованиях. Трансмиокардиальная лазерная реваскуляризация (ТМЛР) Одним из новых методов хирургического лечения тяжелой стенокардии является трансмиокардиальная лазеротерапия. Этот метод официально применяется в США с 1998 года. В России ряд ведущих кардиологических клиник за последние 3-4 года также стали активно использовать трансмиокардиальную лазеротерапию. Эффективность метода связана с улучшением кровоснабжения миокарда за счет поступления крови из полости ЛЖ через вновь образованные 20-40 каналов диаметром 1 мм. Ряд исследований (BELTEF, PACIFIC) свидетельствует о значительных положительных эффектах данной методики (рост толерантности к нагрузкам, уменьшение класса стенокардии). ТМЛР проводится при торакотомии как одновременно с КШ, так и в качестве самостоятельной процедуры. Метод ТМЛР достаточно эффективен, он снижает ФК стенокардии, улучшает перфузию, функцию и метаболизм миокарда ЛЖ. Улучшение перфузии отмечается только в зонах лазерного воздействия при наличии жизнеспособного миокарда. Результаты 5-летнего наблюдения 80 больных с тяжелой рефрактерной стенокардией показали, что у 20% после ТМЛР с использованием высокоэнергетического СО2-лазера стенокардия полностью исчезает, а приблизительно у 90% больных ИБС функциональное состояние уменьшается на один класс, согласно Канадской классификации. Однако связанная с операцией смертность составляет 5-10%, а дополнительная смертность в течение 1 года – еще 10%
Реваскуляризация миокарда – широкое понятие, включающее как операцию КШ, так и различные виды ТКА. Наиболее известна и распространена БАП, которую можно сочетать с другими воздействиями на атеросклеротически измененную коронарную артерию: установкой металлического каркаса – эндопротеза (стента), выжиганием бляшки лазером, разрушением бляшки быстро вращающимся буром и срезанием бляшки специальным атеротомическим катетером. Непосредственная клиническая эффективность ТКА достаточно высока – прекращаются приступы стенокардии, улучшается сократительная функция ЛЖ. Однако, при всей простоте и очевидной целесообразности восстановления коронарного кровотока с помощью ТКА, остается нерешенным вопрос о предотвращении рецидива болезни в результате развития рестеноза, который возникает у 32-40% пациентов в течение 6 месяцев после вмешательства. Показанием для ТКА является, как правило, выраженная стенокардия при поражении одной или более коронарных артерий, плохо поддающаяся антиангинальной терапии, а неинвазивные тесты указывают на неблагоприятный прогноз естественного течения болезни. При определении сроков вмешательства следует учитывать профессию и пожелания больного. Стенозы должны быть доступны для катетерной технологии, а окклюзии иметь давность менее 3-х месяцев. При выраженном поражении основного ствола левой коронарной артерии предпочтительно хирургическое лечение, хотя в ряде случаев возможны ТКА и стентирование пораженной артерии. При сравнении результатов медикаментозного лечения и ТКА, последняя имеет преимущество по эффективности в ближайшие сроки после процедуры; при длительных сроках наблюдения различия исчезают. Коронарное шунтирование КШ с использованием венозных и артериальных трансплантатов получило достаточно широкое распространение. Низкие показатели смертности, высокая клиническая эффективность и увеличение продолжительности жизни больных свидетельствуют о преимуществе КШ перед медикаментозным лечением, особенно при многососудистых поражениях. При сравнении ТКА и КШ отмечаются идентичные клинические результаты, однако хирургический метод имеет преимущество у больных СД и у лиц с серьезными нарушениями сердечного ритма. ТКА не может быть выполнена в ряде случаев из-за ограничения технических возможностей и анатомических особенностей – протяженные окклюзии артерии, выраженный кальциноз. Дифференцированный подход к назначению того или иного метода лечения позволяет добиться лучших конечных результатов. Несмотря на расширение возможностей медикаментозного лечения больных ИБС, внедрение в клиническую практику ТКА со стентированием коронарных артерий, хирургические методы реваскуляризации миокарда остаются наиболее радикальным методом лечения ИБС. Показания к хирургической реваскуляризации миокарда – КШ, определяются выраженностью клиники стенокардии (III-IV ФК) и сегментарным сужением просвета коронарных артерий >70%. Показания к операции могут быть определены только на основании результатов КАГ и вентрикулографии с учетом данных клинического обследования. Шунтированию подлежат магистральные коронарные артерии и их крупные ветви первого порядка. Перенесенный ИМ не является противопоказанием к операции, и при сохраняющейся постинфарктной стенокардии рекомендуется выполнять вмешательство, не дожидаясь 4-6 месяцев, как это принято при благоприятном течении постинфарктного периода. Объем реваскуляризации миокарда определяется количеством пораженных артерий, снабжающих кровью жизнеспособный миокард. Каждая ишемизированная зона миокарда должна быть реваскуляризирована. Восстанавливать кровоснабжение в зоне постинфарктного кардиосклероза нецелесообразно. В настоящее время наметилась определенная тенденция к шунтированию максимально возможного числа коронарных артерий с помощью аутоартерий. С этой целью используют внутренние грудные артерии, лучевые артерии, правую желудочно-сальниковую и нижнюю надчревную артерии. Несмотря на вполне удовлетворительные результаты КШ, у 20-25% больных в течение 8-10 лет стенокардия возвращается. Такие пациенты рассматриваются как кандидаты для повторной операции. Чаще возврат стенокардии обусловлен прогрессированием коронаросклероза и поражением аутовенозных шунтов, что ведет к стенозу и облитерации их просвета. Этому процессу особенно подвержены шунты у больных с наличием ФР: АГ, СД, ГХС, курение, ожирение. Показаниями к КШ служат: ✓ тяжелая инвалидизирующая или изменяющая КЖ стенокардия (III-IV ФК), не поддающаяся максимальной лекарственной терапии; ✓ результаты неинвазивных исследований, при которых присутствуют низкая толерантность к ФН и выраженная ишемическая реакция на ЭКГ, при наличии функционально значимых (≥70%) стенозов одной и более коронарных артерий; ✓ стеноз основного ствола левой коронарной артерии ≥50%. Для принятия решения об операции важное значение имеют такие факторы, как наличие и тяжесть сопутствующих заболеваний, возраст, социальная активность пациента и его настроенность на хирургическое лечение. Сообщения последних лет об успешном оперативном лечении ИБС у пациентов с почечной недостаточностью, онкологическими заболеваниями, тяжелым СД показали, что в подобных ситуациях в каждом случае необходимо тщательно сопоставлять возможный риск и ожидаемую эффективность операции. Преклонный возраст сам по себе не является противопоказанием к операциям, однако пожилые пациенты с комплексом сопутствующих заболеваний подвержены существенно большему риску. Многие социальные и психологические факторы могут стать причиной категорического отказа больных от операции. Наличие гемодинамически значимых поражений основного ствола левой коронарной артерии, проксимальных сужений во всех трех основных коронарных сосудах или других изменений с вовлечением проксимального отдела передней нисходящей коронарной артерии предполагает положительное решение вопроса об операции. При указанных выше условиях больные даже с маловыраженной клинической картиной ИБС могут иметь несравнимо лучшие перспективы при хирургическом, нежели медикаментозном, лечении. Значительное нарушение функции ЛЖ – ФВ 25 мм рт.ст., при наличии клинически манифестированной СН существенно ухудшают прогноз как хирургического, так и медикаментозного лечения, однако в настоящее время не рассматриваются абсолютными противопоказаниями к хирургическому вмешательству
Источник: http://venus-med.ru/cardial/103-revaskulyarizaciya-miokarda.html
Источник: studfile.net
Определение реваскуляризации миокарда
Реваскуляризация мышцы сердца представляет собой определенные методики хирургического лечения коронарной ишемии. Оперативные способы восстановления кровоснабжения направлены на улучшение прогноза выживаемости, полную ликвидацию либо уменьшение симптомов стенокардии и других, на повышение качества жизни больного.
Показания к реваскуляризации миокарда заключаются в отсутствии стабильного результата при медикаментозной терапии либо выраженных противопоказаниях к таковой. Вот конкретные критерии:
- вариантная и нестабильная стенокардия при удовлетворительном общем состоянии пациента;
- риск развития осложнений после острого инфаркта сердечной мышцы;
- значительное сужение левой коронарной артерии;
- сердечная недостаточность, желудочковая тахикардия и аритмия;
- ишемическая болезнь миокарда с сужением артериального просвета на 50% и больше (независимо от наличия стенокардии).
По степени хирургического вмешательства различают прямую и непрямую формы операции. Факторами, влияющими на выбор определенного метода реваскуляризации миокарда, являются индивидуальные особенности сердечно-сосудистой системы больного, специфика клинической картины, риски развития ишемии и сопутствующие заболевания.
Решение о подобном оперативном вмешательстве принимается с учетом таких противопоказаний:
- аневризма сердечного левого желудочка;
- дисфункция клапанов;
- обширное поражение коронарных сосудов;
- онкологические заболевания;
- гибернирующий миокард;
- присутствие источника инфекции;
- кровотечение из других органов (открытое).
Таким образом, хирургические методы реваскуляризации миокарда направлены на полное восстановление сосудистого кровотока при неэффективности других методов лечения, острой форме ишемии и клинических к тому показаниях.
Методы прямой реваскуляризации миокарда
К прямым методам хирургического восстановления сердечных сосудов относятся в традиционные, общепринятые способы лечения. Это коронарное шунтирование и ангиопластика. Если первый метод представляет собой замену нефункционирующего участка артерии другим сосудом, то второй способ предполагает искусственное увеличение просвета, а значит – проходимости артерии.
Аортокоронарное шунтирование
Операция шунтирования предполагает исключение поврежденных участков артерии из системы кровоснабжения. Шунт выполняется из большой подкожной вены одной из конечностей (бедра или предплечья). Практикуется замена не более 5-6 штук за одну процедуру.
Анастомоз соединяет аорту с коронарной артерией ниже места ее закупорки, восстанавливая таким образом кровоснабжение. Процедура проводится при таких показаниях:
- стенокардия III, IV класса при неэффективности ее лечения другими методами;
- сужение просвета сосудов более чем на 1 мм;
- ярко выраженное уменьшение проходимости венечной артерии;
- атеросклероз (закупоривание сосудов холестериновыми бляшками) 2-3 крупных артерий.
Операция проводится на основании данных коронарографии, которая заключается во введении в систему кровеносных сосудов подсвечивающего вещества и просмотре на рентгене проблемных зон.
Читайте также: Коронарография сосудов сердца – последствия, методы исследования коронарных сосудов
Отмечается ряд противопоказаний, которые обязан учитывать хирург при определении соотношения пользы и вреда от коронарного шунтирования:
- дисфункция левого сердечного желудочка, выражающаяся в выбросе менее 25% крови (застойная недостаточность);
- почечная недостаточность;
- тяжелые состояния после инсульта;
- легочные заболевания;
- гипертония;
- онкология.
С учетом всего вышеперечисленного принимается решение о рисках и целесообразности проведения операции. Но ее плюсы несомненны: повышаются качественные показатели жизни и снижаются риски инфаркта, сердечной недостаточности и аритмии.
Стоит отметить, что усредненный срок службы таких шунтов составляет 5-6 лет. Далее потребуется шунтирование повторять.
Важно! Приемлемые возрастные показания для аортокоронарного шунтирования – от 30 до 55 лет. Более позднее вмешательство ограничивается обширным атеросклерозом даже мелких коронарных артерий, а также сосудов мозга.

Ангиопластика
Ангиопластика коронарных сосудов предполагает введение при помощи специального катетера определенного средства, увеличивающего артериальный просвет. Для нее применяются такие инструменты:
- баллонные катетеры;
- лазерные баллоны;
- стенты;
- атерэктомические катетеры.
Показания для ангиопластики соответствуют таковым для шунтирования, но ее цель заключается в максимальной отсрочке оперативного вмешательства. Но и после такой малоинвазивной операции возможны осложнения, напрямую зависящие от ее травматизма:
- сужение артерий – с 50% вероятностью, для предотвращения этого назначаются антагонисты кальция;
- нестабильность кровотока без образования тромба;
- тромбоз венечной артерии.
Противопоказания к методу ангиопластики:
- затрудненная проходимость левой артерии, которая питает непосредственно сердце;
- уменьшение просвета кровеносного сосуда, обеспечивающего неповрежденную часть миокарда;
- тяжелая дисфункция сердечного левого желудочка;
- обширные поражения сердечно-сосудистой системы;
- значительное повреждение артерии, питающей большой участок миокарда;
- терминальная или неконтролируемая гипертензия артерий;
- нарушение электролитных обменных процессов;
- анафилактические расстройства.
Процедуры ангиопластики проводятся под четким контролем коронарографии, а иногда и во время нее.
Баллонная ангиопластика
Наименьшее количество противопоказаний и относительное удобство в применении отдают предпочтение баллонному способу восстановления кровотока в сосудах. Операция проходит таким образом: через отверстие в бедре либо плече по артерии до закупоренного прохода продвигается катетер с баллоном, который по прибытии в назначенный участок 2-3 раза надувают до определенного уровня. Это позволяет механически расширить просвет в сосуде.
Стоит указать на то, что у четверти больных после баллонной ангиопластики те же артерии повторно подвергаются стенозу.

Коронарное стентирование
Процедура стентирования коронарных артерий тоже относится к малоинвазивным оперативным вмешательствам. Она заключается во введении в бедренный либо плечевой кровеносный сосуд катетера, несущего сложенный стент (металлическую сетку). В месте сужения просвета стент раскрывается, расширяя стенки и придавая нужный диаметр артерии. Процесс постоянно контролируется с помощью коронарографии, а может быть проведен и во время ее, так как считается безопасным и малотравматичным.

Коронарная атерэктомия
Такой метод хирургического лечения, как коронарная атерэктомия, предполагает срезание со стенок артерии холестериновой бляшки с дальнейшим удалением срезанного. Процесс происходит посредством атерэктомического катетера, снабженного острым ножом. Этот способ показан только при атеросклерозе сосудов, имеющих просвет не менее 3 мм, что связано с размерами самого катетера.
Лазерная реваскуляризация
Реваскуляризация лазерным методом проводится путем введения в артерию световода, который по достижении места сужения артерии лазерной энергией срезает холестериновую бляшку, не повреждая стенки сосуда.

Методы непрямой реваскуляризации миокарда
Непрямые методы реваскуляризации сердечной мышцы объединяют современные, слабо изученные способы увеличения просвета в коронарных артериях либо создания новой системы сосудов. Они, как правило, предназначены для пациентов, имеющих противопоказания к шунтированию и ангиопластике. Но спорные результаты либо их недостаточное количество не дают этим методам широкого распространения.
Трансмиокардиальная лазерная реваскуляризация
Эта методика является новым способом восстановить поставку крови к сердечной мышце. Трансмиокардиальная лазерная реваскуляризация заключается в создании в миокарде маленьких отверстий (диаметром по 1 мм) посредством сверхтонкого лазерного проводника, который подводится через небольшой разрез на груди. Цель такой процедуры – снабжение миокарда кровью, насыщенной кислородом, непосредственно из левого желудочка, и дальнейшее образование из проделанных отверстий артерий. Помимо этого, лазер разрушает миокардиальные аксоны, что ослабляет выраженный болевой эффект у пациента.
Показаниями к такому методу является невозможность проведения шунтирования или стентирования из-за атеросклероза многочисленных мелких сосудов.
Важно! Трансмиокардиальная лазерная реваскуляризация не требует для проведения остановки сердца. Она практически не приводит к осложнениям и отличается быстрым восстановительным периодом.

Ударно-волновая терапия
Новейшей экспериментальной методикой является и ударно-волновая терапия. Она заключается в воздействии на миокард акустической волны, что впоследствии стимулирует образование новых артерий в органе. Эта процедура бескровна и безболезненна, но спорные результаты не способствовали ее дальнейшему массовому применению.
Таким образом, методы реваскуляризации миокарда находятся в постоянном совершенствовании. Разрабатываются способы проведения шунтирования без использования аппарата искусственного кровообращения (на работающем сердце). Помимо этого, изобретаются новые бескровные или малоинвазивные методики воздействия на коронарную систему с целью избавления от атеросклероза.
Усовершенствованию способов реваскуляризации миокарда способствуют многочисленные тонкости ишемии и наличие у больного сопутствующих патологий, ограничивающие проведение прямых хирургических методов.
Но все это направлено на исправление последствий болезни. А чтобы убрать причину, важно придерживаться сбалансированного питания, уменьшить прием жиросодержащей пищи и избавиться от вредных привычек, в частности, курения. Это поможет значительно снизить риск образования холестериновых бляшек на стенках кровеносных сосудов и избежать атеросклероза с вытекающими последствиями.
Источник: lechiserdce.ru
Что такое реваскуляризация миокарда
Поражение среднего мышечного слоя сердца (миокарда), обусловленное нарушением циркуляции крови по коронарным артериям, имеет несколько клинических форм, некоторые из них вызывают необратимые изменения сердечной мышцы. Дефицит кровоснабжения (ишемия) возникает вследствие сужения просвета сосудов, которые питают миокард. Причиной снижения проходимости коронарных артерий и вен в большинстве случаев выступает атеросклероз (отложение холестериновых бляшек на сосудистых стенках).
При обращении к врачу пациента, имеющего жалобы на характерные для ишемической болезни сердца (ИБС) грудные боли, ему назначается проведение диагностического обследования, основным методом которого является коронарография (рентген сосудов с применением рентгеноконтрастного вещества). Результаты диагностики служат основой для назначения лечения. При выявлении определенных параметров возникают показания для кардинальной терапии, одним из методов которой является реваскуляризация.
Суть операции заключается в восстановлении сосудов, поврежденных вследствие воспалительных, некротических или склеротических процессов. Об успешности проведенного хирургического вмешательства свидетельствует степень достижения основных целей операции – возобновления нормального кровоснабжения миокарда, полного восстановления проходимости всех сердечных артерий и их ветвей. Своевременно проведенные манипуляции могут предотвратить необратимые изменения сердечной мышцы и повысить продолжительность жизни пациентов с ИБС.
К методам реваскуляризации прибегают в случае неудовлетворительной эффективности проводимого медикаментозного лечения или при наличии серьезных противопоказаний к применяемым в ходе терапии лекарственным средствам. Другими критериями, которые служат причиной для назначения пациенту оперативного лечения миокарда, являются:
- выраженное сужение основного ствола коронарного кровоснабжения (левой коронарной артерии);
- высокий риск развития осложнений после перенесенного инфаркта миокарда;
- острая сердечная недостаточность, желудочковая тахикардия;
- нестабильная стенокардия;
- ишемия миокарда, при которой наблюдается существенное уменьшение артериального просвета (на 50% и более).
Методы реваскуляризации миокарда
Цель хирургического лечения миокарда достигается путем соединения пораженных коронарных артерий со внешними сосудами (аортокоронарное шунтирование), расширения суженных участков с помощью установки специального каркаса (стентирование) или удаления холестериновых отложений, которые стали причиной закупорки сосудов. Все способы восстановления коронарного кровообращения имеют свои особенности, показания, противопоказания, преимущества и недостатки.
По степени вмешательства методы восстановления нарушенного кровоснабжения сердечной мышцы подразделяются на прямые и непрямые. Общепринятым стандартом лечения ишемии миокарда является прямая хирургическая реваскуляризация миокарда, к которой относится:
- Коронарное шунтирование – помогает восстановить коронарное кровоснабжение путем соединения аутотрансплантами (шунтами) аорты с коронарными артериями. Операция может проводиться как с применением специального оборудования, поддерживающего жизнедеятельность организма пациента при полной или частичной дисфункции сердца, так и без него.
- Эндоваскулярная коронароангиопластика – малоинвазивное (чрескожное, транслюминальное) вмешательство, к которому относится баллонная ангиопластика и стентирование. Отличительной характеристикой этих методов является отсутствие разрезов – вмешательство проводится путем чрескожной пункции под контролем рентгеновских лучей. Эти особенности существенно снижают операционный риск и период восстановления по сравнению с традиционной хирургической реваскуляризацией.
В кардиологической практике в 9–10% случаев у больных ИБС отмечается дистальный тип поражения венечных сосудов (холестериновые бляшки закупоривают множественные мелкие сердечные артерии). В отношении этой категории пациентов применение прямых методов вмешательства нецелесообразно ввиду большого количества пораженных участков и недоступности некоторых мелких артерий. Для лечения таких больных разработан метод непрямой реваскуляризации – трансмиокардиальная лазерная реваскуляризация (ТМЛР).
В основе метода ТМЛР лежит идея создания в стенке сердечных желудочков каналов, которые будут соединять миокард с афферентными сосудами, и кровь будет напрямую поступать из полости левого желудочка в сердечную мышцу. Операция выполняется с помощью лазеров (углекислотных или эксимерных), под воздействием которых в толще миокарда формируются каналы диаметром до 0,01 см. Закрытие отверстий происходит спустя 2–4 мес. после вмешательства, но лечебный эффект сохраняется более 2 лет.
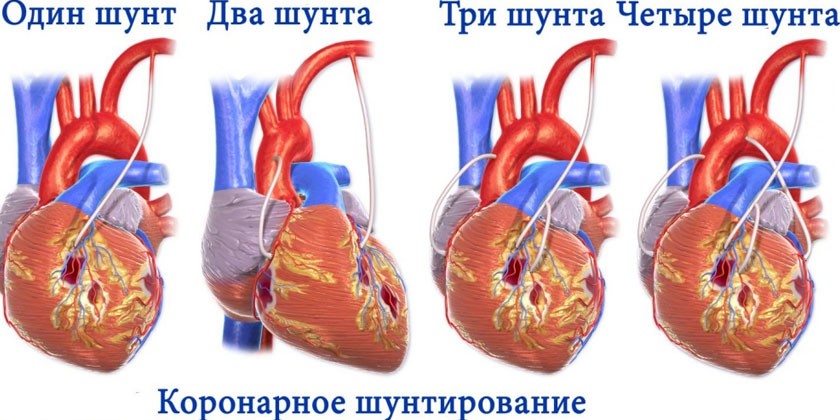
Коронарное шунтирование
При необходимости хирургического лечения патологий сердечно-сосудистой системы, связанных с нарушением проходимости сосудов, методом выбора традиционно является коронарное шунтирование. Суть операции заключается в создании обходных артериовенозных анастомозов (соединений между кровеносными сосудами без образования капиллярных сетей) с помощью шунтов. Графты (участки сосудов для трансплантации) для проведения операции могут выделяться открытым или эндоскопическим способом из лучевой, внутренней грудной артерий или большой подкожной вены ноги.
Коронарная реваскуляризация путем шунтирования является самой сложной и дорогостоящей из операций по восстановлению кровоснабжения миокарда, но по эффективности превосходит все известные методики. Операция осуществляется с применением аппарата искусственного кровообращения или на бьющемся сердце (при наличии риска ухудшения состояния пациента во время кратковременной остановки сердца).
Во время хирургических манипуляций (длящихся 3–4 ч.) от всех членов оперирующей команды (хирург, ассистенты, анестезиолог, перфузиолог – врач, контролирующий систему искусственной циркуляции крови, операционные сестры) требуется максимальная концентрация. Коронарное шунтирование проводится по следующему алгоритму:
- введение общего наркоза;
- выполнение разреза вдоль средней линии грудной клетки;
- блокировка главной аорты для минимизации кровопотери;
- забор вены или артерии (длиной 65–75 см) для шунтирования (материал выделяют, перевязывают, отрезают и промывают);
- введение прямого антикоагулянта (гепарина) с целью недопущения тромбообразования;
- подключение аппарата «искусственное сердце» для обеспечения кровообращения;
- вживление сосудов-имплантатов;
- «запуск» сердца, отключение аппарата искусственного кровообращения;
- нейтрализация гепарина в крови (введение Протамина сульфата) для улучшения свертываемости крови;
- дренирование раны, скрепление грудины металлическими швами, наложение швов.
Средняя продолжительность реабилитационного периода после шунтирования составляет 3 мес., на протяжении которых пациенту следует четко соблюдать рекомендации врача для минимизации риска закрытия вживленных шунтов. Этот метод реваскуляризации наряду с преимуществами имеет ряд недостатков, выраженность которых снижается при проведении шунтирования на работающем сердце:
|
Показания к проведению |
Противопоказания |
Преимущества метода |
Недостатки метода |
|
Стенокардия 3 и 4 классов; просвет между стенками сосудов сужен на 1 мм и более; проходимость венечной артерии существенно снижена; закупорка атеросклеротическими бляшками 2–3 крупных сосудов; желудочковые аритмии и тахикардии. |
Дисфункция левого желудочка сердца (выражается в уменьшении выброса крови на 75% и более); нарушения функционирования почек; постинсультное состояние; патологии легких; повышенное кровяное давление; онкологические заболевания; возраст после 55 лет; диффузный тип поражения венечных сосудов. |
Существенное улучшение сократимости миокарда; длительное сохранение результативности проведенного вмешательства (95% шунтов продолжают функционировать на протяжении 5 и более лет, 90% – 10 лет, 50% – 20 лет.). |
Длительный восстановительный период; высокая стоимость операции; большая вероятность возникновения послеоперационных осложнений (кровотечения, инфицирование, развитие сердечной недостаточности); серьезные косметические дефекты. |
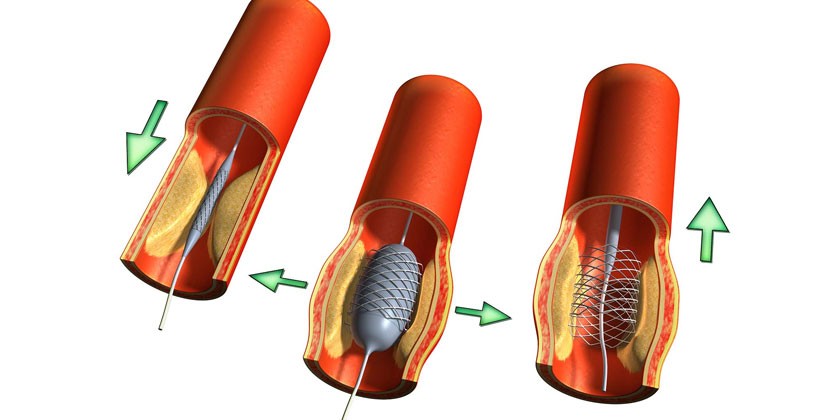
Стентирование
К малоинвазивным методикам восстановления суженных участков артерий относится внутрисосудистая операция с применением стентов – специальных тонких трубочек из металла, имеющих клетчатый каркас. После установления стента в пораженный сосуд, его раздувают с помощью баллона, за счет чего происходит расширение эндопротеза и увеличение сосудистого просвета. Манипуляции совершаются с применением местной анестезии ввиду отсутствия необходимости выполнения разрезов тканей.
Операция происходит в помещении, оборудованном рентген-аппаратурой, для осуществления постоянного контроля за процессом. Весь операционный процесс занимает 30–40 мин., на протяжении которых производятся следующие действия:
- Введение катетера, снабженного специальным баллончиком, который смонтирован со стентом, через бедренные или предплечные сосуды к устью суженной венечной артерии (при кальцифицированных стенозах для просверливания каналов прохождения катетера применяются ротаблаторы – высокоскоростные буры, покрытые алмазной крошкой).
- Раздувание баллона (при этом происходит расширение стента и вдавливание его во внутреннюю стенку сосуда).
- Сжатие и удаление баллона.
Минимально-инвазивный метод восстановления кровоснабжения миокарда может применяться не во всех случаях, а только при наличии показаний к его проведению. В остальных случаях результативность реваскуляризации, осуществленной с помощью стентирования, может оказаться малоэффективной:
|
Показания к проведению |
Противопоказания |
Преимущества метода |
Недостатки метода |
|
Стенокардия напряжения (провоцируемая незначительными физическими нагрузками); высокая вероятность инфаркта миокарда; необходимость повторного перекрытия просвета сосудов после проведенной ранее реваскуляризации одним из стандартных методов; начальная стадия обширного инфаркта миокарда (первые 6 часов после появления симптомов). |
Наличие аллергической реакции на йодсодержащие препараты; острая стадия хронических заболеваний; недостаточность функционирования внутренних органов; множественные сужения сосудов; наличие злокачественных новообразований. |
Минимальный риск развития осложнений; безвредное и безболезненное вмешательство (нет необходимости вводить общий наркоз и делать разрезы); короткий период восстановления. |
Риск развития аллергической реакции на вводимое для осуществления рентген-контроля вещество; образование гематом на месте прокола артерии; в 15–20% случаев происходит обратное сужение сосудистых стенок. |
Балонная ангиопластика
Одним из методов эндоваскулярной хирургии, применяемых для возобновления проходимости венечных сосудов, является коронарная реваскуляризация миокарда с применением ангиопластики. Этот вид вмешательства может применяться как самостоятельно, так и в сочетании со стентированием. Суть проводимых манипуляций сводится к введению через паховый доступ к месту склеротических уплотнений тонкой трубочки с прикрепленным баллоном. Расширение просвета достигается путем нагнетания воздуха в баллон.
Целью операции является максимальная отсрочка высокотравматичного хирургического вмешательства. Решение о возможности проведения малоинвазивной баллонной ангиопластики вместо традиционных методов хирургического лечения ИБС должен принимать специалист, учитывая имеющиеся показания и противопоказания:
|
Показания к проведению |
Противопоказания |
Преимущества метода |
Недостатки метода |
|
Стенозы в одной или нескольких венечных артериях, доступных катетеризации; отсутствие результативности медикаментозного лечения стабильной стенокардии. |
Поражение левой артерии; тяжелое состояние пациента; дисфункциональные расстройства левого желудочка сердца; серьезные патологии сердечно-сосудистой системы; неконтролируемая гипертензия; нарушение водно-электролитного обмена. |
Отсутствие общего наркоза; короткий послеоперационный период; минимальные косметические повреждения. |
В 50% случаев происходит рестеноз (повторное сужение сосудов), для его предотвращения назначаются антагонисты кальция; зачастую требуются повторные вмешательства; образование тромбов; нарушение кровотока; риск прободения (образования сквозного отверстия) коронарной артерии. |
Лазерная реваскуляризация
Возможность применения лазерного излучения для восстановления кровоснабжения миокарда была обнаружена сравнительно недавно, поэтому этот метод еще недостаточно изучен и пока относится к экспериментальным. Суть операции заключается в прожигании в сердечной мышце каналов, доходящих до полости желудочка сердца. Осуществляется поставленная задача с помощью подведения к сердцу специальных катетеров с проводниками. Доступ к стенкам желудочка обеспечивается путем выполнения торакотомии (рассечения грудной клетки).
Трансмиокардиальная лазерная реваскуляризация миокарда в настоящее время применяется только при невозможности проведения стандартного хирургического вмешательства. Ввиду наличия неоспоримых достоинств метода, он начинает пользоваться все большей популярностью:
|
Показания к проведению |
Противопоказания |
Преимущества метода |
Недостатки метода |
|
Выраженное атеросклеротическое поражение диффузного характера (поражены 2 и более артерии); сильные боли в загрудинной области, существенно снижающие качество жизни; рефрактерность (нечувствительность) стенокардии к медикаментозному лечению; индивидуальные морфологические особенности коронарного русла, которые препятствуют проведению прямой реваскуляризации. |
Порок сердца (врожденный или приобретенный); постинфарктная аневризма левого желудочка. |
Выраженный положительный клинический эффект; возможность реваскуляризации труднодоступных участков миокарда; низкий уровень риска развития осложнений во время операции и после нее; короткий период реабилитации (относительно прямых методов реваскуляризации миокарда); симпатическая денервация сердечной мышцы (устранение болевого синдрома). |
Существует риск термического и механического повреждения миокарда во время создания каналов с помощью лазера; отсутствие точных данных относительно принципов физиологического воздействия и механизма влияния лазерного излучения на организм. |
Ударно-волновой метод
Кратковременное воздействие ударных волн низкой мощности успешно используется в медицинской практике для лечения воспалительных заболеваний. Применение этого метода с целью реваскуляризации миокарда пока не имеет клинических доказательств эффективности и безопасности. Механизм ударно-волнового метода основан на дистанционном воздействии акустической волны на миокард, результатом чего становится двойной эффект:
- первичный (кратковременный) – расширение сосудов, улучшение кровотока;
- вторичный (долговременный) – высвобождение биологического фактора, который стимулирует рост новых сосудистых ветвей.
Ввиду недостаточности данных, свидетельствующих о безопасности ударно-волновой терапии при поражениях миокарда, метод на текущем этапе не получил широкого распространения и применяется только на договорной основе и при отсутствии серьезных сердечно-сосудистых патологий. Из преимуществ этой методики реваскуляризации можно выделить стимуляцию терапевтического ангиогенеза (сосудообразования), безболезненность и неинвазивность, к недостаткам относятся:
- риск усугубления атеросклеротических процессов;
- отсутствие достаточных обоснований безопасности и прогнозируемых последствий;
- высокая вероятность развития регенерационной гипертрофии (процесса замещения некротизированных тканей миокарда соединительной).
Источник: vrachmedik.ru
